biologi for Majors i
læringsresultater
- forstå forskellen mellem præ-mRNA og mRNA
efter transkription skal eukaryote præ-mRNA ‘ er gennemgå flere behandlingstrin, før de kan oversættes. Eukaryote (og prokaryote) tRNA ‘er og rRNA’ er gennemgår også behandling, før de kan fungere som komponenter i proteinsyntesemaskineriet.
mRNA-behandling
det eukaryote præ-mRNA gennemgår omfattende behandling, før det er klar til at blive oversat. De yderligere trin, der er involveret i eukaryot mRNA-modning, skaber et molekyle med en meget længere halveringstid end et prokaryot mRNA. Eukaryote mRNA ‘ er varer i flere timer, mens det typiske E. coli mRNA ikke varer mere end fem sekunder.
præ-mRNA ‘er overtrækkes først i RNA-stabiliserende proteiner; disse beskytter præ-mRNA’ et mod nedbrydning, mens det forarbejdes og eksporteres ud af kernen. De tre vigtigste trin i præ-mRNA-behandling er tilføjelsen af stabiliserings-og signalfaktorer ved molekylets 5′ og 3′ ender og fjernelse af mellemliggende sekvenser, der ikke specificerer de passende aminosyrer. I sjældne tilfælde kan mRNA-transkriptet “redigeres”, efter at det er transkriberet.
5′ Capping
mens præ-mRNA’ et stadig syntetiseres, tilsættes en 7-methylguanosin-hætte til 5 ‘ – enden af det voksende transkript ved hjælp af en fosfatbinding. Denne del (funktionel gruppe) beskytter det spirende mRNA mod nedbrydning. Derudover genkender faktorer involveret i proteinsyntese hætten for at hjælpe med at indlede oversættelse af ribosomer.
3′ Poly-A-hale
når forlængelsen er afsluttet, spaltes præ-mRNA ‘et af en endonuklease mellem en aauaaa-konsensussekvens og en GU-rig sekvens, hvilket efterlader AAUAAA-sekvensen på præ-mRNA’ et. 200 A-rester, kaldet poly-A-halen. Denne modifikation beskytter yderligere præ-mRNA ‘ et mod nedbrydning og signalerer eksporten af de cellulære faktorer, som transkriptionen har brug for til cytoplasmaet.
præ-mRNA-Splejsning
eukaryote gener er sammensat af eksoner, der svarer til proteinkodende sekvenser (eks-on betyder, at de udtrykkes), og mellemliggende sekvenser kaldet introner (intron betegner deres mellemliggende rolle), som kan være involveret i genregulering, men fjernes fra præ-mRNA under behandling. Intronsekvenser i mRNA koder ikke for funktionelle proteiner.
opdagelsen af introner kom som en overraskelse for forskere i 1970 ‘erne, som forventede, at præ-mRNA’ er ville specificere proteinsekvenser uden yderligere behandling, som de havde observeret i prokaryoter. Generne af højere eukaryoter indeholder meget ofte en eller flere introner. Disse regioner kan svare til regulatoriske sekvenser; den biologiske betydning af at have mange introner eller have meget lange introner i et gen er imidlertid uklar. Det er muligt, at introner bremser genekspression, fordi det tager længere tid at transkribere præ-mRNA ‘ er med masser af introner. Alternativt kan introner være ikke-funktionelle sekvensrester tilbage fra fusionen af gamle gener gennem hele evolutionen. Dette understøttes af det faktum, at separate eksoner ofte koder for separate proteinunderenheder eller domæner. For det meste kan sekvenserne af introner muteres uden i sidste ende at påvirke proteinproduktet.
alle et præ-mRNA ‘ s introner skal fjernes fuldstændigt og præcist før proteinsyntese. Hvis processen fejler med endda et enkelt nukleotid, ville læserammen for de genindtrådte eksoner skifte, og det resulterende protein ville være dysfunktionelt. Processen med at fjerne introner og genforbinde eksoner kaldes splejsning (Figur 1). Introner fjernes og nedbrydes, mens præ-mRNA stadig er i kernen. Splejsning sker ved hjælp af en sekvensspecifik mekanisme, der sikrer, at introner fjernes, og eksoner genforenes med nøjagtigheden og præcisionen af et enkelt nukleotid. Splejsningen af præ-mRNA ‘ er udføres af komplekser af proteiner og RNA-molekyler kaldet spliceosomer.
øvelsesspørgsmål
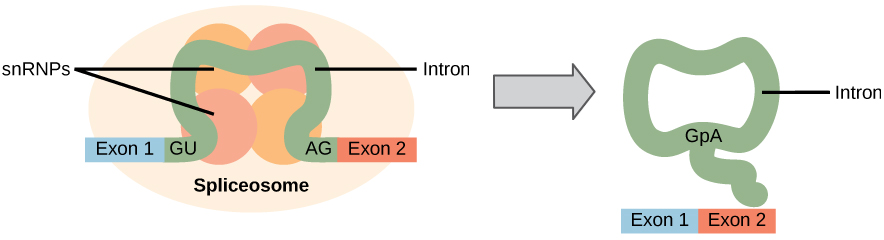
Figur 1. Præ-mRNA-splejsning involverer nøjagtig fjernelse af introner fra det primære RNA-transkript. Splejsningsprocessen katalyseres af proteinkomplekser kaldet spliceosomer, der er sammensat af proteiner og RNA-molekyler kaldet snrna ‘ er. Spliceosomer genkender sekvenser i 5 ‘og 3’ enden af intronen.
fejl i splejsning er impliceret i kræft og andre menneskelige sygdomme. Hvilke slags mutationer kan føre til splejsningsfejl?
Bemærk, at mere end 70 individuelle introner kan være til stede, og hver skal gennemgå splejsningsprocessen—ud over 5′ capping og tilsætning af en poly-A hale—bare for at generere et enkelt, oversætteligt mRNA-molekyle.
RNA-redigering i trypanosomer
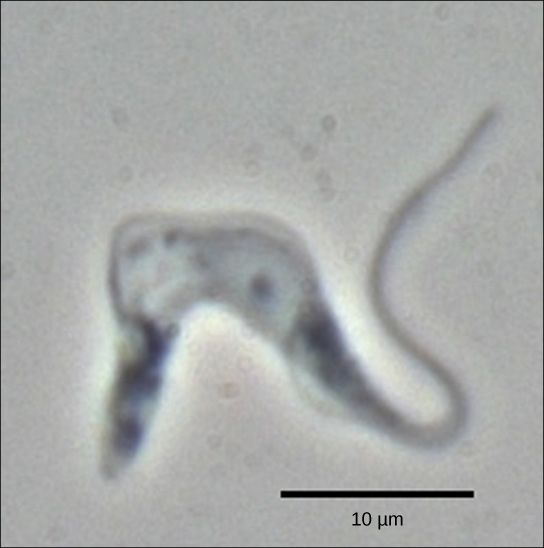
figur 2. Trypanosoma brucei er det forårsagende middel til sovesyge hos mennesker. MRNA ‘ erne for dette patogen skal modificeres ved tilsætning af nukleotider, før proteinsyntese kan forekomme. (kredit: ændring af arbejde af Torsten Ochsenreiter)
trypanosomerne er en gruppe af protosoer, der inkluderer patogenet Trypanosoma brucei, som forårsager sovesyge hos mennesker (figur 2). Trypanosomer og stort set alle andre eukaryoter har organeller kaldet mitokondrier, der forsyner cellen med kemisk energi. Mitokondrier er organeller, der udtrykker deres eget DNA og menes at være resterne af et symbiotisk forhold mellem en eukaryot og en opslugt prokaryot. Mitokondrie-DNA fra trypanosomer udviser en interessant undtagelse fra Det centrale dogme: deres præ-mRNA ‘ er har ikke de korrekte oplysninger til at specificere et funktionelt protein. Normalt skyldes dette, at mRNA mangler flere U-nukleotider. Cellen udfører et yderligere RNA-behandlingstrin kaldet RNA-redigering for at afhjælpe dette.
andre gener i mitokondriegenomet koder for 40 – til 80-nukleotidguide RNA ‘ er. Et eller flere af disse molekyler interagerer ved komplementær baseparring med nogle af nukleotiderne i præ-mRNA-transkriptet. Guide-RNA ‘et har imidlertid mere a-nukleotider end præ-mRNA’ et Har u-nukleotider at binde med. I disse regioner løber guide RNA ud. 3 ‘-enderne af guide-RNA ‘er har en lang poly-u-hale, og disse U-baser indsættes i regioner i præ-mRNA-transkriptet, hvor guide-RNA’ erne er sløjfet. Denne proces er helt medieret af RNA-molekyler. Det vil sige, guide RNA ‘ er—snarere end proteiner—tjener som katalysatorer i RNA-redigering.
RNA-redigering er ikke kun et fænomen af trypanosomer. I mitokondrier af nogle planter redigeres næsten alle præ-mRNA ‘ er. RNA-redigering er også blevet identificeret hos pattedyr som rotter, kaniner og endda mennesker. Hvad kunne være den evolutionære årsag til dette yderligere trin i præ-mRNA-behandling? En mulighed er, at mitokondrierne, der er rester af gamle prokaryoter, har en lige så gammel RNA-baseret metode til regulering af genekspression. Til støtte for denne hypotese varierer redigeringer foretaget til præ-mRNA ‘ er afhængigt af cellulære forhold. Selvom det er spekulativt, kan processen med RNA-redigering være et holdover fra en primordial tid, hvor RNA-molekyler i stedet for proteiner var ansvarlige for katalyserende reaktioner.
Prøv Det
Bidrage!
forbedre denne sidelær mere