Článek
John Plante*, Chelsea Eason, Alan Snyder, Dirk Elston
Oddělení Dermatologie a Dermatologické Chirurgie, Medical University of South Carolina, Charleston, Jižní Karolína
Lichen planopilaris (LPP) je primární jizevnaté alopecie se vyznačuje tím, svědění, citlivost, folikulární trny a erytém v aktivní phase1-3. Ačkoli přesná etiologie není známa, patogeneze zahrnuje chronický zánět zprostředkovaný lymfocyty, který může nakonec vést k nevratnému, zjizvení vypadávání vlasů jeho selektivní destrukcí vlasového folikulu1,2. Tři varianty LPP existují a patří klasické podobě, čelní fibrotizující alopecie (FFA), a Graham-Little-Piccardi-Lassueur syndrom (progresivní alopecie vlasové pokožky, axillae, obočí, a pubis)2. LPP často dokazuje, refrakterní na standardní terapii a takto nepředvídatelné, recidivující průběh, často vede k značně snížené kvalitě life1,2,4,5. Zde dále diskutujeme o naší nedávné studii týkající se použití tofacitinibu při léčbě vzpurného LPP6.
četné terapie byly použity k léčbě LPP s proměnnou úspěšností1-3,5,7-9. Protože v současné době k dispozici léčba obvykle nevede k opětovný růst vlasů, řízení směřuje klesá míra vypadávání vlasů, kontrole příznaků a snížení inflammation2,9. Terapie první linie zahrnují intralezionální a vysoce účinné topické kortikosteroidy, ale mohou mít za následek atrofii pokožky hlavy a ohrozit úspěch budoucí transplantace vlasů. Jiné lokální látky mají menší riziko atrofie a zahrnují inhibitory kalcineurinu takrolimus a pimekrolimus2. I když to není kontrolovat podkladové zánětlivý proces, a to jak lokální a perorální minoxidil může být také použit k maximalizaci opětovný růst vlasů u pacientů, kteří také trpí zdědil vzor alopecie – téměř 50% population9,10. Další systémové terapie patří hydroxychlorochin, mykofenolát mofetil, cyklosporin, methotrexát, thalidomid, doxycyklin, retinoidy, pioglitazon, 5-alfa reduktázy, a krátkodobé prednisolone1,2,9. Nedávné studie naznačují potenciál nízké dávky perorální naltrexon, platelet-rich plasma injekce, a non-farmakologické intervence jako excimer laser, ale žádná nebyla jednotně effective5,7,8. Zatímco kousky vlasů a rozšíření mohou zvýšit objem a pokrýt alopecické oblasti, je třeba postupovat opatrně, aby nedošlo k trakci9.
v nedávno publikované studii jsme zkoumali potenciál topických a perorálních (systémových) formulací tofacitinib6. Tofacitinib je Janus kinázy (JAK) 1/3 inhibitor s účinností proti několika imunitní zprostředkované dermatologické podmínky, včetně atopické dermatitidy, alopecie areata, a vitiligo11-14. Jeho imunomodulační aktivita je zprostředkována inhibicí signální dráhy JAK/STAT12, 13. V LPP se interferony podílely na usnadnění náboru lymfocytů a ztrátě imunitních privilegií vyboulených epiteliálních buněk1. Prostřednictvím účinků tofacitinibu na cestu JAK/STAT může být tento zánět zprostředkovaný interferonem snížen, čímž se zlepší příznaky a zabrání se další destrukci folikulů1, 11-13.
Jsme zkoumali léčebný potenciál tofacitinib v léčbě refrakterní LPP prostřednictvím retrospektivní graf review6. Podle znalostí autorů se jedná o druhou studii zkoumající použití tofacitinibu v léčbě LPP1. Naše studie zahrnovala devět pacientů, u kterých selhala jiná léčba – tři použité topické, pět použitých perorálních a jeden použil obě formulace.
bylo dosaženo příznivé počáteční odpovědi u všech pacientů kromě jednoho. Zbývající subjekt špatně reagoval na topickou léčbu, ale zlepšil se systémovou léčbou tofacitinibem. I když je absolutní počet pacientů malý, u pacientů na systémové léčbě byl trend k lepší klinické odpovědi ve srovnání s pacienty na lokální terapii. Čas příznivé odezvy v rozmezí od 1 do 7 měsíců, s 5 a 8 pacientů prokazují zlepšení během prvních 3 a 5 měsících léčby, respektive.
Naše současné praxi vzor je léčit rychle progresivní onemocnění s krátkou průběhu prednison či cyklosporin a pak zkuste přejít na lokální inhibitory kalcineurinu terapie, pokud je to možné (viz Obrázek 1). Podskupina pacientů dosáhne remise svého onemocnění pioglitazonem v dávkách 15-45 mg denně. Pacienti by měli být upozorněni na označenou indikaci, smíšené údaje týkající se účinnosti a krabicové varování o rakovině močového měchýře při dlouhodobém užívání. Naší praxí není pokračovat v pioglitazonu po maximálně 9 měsících se zvyšujícími se dávkami v krocích. Pomocné látky zahrnují naltrexon v dávce 5 mg denně a N-acetylcystein v dávkách 600-1200 mg třikrát denně. Excimerový laser, ruční úzkopásmová UVB nebo laserová čepice s nízkou intenzitou se často používá jako doplňková terapie u pacientů s částečnou odpovědí. Hydroxychlorochin může být občas přínosem, ale většina pacientů uvedených na naší klinice již selhala v léčbě hydroxychlorochinem. Ti, kteří neodpovídají, mohou vyžadovat léčbu methotrexátem, mykofenolát mofetilem nebo tofacitinibem. Výsledky naší nedávné studie poskytují další podporu myšlence, že jak lokální, tak systémový tofacitinib může být životaschopnými způsoby doplňkové léčby v refrakterních případech. Poruchy vlasů často reagují pomalu a my přehodnocujeme v 3měsíčních intervalech, abychom určili odpověď na terapii a potřebu eskalace.
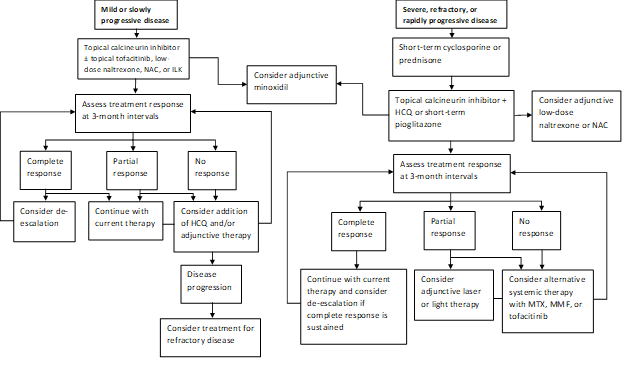
Obrázek 1: Postupné Zpracování Algoritmus pro LPP
NAC, N-acetylcystein; ILK, intralezionální kortikosteroidy; HCQ, hydroxychlorochin; MTX, methotrexát, MMF, mykofenolát mofetil
při zvažování použití tofacitinibu v praxi musí lékaři vyvážit přínosy tohoto léku s jeho riziky. Naše kohorta zaznamenala pouze malé laboratorní abnormality (jedna na lokální a dvě na systémové terapii), které nevyžadovaly zásah. Nicméně, poskytovatelé by měli být vědomi možných vedlejších účinků při předepisování tohoto léku, včetně zvýšené riziko infekce, cytopenie, hyperlipidemie, jaterní a renální abnormality, stejně jako potenciál pro tromboembolické events14-16. Zatímco topické formulace prokázala nižší plazmatické koncentrace než se systémovou protějšek, vedlejší nežádoucí účinky a laboratorní abnormality byly stále hlášeny s aktuální therapy13.
i když jsou naše výsledky slibné, musí být interpretovány po zvážení několika omezení. Použili jsme retrospektivní design studie a nebyli jsme schopni použít validované měřítko závažnosti onemocnění, jako je lichen Planopilaris Activity Index (LPPAI)1,3. LPPAI je vhodný pro prospektivní studie a poskytuje standardizovaný nástroj, pomocí kterého mohou poskytovatelé přímo porovnávat výsledky napříč různými způsoby léčby. Známky a příznaky, jako je erytém, citlivost, přítomnost folikulárních trny, a postižené oblasti byly použity k hodnocení léčebné odpovědi, ale budoucí studie by měly rovněž zahrnovat měření kvality života. Možnost zaujatosti pozorovatele nelze vyloučit, protože naše studie byla nezaslepená a nerandomizovaná.
kromě toho celá naše kohorta používala tofacitinib dodatečně, což ztěžuje posouzení nezávislého příspěvku léku. V předchozí studii, část (N=5) z kohorty používá tofacitinib jako monoterapie, a většina pacientů dosaženo příznivých výsledků, ale tato studie byla také omezena jeho malé velikosti vzorku a retrospektivní design1.
Aktuální studie jsou omezeny jejich malé velikosti vzorku a retrospektivní studie, návrhy, a dobře-navržen tak, prospektivní studie jsou nutně zapotřebí. Doporučujeme postupný přístup k terapii, aby se minimalizovalo riziko nežádoucích účinků. Riziko trvalého zjizvení musí být zváženo proti riziku závažných nežádoucích účinků s ohledem na jednotlivé faktory pacienta a komorbidity a pacienti by měli být aktivními partnery při rozhodování. Transplantace vlasů může být zvážena, jakmile je dosaženo kontroly onemocnění a zánět ustoupil. Je důležité si uvědomit, že agresivní terapie jako prednison či cyklosporin je obvykle potřeba během týdnů po transplantaci, aby se zabránilo vzplanutí onemocnění. I po úspěšné transplantaci lze očekávat postupné opotřebení transplantovaných chloupků, ale data naznačují, že pacienti jsou obecně spokojeni s výsledky a zjistili, že transplantace zlepšuje kvalitu života.
Zkratky
LPP, lichen planopilaris; FFA, čelní fibrotizující alopecie; JAK, Janus kinázy; STAT, signální transduktor a aktivátor transkripce proteiny; LPPAI, Lichen Planopilaris Index Aktivity.
střet zájmů
autoři nehlásí žádný střet zájmů.
- Yang CC, Khanna T, Sallee B, et al. Tofacitinib pro léčbu lichen planopilaris: série případů. Dermatol Ther. 2018; 31 (6): e12656. doi: 10.1111 / d.12656
- Babahosseini H, Tavakolpour S, Mahmoudi H, et al. Lichen planopilaris: retrospektivní studie o charakteristikách a léčbě 291 pacientů. J Dermatolog Léčit. 2019; 30(6): 598–604. doi:10.1080/09546634.2018.1542480
- Chiang C, Sah D, Cho BK, et al. Hydroxychlorochin a lichen planopilaris: účinnost a zavedení systému bodování indexu aktivity Lichen Planopilaris. J Am Acad Dermatol. 2010; 62(3): 387-392. doi: 10.1016 / j. jaad.2009.08.054
- Alirezaei P, Ahmadpanah M, Rezanejad A, et al. Ve srovnání s kontrolami mají jedinci s Lichen Planopilaris větší depresi, nižší sebeúctu a nižší kvalitu života. Neuropsychobiologie. 2019; 78(2): 95-103. doi:10.1159/000499135
- Jha AK. Plazma bohatá na destičky jako doplňková léčba lichen planopilaris. J Am Acad Dermatol. 2019; 80 (5): e109-e110. doi: 10.1016 / j. jaad.2018.09.013
- Plante J, Eason C, Snyder A, et al. Tofacitinib v léčbě lichen planopilaris: retrospektivní přehled . J Am Acad Dermatol. 2020; S0190-9622 (20)30979-8. doi:10.1016 / j. jaad.2020.05.104
- Lajevardi V, Salarvand F, Ghiasi M, et al. Účinnost a bezpečnost perorální nízké dávky naltrexonu oproti placebu u pacientů s lichen planopilaris: randomizovaná kontrolovaná klinická studie . J Dermatolog Léčit. 2020; 1-5. doi:10.1080/09546634.2020.1774488
- Lee B, Elston DM. Použití naltrexonu v dermatologických podmínkách. J Am Acad Dermatol. 2019; 80(6): 1746-1752. doi: 10.1016 / j. jaad.2018.12.031
- Bolduc C, Sperling LC, Shapiro J. primární jizevnatá alopecie: Lymfocytární primární jizevnaté alopecie, včetně chronické kožní lupus erythematodes, lichen planopilaris, čelní fibrotizující alopecie, a Graham-Little syndrom. J Am Acad Dermatol. 2016; 75(6): 1081-1099.
- Vano-Galvan S, Trindade de Carvalho L, Saceda-Corralo D, et al. Perorální minoxidil zlepšuje tloušťku vlasů v lichen planopilaris . J Am Acad Dermatol. 2020; S0190-9622 (20)30566-1. doi: 10.1016 / j. jaad.2020.04.026
- Tegtmeyer K, Zhao J, Maloney NJ, et al. Off-label studie na tofacitinib v dermatologii: přehled . J Dermatolog Léčit. 2019; 1–11. doi: 10.1080/09546634.2019.1673877
- Montilla AM, Gomez-Garcia F, Gomez-Arias PJ, et al. Scoping přehled o užívání léků zaměřených na jak / STAT dráhy v atopické dermatitidy, Vitiligo a Alopecia Areata. Dermatol Ther (Heidelb). 2019; 9(4): 655–683. doi: 10.1007 / s13555-019-00329-y
- Hosking AM, Juhasz M, Mesinkovska NA. Lokální inhibitory Janus kinázy: přehled aplikací v dermatologii. J Am Acad Dermatol. 2018; 79(3): 535–544. doi: 10.1016 / j. jaad.2018.04.018
- Shreberk-Hassidim R, Ramot Y, Zlotogorski a. Janus inhibitory kinázy v dermatologii: systematický přehled. J Am Acad Dermatol. 2017; 76(4): 745-753.e19. doi: 10.1016 / j. jaad.2016.12.004
- Xeljanz/Xeljanz XR (tofacitinib) . New York, NY: divize Pfizer Laboratories společnosti Pfizer Inc. https://labeling.pfizer.com/showlabeling.aspx?id=959; 2019. Přístup K 7. Červenci 2020.
- FDA. Bezpečnost soud shledá riziko krevní sraženiny v plicích a na smrt s vyšší dávkou tofacitinib (Xeljanz, Xeljanz XR) u pacientů s revmatoidní artritidou; FDA, aby prošetřila. https://www.fda.gov/drugs/drug-safety-and-availability/safety-trial-finds-risk-blood-clots-lungs-and-death-higher-dose-tofacitinib-xeljanz-xeljanz-xr; 2019. Přístup K 6. Červenci 2020.