chroman
chroman Chemické Vlastnosti,Použití,Výroba
Anorganické sloučeniny
chromanu Draselného, běžně známý jako tarapacaite, je anorganická sloučenina, která je žlutá orthorhombic nebo hexagonální krystal při pokojové teplotě. Relativní hustota je 2.732, a bod tání 968 °C. To je toxický a může se rozpustí ve vodě za vzniku alkalického chromanu ion hydrolýze roztoku. A je nerozpustný v alkoholu a etheru. Po přidání kyseliny se žlutý roztok chromanu draselného změní na oranžovou, což je barva dichromanu. Tam je rovnováha mezi konverze chromanu a dichromanu v roztoku: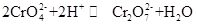
Když kyselina se přidává k roztoku chromanu draselného, rovnováha posune směrem generování dichromanu draselného, a když alkalický je přidán dichroman draselný řešení, rovnováha se posune ve směru generování chromanu draselného. Chroman má oxidační vlastnosti, a může reagovat s redukčním činidlem v alkalickém prostředí k formě Cr(OH)4-(a to CrO2-). Přidáním různých řešení, respektive obsahující baryum ion, vést iontů stříbra a iontů k roztoku chromanu draselného bude tvořit odpovídající nerozpustný chroman: chroman barnatý BaCrO4 (žlutý), vést chromanu olovnatého pbCrO4 (žlutá), chroman stříbrný Ag2CrO4(cihlově červená). A přítomnost chromátových iontů může být prokázána charakteristickou barvou těchto nerozpustných chromátů. Chroman draselný lze použít jako analytické činidlo, okysličovadlo, mořidlo, inhibitor kovové rzi a použít pro analýzu stopových Stop barya a stříbra. Může být také použit jako surovina pro opalovací a medicínský průmysl a další sloučeniny chrómu. Chromit Fe(CrO2)2 prášek může být použit jako surovina a kalcinovaný hydroxidem draselným, vápenec (dolomit) ve vzduchu, a poté se extrahuje s síran draselný roztok pro získání chromanu draselného.
výše uvedené informace upravuje Xiao Nan z Chemicalbook.
chroman ukazatel metoda
chroman ukazatel metoda, také známý jako Moore (Mohr), je srážecí titrační metoda (stříbrná metoda), který používá chroman draselný (K2CrO4) jako indikátor a dusičnanu stříbrného (AgNO3) jako standardní řešení. Tato metoda se používá hlavně pro stanovení chlorových iontů (Cl -) nebo bromidových iontů (Br -). Před stanovením stanovení přidejte malé množství K2CrO4 jako indikátor a poté titrujte standardním roztokem AgNO3. Po zahájení titrace se nejprve vysráží sraženina bílého (chloridu stříbrného) nebo světle žlutého (bromidu stříbrného). Když Cl-nebo Br-sráží kvantitativně, trochu přebytek dusičnanu stříbrného roztok způsobí, že koncentrace Ag+ se náhle zvyšuje, aby okamžitě generovat cihlově červená stříbrný chromát (Ag2CrO4) srážky, což naznačuje, že koncový bod titrace. Množství indikátoru a kyselost roztoku jsou dva hlavní problémy této titrační metody. Pokud K2CrO4 koncentrace je příliš vysoká, barva titrační roztok bude příliš hluboko bránit pozorování srážení Ag2CrO4 barva v end; pokud K2CrO4 koncentrace je příliš nízká, příliš značné množství roztoku dusičnanu stříbrného, bude zapotřebí po kvantitativním vysrážení halogenidů stříbra generovat stříbrný chromát srážek na pokyn koncový bod titrace, který bude výsledky titrační chyba zvyšuje. Při použití 0,1 mol / l roztoku AgNO3 k titraci 0.1mol / l halogenid, pokud je koncentrace K2CrO4 5× 10-3mol / l, chyba koncového bodu je pouze + 0,06%, což lze předpokládat, že přesnost výsledku analýzy není ovlivněna. Indikátor K2CrO4 metodu nelze provádět v kyselém nebo alkalickém roztoku, protože K2CrO4 budou převedeny na dichroman draselný (K2Cr2O7) v malé hodnotě pH, a Ag+ se sráží v podobě oxidu stříbrného (Ag2O), když je hodnota pH je příliš vysoká. Obvykle je vhodný rozsah kyselosti pH = 6,5~ 10,5, ale pokud jsou v roztoku amonné soli, je vhodná kyselost roztoku pH = 6,5~7,2.
metoda indikátoru chromanu draselného může být použita pouze pro přímou titraci Cl-nebo Br-iontů a výsledek titrace je jejich celkový při koexistenci. Tato metoda není vhodná pro stanovení jodidu draselného iontu (I-) nebo thiokyanatanu draselného iontu (SCN-), protože jsou příliš snadno vstřebává sedimentací a koncový bod je nejasný. Tato metoda také není vhodná pro titraci Ag+ s Cl-, ale Ag+ může být stanovena pomocí titrace, tj. přidávat nadměrné množství NaCl standardní řešení ve zkušebním roztoku, a pak použít AgNO3 standardní roztok titrovat přebytek Cl-ionty. V roztoku budou všechny kationty, které mohou tvořit sraženiny s CrO2-4 nebo anionty, které se mohou vysrážet s Ag+, interferovat s určením. Metoda indikátoru chromanu draselného se používá hlavně pro stanovení iontů Cl ve velmi zředěném roztoku, jako je stanovení nečistot Cl-v pitné vodě a průmyslových výrobcích.
dichroman draselný
dichroman draselný, také známý jako červený kamenec draslík, je oranžovo-červený triklinický krystal nebo jehlicovitý krystal. Hustota je 2,676 g / cm3. Teplota tání je 398 °C. Je rozpustný ve vodě a nerozpustný v ethanolu. Má silné oxidační vlastnosti a rozkládá se na 1300 °C.
Ve výrobě, dichroman draselný se používá vždy představit chromu, aby se smalt barevné, když taje. Je to barvivo barevné titanové mléčné žluté glazury a titanové žluté glazury a použitá dávka je obecně 0,06%~0,12%. Dichroman draselný a oxid měďnatý lze také smíchat – použít k získání zelené, bambusové zelené, ovocné zelené a jiné barevné glazury. Tyto barevné glazury jsou však obecně méně lesklé kvůli vlivu chromátu.
barevná glazura získaná z oxidu chromitého nebo dichromanu draselného (sodného) je často žlutozelená kvůli valenční změně chromových iontů v procesu tavení. Dichroman draselný se také běžně používá k výrobě různých zelených pigmentů a růžových pigmentů.
dichroman draselný by měl splňovat požadované cíle: obsah dichromanu draselného ≥ 99%, obsah chloridu (Cl) ≤ 0,08%, ve vodě nerozpustný ≤ 0,05%.
výše uvedené informace sestavuje Yaoyao z Chemicalbook.
rozpustnost ve vodě (g/100 ml)
rozpuštěné gramy na 100 ml vody při různých teplotách (°c):
60 g/10 °C; 63.7 g/20 °C; 66.7 g/30 °C; 67.8 g/40 °C
70.1 g/60 °C; 74.5 g/90 °C
Toxicity
Viz chroman sodný
Chemické vlastnosti
Citronově žluté orthorhombic krystal; Rozpustný ve vodě, nerozpustný v alkoholu
Aplikace
Používá se jako analytické činidlo, oxidační činidlo, mořidlo a kovové inhibitor koroze;používá se pro výrobu chroman,který se používá jako antioxidant a mořidlo tisku a barvení. Používá se pro inkoust, barvy, smalt, kovovou korozi atd., používá se hlavně při výrobě chemických činidel a pigmentů.
Příprava
neutralizační metoda: Dichroman draselný se rozpustí v matečném louhu a ve vodě a směs se přidá do reaktoru. Dále přidejte hydroxid draselný za míchání k provedení neutralizační reakce. Vyrobený chroman draselný je slabě alkalický a poté se odpaří pro koncentraci, ochladí se pro krystalizaci, oddělí se a vysuší, aby se získaly hotové produkty chromanu draselného.
K2Cr2O7 + 2KOH → 2K2CrO4 + H2O
oddělené matka alkohol, budou vráceny k rozpouštění krok pro rozpouštění dichroman draselný.
chemické vlastnosti
citronově žluté krystaly
chemické vlastnosti
chroman draselný (VI) je žlutá krystalická pevná látka.
použití
chroman draselný (K2CrO4) je rozpustný ve vodě a používá se k výrobě jasně žlutých inkoustů a barevných pigmentů. Používá se také jako činidlo v chemických laboratořích a jako mordant pro „fixaci“ barviv v barevných textiliích.
používá
používá se jako oxidační činidlo.
Používá
Má omezené použití v smalty, konečnou úpravu kůže, odolnost proti korozi kovů, jsou nahrazeny sodná sůl; jako činidlo v analytické chemii.
definice
ChEBI: draselná sůl sestávající z iontů draslíku a chromanu v poměru 2:1.
definice
sůl obsahující ionCrO42-.
Definice
chromanu draselného: světlé yellowcrystalline pevné, K2CrO4, solublein vodě a nerozpustný v alkoholu;kosočtverečný; r.d. 2.73; m.p. 968.3°C; rozkládá bez varu. Vyrábí se průmyslově pražením práškové chromitové rudy potassiumhydroxidem a vápencem a vyluhováním výsledné škváry horkým roztokem síranu draselného. Potassiumchromát se používá v kůžidokončení, jako textilní mordant, a vsamely a pigmenty. V laboratořipoužívá se jako analytickýreagent a jako indikátor. Stejně jako ostatní sloučeniny chrómu (III) je toxický při požití nebo vdechnutí.
obecný popis
chroman draselný je žlutá krystalická pevná látka. Chroman draselný je rozpustný ve vodě. Primárním nebezpečím je ohrožení životního prostředí. Měly by být podniknuty okamžité kroky k omezení jeho šíření do životního prostředí. Chroman draselný se používá při chemické analýze, při výrobě pigmentů pro barvy a inkousty, jako fungicid a při výrobě dalších sloučenin chrómu.
vzduch & reakce vody
rozpustné ve vodě.
Reaktivita Profil
Oxidační činidla, např. chroman , může reagovat s redukčními činidly k výrobě tepla a produktů, které mohou být plynné (což způsobuje přetlak uzavřených nádobách). Samotné produkty mohou být schopné dalších reakcí (jako je spalování ve vzduchu). Chemická redukce materiálů v této skupině může být rychlá nebo dokonce výbušná, ale často vyžaduje iniciaci (teplo, jiskra, katalyzátor, přidání rozpouštědla). Výbušné směsi anorganických oxidačních činidel s redukčními činidly často přetrvávají nezměněné po dlouhou dobu, pokud je zabráněno zahájení. Takové systémy jsou typicky směsi pevných látek, ale mohou zahrnovat jakoukoli kombinaci fyzikálních stavů. Některá anorganická oxidační činidla jsou soli kovů, které jsou rozpustné ve vodě; rozpouštění zředí, ale nezruší oxidační sílu takových materiálů. Organické sloučeniny mají obecně určitou redukční sílu a mohou v zásadě reagovat se sloučeninami v této třídě. Skutečná reaktivita se velmi liší s identitou organické sloučeniny. Anorganická oxidační činidla mohou prudce reagovat s aktivními kovy, kyanidy, estery a thiokyanáty.
nebezpečí
toxické při požití a inhalaci.
zdravotní riziko
inhalace způsobuje lokální podráždění sliznic; pokračující podráždění nosu může vést k perforaci nosní přepážky. Požití může způsobit násilnou gastroenteritidu, oběhový kolaps, vertigo, kóma a toxickou nefritidu; požití nadměrného množství může být fatální. Kontakt s očima způsobuje silné podráždění a konjunktivitidu. Opakované nebo dlouhodobé expozici prachu, mlhy, nebo řešení může způsobit dermatitidu; kontakt s přestávky v kůži může způsobit `chrome rány“ se objevuje jako pomalé hojení, hard-lemované vředy, které zanechávají oblasti náchylné k infekci.
nebezpečí požáru
chování při požáru: může zvýšit intenzitu požáru při kontaktu s hořlavými materiály. Chladné nádoby a rozlitý materiál s velkým množstvím vody.
bezpečnostní profil
potvrzený karcinogen s experimentálními tumorigenními údaji. Poisonpožití, intravenózní, subkutánní aintramuskulární cestou. Experimentalteratogen. Další experimentální reprodukovatelnéúčinky. Hlášeny údaje o lidských mutacích. Výkonný oxidační činidlo. Při zahřátísložení vydává toxické výpary K2O. Používá se jako mořidlo pro vlnu, při oxidacia ošetření barviv na materiálech. Viz také sloučeniny chromu.
potenciální expozice
chroman draselný se používá při tisku: fotomechanické zpracování; chrome-produkce pigmentu; a vlny konzervačních metod; barviva, pigmenty, barvy a laky; jako oxidační činidlo; analytické činidlo; v elektrolytické pokovování; výbušniny.
Doprava
UN1479 Oxidační solid, n.o.s., Třída Nebezpečnosti: 5.1; Štítky: 5.1-Oxidační Činidlo, Technický Název Požadované. UN3288 Toxické látky, anorganická, n.o.s., Třída nebezpečnosti: 6.1; Štítky: 6.1-Jedovaté materiály, Technické Jméno povinné
Metody Čištění
Krystalizovat z vodivost vody (0,6 g/mL při teplotě 20o), a suché to mezi 135o a 170o.
Nekompatibility
silný oxidant. Násilné reakce s hořlavinami, organickými látkami, práškovými kovy nebo snadno oxidovatelnými látkami. Kontakt s hydroxylaminem, hydrazin způsobuje výbuch.