Elektrony V Mušle
![]()
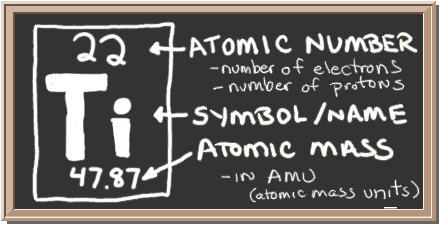
podívejte se na tabuli. Toto pole vlevo obsahuje všechny informace, které potřebujete vědět o jednom prvku. Říká vám hmotnost jednoho atomu, kolik kusů je uvnitř a kde by měl být umístěn na periodické tabulce.
nyní pracujeme se čtvrtou tečkou/řádkem v tabulce prvků. Můžete mít snadný způsob, jak zjistit počet elektronů v neutrálním atomu, ale umístění těchto elektronů je trochu složitější. Podívejme se na uspořádání elektronů v základních prvcích (levá a pravá strana tabulky) periody čtyři a složitější uspořádání přechodových prvků (uprostřed řádku). Pokud si myslíte, že je to trochu přes hlavu, vraťte se a podívejte se na prvky 1-18, které mají organizace, které jsou trochu jednodušší.
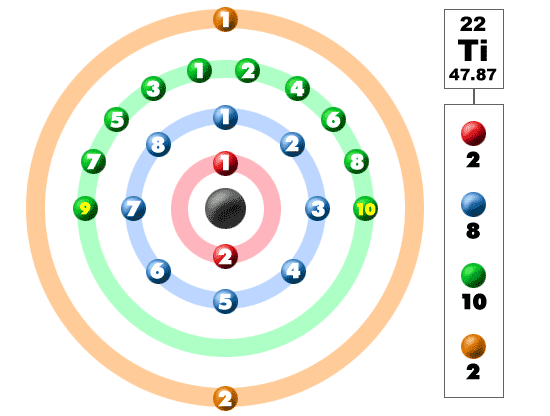
podívejte se na obrázek níže. Každá z těch barevných koulí je elektron. V atomu se elektrony točí kolem středu, nazývaného také jádro. Elektrony jsou rádi v samostatných skořápkách / orbitálech. Jak se dozvíte více o atomové struktuře, zjistíte, že elektrony nezůstávají v definovaných oblastech kolem jádra. Nacházejí se v oblacích, které mohou mít různé tvary, které zahrnují koule a činky podobné tvary. Takže pamatujte, když se podíváte na náš rozpis, že elektrony nejsou vždy v pěkném čistém pořadí, jak je ukázáno zde.
tento prvek je jedním z přechodových prvků, který neumisťuje další elektrony do vnějšího pláště,ale do toho pod ním. Pro čtvrté období / řádek všechny tyto elektrony vytvářejí třetí skořápku na maximálně 18 elektronů. Nezapomeňte, že prvních osm bylo umístěno během naší cesty přes třetí období / řádek. Čtvrtý řádek periodické tabulky má přechodné kovy v rozmezí od Skandia (21) po zinek (30).
Titan je kov. Není to jen tak ledajaký kov, je to přechodný kov. Jako přechodný kov má speciální elektronovou konfiguraci. Přidává svůj další elektron do třetí skořápky, ne nejvzdálenější čtvrtou skořápku. S konfigurací 2-8-10-2 je titan na světě a je připraven se spojit s dalšími prvky. Vyrábí mnoho přírodních sloučenin s halogeny a kyslíkem. Vzhledem k tomu, že Titan je tam se čtyřmi extra elektrony, je poměrně flexibilní a tvoří mnoho sloučenin.