Veraflox (pradofloxacin) Perorální Suspenze pro Kočky
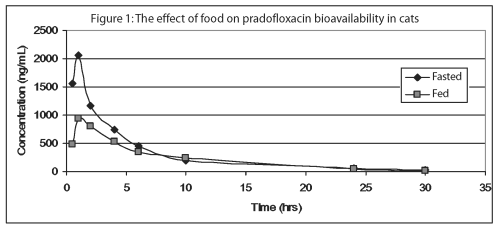
Přibližně 30% z celkové koncentrace léku se váže na plazmatické proteiny v koncentraci léčiva v rozmezí od 150 do 1500 ng/mL. Při podávání perorální suspenze kočkám nalačno v dávkách od 2, 5 mg/kg do 10 mg/kg je pozorováno zvýšení koncentrací léčiva úměrné dávce. Vzhledem k jeho krátký eliminační poločas, tam je minimální pradofloxacin akumulace po opakovaném denní správy.
Farmakodynamika:
Farmakodynamika byla stanovena pomocí in vitro citlivost, která ukázala, patogeny Pasteurella multocida, Staphylococcus pseudintermedius a Streptococcus spp. měl pradofloxacin MIC90 ≤0, 015 až 0, 12 ug / ml. Farmakodynamiku metriky (Cmax/ MIC90 a AUC/MIC90) byly odhadnuty pomocí lineární regresní analýzy volného léčiva v ustáleném stavu pradofloxacin farmakokinetika parametrů z postil kočky a pradofloxacin MIC90 hodnotu 0.12 ug/mL. Intervaly spolehlivosti 95% ohledně předpokládaných průměrných hodnot Cmax/MIC90 a AUC/MIC90 byly 15 až 17 a 70 až 81. Byl učiněn závěr, že velikost Cmax/MIC90 a AUC/MIC90 hodnoty je prediktivní výrobku účinnost při perorálním podání dávky 7,5 mg/kg tělesné hmotnosti pradofloxacin kapalný přípravek je podáván nalačno kočky. Kromě toho, účinnost byla prokázána pro kočky v dávce 7,5 mg/kg tělesné hmotnosti a fed svobodné volby, nebo do dvou hodin po podání, v poli studovat.
mikrobiologie:
VERAFLOX je baktericidní, s aktivitou proti gramnegativním, grampozitivním a anaerobním bakteriím. Mechanismus účinku je dvojí cílení prostřednictvím inhibice DNA gyrázy a topoizomerázy IV.
minimální inhibiční koncentrace (Mic) pro pradofloxacin proti Pasteurella multocida, Streptococcus canis, Staphylococcus aureus, Staphylococcus felis, a Staphylococcus pseudintermedius izolován od kožní infekce (rány a abscesy) u koček v USA studie z roku 2008 na rok 2009 jsou uvedeny v Tabulce 3. Pouze dva izoláty ze dvou případů selhání léčby pradofloxacinem měly zvýšené Mic pradofloxacinu (nehemolytický Staph. aureus-MIC = 2 µg / mL; E. coli-MIC = 4 µg/mL).
Tabulka 3. Činnost VERAFLOX proti Patogenům Izolovaným z Koček Léčených VERAFLOX v Klinické Studii v USA v roce 2008.
|
Onemocnění |
Patogen |
Klinický Výsledek Léčby |
Počet Izolátů |
Odběru Vzorku (Čas Relativní k Léčbě) |
MIC50 µg/mL |
MIC90 µg/mL |
MIC Rozsah µg/mL |
|
Kožní Infekce |
Pasteurella multocida |
Úspěch |
Pre-Léčba |
≤0.004 – 0.03 |
|||
|
Selhání |
Pre-Léčba |
≤0.004 – 0.015 |
|||||
|
Streptococcus canis |
Úspěch |
Pre-Léčba |
0.03 – 0.25 |
||||
|
Selhání |
Pre-Léčba |
0.06 – 0.12 |
|||||
|
Staphylococcus aureus |
Úspěch |
Pre-Léčba |
0.015 – 0.12 |
||||
|
Selhání |
|||||||
|
Staphylococcus felis |
Úspěch |
Pre-Léčba |
0.03 – 0.12 |
||||
|
Selhání |
Pre-Léčba |
||||||
|
Staphylococcus pseudintermedius |
Úspěch |
Pre-Léčba |
0.03 – 0.06 |
||||
|
Selhání |
Pre-Léčba |
Účinnost
klinická účinnost VERAFLOX byla prokázána v multi-site (16 stránek) terénní studie. V této maskované a randomizované studii byla účinnost verafloxu srovnávána s placebovou kontrolou (vehikulum bez účinné látky). Z 282 koček zařazených do této studie bylo 190 léčeno verafloxem jednou denně v dávce 7,5 mg / kg (3 .4 mg / lb) tělesné hmotnosti po dobu 7 po sobě jdoucích dnů a 92 bylo léčeno placebem jednou denně v dávce 0, 3 mL / kg tělesné hmotnosti po dobu 7 po sobě následujících dnů. Databáze účinnosti zahrnovala 182 koček: 66 koček léčených placebem (vehikulem) a 116 koček léčených verafloxem. Analýza této databáze účinnosti ukázala, že míra vyléčení byla vyšší ve skupině VERAFLOX v den 15, jak je shrnuto v tabulce 4. Míra vyléčení ve studii byla stanovena přibližně 15 dní po zahájení léčby. Statistické hodnocení primární účinnosti léčby (Studie Léčby) ukázal, že VERAFLOX byla odlišná od placeba s 73.4% VERAFLOX studie léků proti 38.9% placebo studie léčí.
Tabulka 4: Den 15 Klasifikace případů
|
Léčba Skupiny |
Procenta Léčí |
|
VERAFLOX N= 116 |
73.4% |
|
Placebo N= 66 |
38.9% |
|
P-hodnota |
Zvíře Bezpečnost
Bezpečnost Cílového Zvířete Obor: Bezpečnost byla hodnocena u 32 zdravých, 12-týdenní koťata podáván VERAFLOX jednou denně v dávkách 0, 7.9, 23.7, nebo 39.5 mg/kg (0, 1, 3, a 5 násobku doporučené dávky) po dobu 21 po sobě jdoucích dnů. Doplňková kontrola (0X) a vysoká dávka (5X) zvířat byla udržována po dobu 45 dnů po ukončení léčby.
ve skupině 3x a 5X byl statisticky významný pokles neutrofilů, lymfocytů a monocytů ve srovnání s kontrolami. Během léčebného období měla jedna 3x kočka a tři 5x kočka absolutní počet neutrofilů pod referenčním rozsahem. Výsledky cytologie kostní dřeně odpovídající supresi kostní dřeně (myeloidní hypoplazie) byly pozorovány u 3x neutropenických koček a dvou ze tří 5X neutropenických koček. 3x kočka byla neutropenická poslední den studie před plánovanou eutanazií, zatímco absolutní hodnoty neutrofilů u tří 5x koček se vrátily k normálu buď během léčby, nebo po ukončení léčby.
nejčastějším abnormálním klinickým nálezem byly měkké výkaly. Zatímco toto bylo pozorováno jak u léčených, tak u kontrolních skupin, bylo pozorováno častěji u 3x a 5X koťat.
Studie Bezpečnosti Očí: Oční bezpečnost byla hodnocena u 20 zdravých dospělých koček pomocí pradofloxacin v kapslích podává perorálně, jednou denně v dávkách 30 mg/kg a 50 mg/kg po dobu 23 dnů. U následujících zkoumaných očních parametrů nebyly pozorovány žádné účinky: oční vyšetření, ERGs a optická koherentní tomografie. Kočky, které dostávaly pradofloxacin v dávce 50 mg / kg / den, vykazovaly mírný úbytek hmotnosti. Kočky užívající 30 a 50 mg/kg / den pradofloxacinu vykazovaly hypersalivaci a zvracení po celou dobu studie. U koček léčených pradofloxacinem bylo zaznamenáno snížení počtu bílých krvinek v závislosti na dávce. Jedna kočka příjem 30 mg/kg/den pradofloxacin vykazovaly minimální photoceptor degenerace na světelné a elektronové mikroskopie typu, které se lišily od enrofloxacin léčených koček (komparátor použitý v této studii); účinky pradofloxacin na tyto změny sítnice není znám.
pilotní studie Toxicity: ve studii perorální toxicity dostávaly 4 kočky pradofloxacin v dávce 50 mg / kg / den po dobu 25 dnů. Všechny kočky vykazovaly zvracení a hypersalivaci. Jedna kočka vystavoval fluorochinolon-indukované neurologické příznaky (snížená pohyblivost, ohromující, a vokalizace) 5. Den studie.
podmínky uchovávání
uchovávejte při teplotě do 30°C (86°F).
po úvodním otevření prokázal Veraflox stabilitu po otevření po dobu 60 dnů.
JAK DODÁVÁ
|
Kód Číslo |
Láhev Velikost |
|
15 mL |
|
|
30 mL |
NADA 141-344, Schválený FDA
84364593 / 84364607, R.0
Vyrobeno v Německu
© 2012 Bayer HealthCare LLC
Bayer Bayer Kříž a VERAFLOX jsou registrované ochranné známky společnosti Bayer.
VERAFLOX je chráněn následujícím patentem USA 6,323,213.
Bayer HealthCare LLC, Animal Health Division, Shawnee Mission, Kansas 66201, U. S. a.