Veraflox (Pradofloxacin) Suspension zum Einnehmen für Katzen
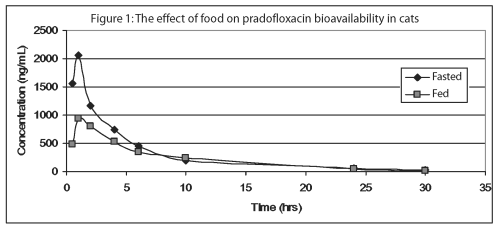
Ungefähr 30% der gesamten Wirkstoffkonzentrationen sind in Wirkstoffkonzentrationen von 150 bis 1500 ng / ml an Plasmaproteine gebunden. Dosisproportionale Erhöhungen der Arzneimittelkonzentrationen werden beobachtet, wenn die Suspension zum Einnehmen nüchternen Katzen in Dosen von 2,5 mg / kg bis 10 mg / kg verabreicht wird. Aufgrund seiner kurzen Eliminationshalbwertszeit ist die Akkumulation von Pradofloxacin nach mehrmaliger täglicher Verabreichung minimal.
Pharmakodynamik:
Die Pharmakodynamik wurde unter Verwendung der In-vitro-Empfindlichkeit bestimmt, die die Erreger Pasteurella multocida, Staphylococcus pseudintermedius und Streptococcus spp. Pradofloxacin-MHK90 von ≤0,015 bis 0,12 ug/ml aufwies. Die pharmakodynamischen Metriken (Cmax/ MHK90 und AUC/MHK90) wurden unter Verwendung einer linearen Regressionsanalyse der pharmakokinetischen Parameter von Pradofloxacin im Steady-State von nüchternen Katzen und eines Pradofloxacin-MHK90-Wertes von 0,12 ug/ml geschätzt. Die 95% -Konfidenzintervalle über die vorhergesagten mittleren Cmax/MHK90- und AUC/MHK90-Werte betrugen 15 bis 17 bzw. 70 bis 81. Es wurde der Schluss gezogen, dass die Größe der Cmax/MHK90- und AUC/MHK90-Werte die Wirksamkeit des Arzneimittels vorhersagt, wenn eine orale Dosis von 7,5 mg/kg Körpergewicht der flüssigen Pradofloxacin-Formulierung an nüchterne Katzen verabreicht wird. Darüber hinaus wurde in einer Feldstudie die Wirksamkeit bei Katzen gezeigt, die 7,5 mg / kg Körpergewicht erhielten und nach freier Wahl oder innerhalb von zwei Stunden nach der Dosierung gefüttert wurden.
Mikrobiologie:
VERAFLOX wirkt bakterizid gegen gramnegative, grampositive und anaerobe Bakterien. Der Wirkungsmechanismus ist dual Targeting durch Hemmung der DNA-Gyrase und Topoisomerase IV.
Die minimalen Hemmkonzentrationen (MICs) für Pradofloxacin gegen Pasteurella multocida, Streptococcus canis, Staphylococcus aureus, Staphylococcus felis und Staphylococcus pseudintermedius, die aus Hautinfektionen (Wunden und Abszesse) bei Katzen in einer US-Feldstudie von 2008 bis 2009 isoliert wurden, sind in Tabelle 3 aufgeführt. Nur zwei Isolate aus zwei Fällen von Pradofloxacin-Behandlungsversagen hatten erhöhte Pradofloxacin-MICs (nicht hämolytische Staph. aureus – MHK = 2 µg/ml; E. coli – MHK = 4 µg/ml).
Tabelle 3. Aktivität von VERAFLOX gegen Krankheitserreger, die aus Katzen isoliert wurden, die mit VERAFLOX in einer klinischen Studie in den USA im Jahr 2008 behandelt wurden.
|
Krankheit |
Pathogen |
Klinisches Behandlungsergebnis |
Anzahl der Isolate |
Probenentnahme (Zeit relativ zur Behandlung) |
MHK50 µg/ml |
MHK90 µg/ml |
MHK-Bereich µg/ml |
|
Hautinfektionen |
Pasteurella multocida |
Erfolg |
Vorbehandlung |
≤0.004 – 0.03 |
|||
|
Versagen |
Vorbehandlung |
≤0.004 – 0.015 |
|||||
|
Streptococcus canis |
Erfolg |
Vorbehandlung |
0.03 – 0.25 |
||||
|
Versagen |
Vorbehandlung |
0.06 – 0.12 |
|||||
|
Staphylococcus aureus |
Erfolg |
Vorbehandlung |
0.015 – 0.12 |
||||
|
Versagen |
|||||||
|
Staphylococcus felis |
Erfolg |
Vorbehandlung |
0.03 – 0.12 |
||||
|
Versagen |
Vorbehandlung |
||||||
|
Staphylococcus pseudintermedius |
Erfolg |
Vorbehandlung |
0.03 – 0.06 |
||||
|
Versagen |
Vorbehandlung |
Wirksamkeit
Die klinische Wirksamkeit von VERAFLOX wurde in einer Feldstudie an mehreren Standorten (16 Standorte) nachgewiesen. In dieser maskierten und randomisierten Studie wurde die Wirksamkeit von VERAFLOX mit einer Placebokontrolle (Vehikel ohne Wirkstoff) verglichen. Von den 282 Katzen, die an dieser Studie teilnahmen, wurden 190 einmal täglich mit 7,5 mg/kg VERAFLOX behandelt (3.4 mg / lb) Körpergewicht an 7 aufeinanderfolgenden Tagen und 92 wurden einmal täglich mit 0,3 ml / kg Körpergewicht an 7 aufeinanderfolgenden Tagen mit Placebo behandelt. Die Wirksamkeitsdatenbank umfasste 182 Katzen: 66 mit Placebo (Vehikel) behandelte Katzen und 116 mit VERAFLOX behandelte Katzen. Die Analyse dieser Wirksamkeitsdatenbank zeigte, dass die Heilungsrate in der VERAFLOX-Gruppe am Tag 15 höher war, wie in Tabelle 4 zusammengefasst. Die Heilungsraten der Studie wurden ungefähr 15 Tage nach Therapiebeginn bestimmt. Die statistische Auswertung des primären Wirksamkeitsendpunkts (Studienkuren) zeigte, dass sich VERAFLOX von Placebo mit 73,4% VERAFLOX-Studienkuren gegenüber 38,9% Placebo-Studienkuren unterschied.
Tabelle 4: Fallklassifizierung an Tag 15
|
Behandlungsgruppe |
Prozent Kuren |
|
VERAFLOX N= 116 |
73.4% |
|
Placebo N= 66 |
38.9% |
|
P-Wert |
Tiersicherheit
Zieltiersicherheitsstudie: Die Sicherheit wurde an 32 gesunden, 12 Wochen alten Kätzchen untersucht, denen VERAFLOX einmal täglich in Dosen von 0, 7,9, 23,7 oder 39,5 mg / kg (0-, 1-, 3- und 5-fache der empfohlenen Dosis) an 21 aufeinanderfolgenden Tagen verabreicht wurde. Zusätzliche Kontroll- (0X) und hochdosierte (5X) Tiere wurden 45 Tage nach Beendigung der Behandlung beibehalten.
Es gab statistisch signifikante Abnahmen von Neutrophilen, Lymphozyten und Monozyten in den 3X- und 5X-Gruppen im Vergleich zu den Kontrollen. Während des Behandlungszeitraums wiesen eine 3X-Katze und drei 5X-Katzen absolute Neutrophilenzahlen unterhalb des Referenzbereichs auf. Die Ergebnisse der Knochenmark-Zytologie, die mit der Knochenmarksuppression (myeloische Hypoplasie) übereinstimmten, wurden bei der 3X neutropenischen Katze und zwei der drei 5X neutropenischen Katzen beobachtet. Die 3X-Katze war am letzten Tag der Studie vor der geplanten Euthanasie neutropenisch, während sich die absoluten Neutrophilenwerte für die drei 5X-Katzen entweder während der Behandlung oder nach Beendigung der Behandlung wieder normalisierten.
Der häufigste abnormale klinische Befund war weicher Kot. Während dies sowohl in der behandelten als auch in der Kontrollgruppe beobachtet wurde, wurde es häufiger bei den 3X- und 5X-Kätzchen beobachtet.
Okuläre Sicherheitsstudie: Die Augensicherheit wurde bei 20 gesunden erwachsenen Katzen untersucht, die Pradofloxacin in Kapseln erhielten, die einmal täglich in Dosen von 30 mg / kg und 50 mg / kg über 23 Tage oral verabreicht wurden. Bei den folgenden untersuchten Augenparametern wurden keine Auswirkungen beobachtet: ophthalmische Untersuchungen, ERGs und optische Kohärenztomographie. Katzen, die 50 mg /kg / Tag Pradofloxacin erhielten, zeigten einen leichten Gewichtsverlust. Katzen, die 30 und 50 mg/kg/Tag Pradofloxacin erhielten, zeigten während der gesamten Studie Hypersalivation und Erbrechen. Bei den mit Pradofloxacin behandelten Katzen wurden dosisabhängige Verringerungen der Anzahl der weißen Blutkörperchen festgestellt. Eine Katze, die 30 mg / kg / Tag Pradofloxacin erhielt, zeigte eine minimale Photorezeptordegeneration auf Licht- und Elektronenmikroskopie eines Typs, der sich von Enrofloxacin-behandelten Katzen unterschied (in dieser Studie verwendeter Komparator); Die Auswirkungen von Pradofloxacin auf diese Netzhautveränderungen sind unbekannt.
Pilotstudie zur Toxizität: In einer Studie zur oralen Toxizität erhielten 4 Katzen Pradofloxacin in einer Dosis von 50 mg/kg/Tag über einen Zeitraum von 25 Tagen. Alle Katzen zeigten Erbrechen und Hypersalivation. Eine Katze zeigte am Tag 5 der Studie Fluorchinolon-induzierte neurologische Anzeichen (verminderte Mobilität, Staffelung und Vokalisierung).
Lagerbedingungen
Unter 30°C (86°F) lagern.
Nach dem ersten Öffnen hat VERAFLOX eine Gebrauchsstabilität von 60 Tagen gezeigt.
WIE GELIEFERT
|
Codenummer |
Flasche Größe |
|
15 ML |
|
|
30 ML |
NADA 141-344, genehmigt durch FDA
84364593 / 84364607, R.0
Made in Germany
© 2012 Bayer HealthCare LLC
Bayer, das Bayer-Kreuz und VERAFLOX sind eingetragene Marken von Bayer.
VERAFLOX ist durch das folgende US-Patent 6,323,213 geschützt.
Bayer HealthCare LLC, Abteilung Tiergesundheit, Shawnee Mission, Kansas 66201, USA