Échographie oculaire B-Scan
Vitré
Dans un œil jeune et sain, le vitré est relativement écholucent. Cependant, à mesure que l’œil vieillit, le vitré subit une synérèse et des opacités vitreuses peu réfléchissantes peuvent être détectées. Une séparation postérieure du vitré (une affection bénigne de l’œil vieillissant) peut se produire et est représentée par une ligne mobile, fine et peu réfléchissante sur le balayage B.
Voir l’image ci-dessous.
 et décollement vitreux postérieur observé avec un vieillissement normal de l’œil.
et décollement vitreux postérieur observé avec un vieillissement normal de l’œil. D’autres conditions ou maladies du vitré qui peuvent être détectées par ultrasons comprennent l’hyalose des astéroïdes, une autre affection bénigne du vitré où les sels de calcium s’accumulent dans la cavité vitréenne. Le calcium est relativement dense et, par conséquent, produit de multiples opacités vitrées très réfléchissantes.
Voir l’image ci-dessous.
 hyalose de l’astéroïde. Les savons de calcium dans cet état font que les points dans la cavité vitrée sont beaucoup plus brillants que ceux observés avec des hémorragies vitrées.
hyalose de l’astéroïde. Les savons de calcium dans cet état font que les points dans la cavité vitrée sont beaucoup plus brillants que ceux observés avec des hémorragies vitrées. Une hémorragie vitrée peut survenir dans plusieurs situations différentes, comme après un traumatisme ou une déchirure de la rétine ou comme une complication du diabète sucré ou une occlusion de la veine rétinienne. Le schéma échographique d’une hémorragie vitreuse dépend de son âge et de sa gravité. Les hémorragies légères fraîches apparaissent sous forme de petits points ou de zones linéaires d’opacités vitreuses mobiles peu réfléchissantes, tandis que dans les hémorragies plus anciennes plus graves, le sang s’organise et forme des membranes. Les membranes forment de grandes interfaces qui sont visualisées échographiquement comme un vitreux rempli de multiples grandes opacités qui sont plus élevées dans leur réflectivité. Les hémorragies vitreuses peuvent également se superposer de manière inférieure en raison des forces gravitationnelles.
Voir l’image ci-dessous.
 Balayage horizontal de la macula dans un œil avec une hémorragie vitreuse. La surface de la lentille postérieure est vue centrée vers la gauche, la macula centrée vers la droite. Le nerf optique est vu juste au-dessus de la macula, car le marqueur est dirigé nasalement.
Balayage horizontal de la macula dans un œil avec une hémorragie vitreuse. La surface de la lentille postérieure est vue centrée vers la gauche, la macula centrée vers la droite. Le nerf optique est vu juste au-dessus de la macula, car le marqueur est dirigé nasalement. La formation de membranes peut également survenir après un traumatisme, en particulier après des lésions oculaires pénétrantes ou perforantes. Une piste membraneuse se développe souvent le long du trajet de l’objet incriminé. Dans les blessures pénétrantes, cette piste peut se terminer dans la cavité vitreuse ou sur un site d’impact opposé au site d’entrée. Dans les blessures perforantes, la piste couvre l’œil du site d’entrée au site de sortie. Par conséquent, le suivi de la piste peut entraîner un corps étranger intraoculaire et / ou une pathologie rétinienne à un site d’impact ou de sortie. Les corps étrangers intraoculaires peuvent être détectés facilement par ultrasons. Même si elles sont déjà détectées avec une autre modalité d’imagerie, telle que la tomographie informatisée ou l’imagerie par résonance magnétique, les ultrasons peuvent localiser plus précisément l’objet étranger. Cela peut être une information extrêmement vitale car elle peut déterminer comment le chirurgien aborde le cas.
Dans une étude de la fiabilité de l’échographie oculaire pour l’évaluation préchirurgicale de diverses affections vitréo-rétiniennes, y compris un traumatisme, une hémorragie vitréenne diabétique, une endophtalmie et d’autres causes d’hémorragie vitréenne, la sensibilité et la spécificité globales étaient de 92,31% et 98,31%, respectivement, pour l’identification du décollement rhégmatogène de la rétine et étaient de 96,2% et 100%, respectivement, pour le décollement postérieur du vitré. Dans les yeux traumatisés, la sensibilité était de 90,9% et la spécificité de 97,7% pour identifier l’état de la rétine.
Rétine
Une déchirure rétinienne peut être détectée par ultrasons lors de l’utilisation d’approches longitudinales. Parfois, les déchirures rétiniennes s’accompagnent d’hémorragies vitrées, ce qui empêche la visualisation de la déchirure étiologique. Dans de tels cas, on peut souvent voir le hyaloïde vitré postérieur ou un brin vitré attaché au lambeau rétinien. Ceux-ci ont tendance à se produire à la périphérie éloignée, où le vitré est le plus fermement attaché à la surface rétinienne, en particulier de manière superotemporelle. Une manchette peu profonde de liquide sous-rétinien peut accompagner la déchirure et rendre le diagnostic plus évident.
Voir l’image ci-dessous.
 Hémorragie vitreuse avec déchirure de la rétine au 1:30. Notez l’hyaloïde vitré qui se fixe à l’extrémité de la déchirure. Il s’agit d’un balayage longitudinal, nécessaire pour afficher la déchirure due à la direction radiale du volet.
Hémorragie vitreuse avec déchirure de la rétine au 1:30. Notez l’hyaloïde vitré qui se fixe à l’extrémité de la déchirure. Il s’agit d’un balayage longitudinal, nécessaire pour afficher la déchirure due à la direction radiale du volet. Lorsqu’un décollement de la rétine est présent, l’examinateur voit une membrane ondulée hautement réfléchissante. Chez les patients présentant des détachements rétiniens totaux, la surface généralement pliée se fixe à l’ora serrata en avant et au nerf optique en arrière. Initialement, un décollement de la rétine est relativement mobile (avec mouvement oculaire). Cependant, avec le temps, une vitréorétinopathie proliférative (formation de membrane épirétinienne) peut survenir, et la rétine devient plus rigide et prend davantage une configuration d’entonnoir.
Voir l’image ci-dessous.
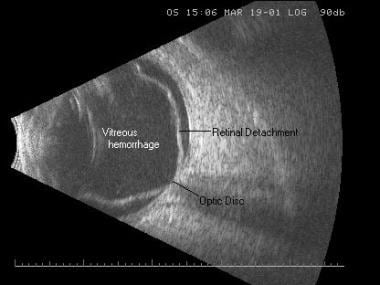 Décollement total de la rétine et hémorragie vitreuse. Le décollement de la rétine se présente sous la forme d’une membrane légèrement ondulée de haute réflectivité dans une configuration en entonnoir ouvert, se fixant au niveau du disque optique et en périphérie au niveau de l’ora serrata.
Décollement total de la rétine et hémorragie vitreuse. Le décollement de la rétine se présente sous la forme d’une membrane légèrement ondulée de haute réflectivité dans une configuration en entonnoir ouvert, se fixant au niveau du disque optique et en périphérie au niveau de l’ora serrata. La rétinoschisie est une affection caractérisée par une scission entre des couches spécifiques de la rétine. Cliniquement, il est difficile de différencier une rétinoschisie d’un décollement de la rétine. Les ultrasons peuvent en outre aider à la différenciation car la rétinoschisis est plus focale, lisse, en forme de dôme et mince.
Dans une étude utilisant une échographie B à haute résolution pour différencier la rétinoschisie du décollement de la rétine, dans les yeux avec rétinoschisie, la rétine externe a démontré la présence de 2 lignes hyperréflectives correspondant aux interfaces de la couche plexiforme externe et de l’épithélium pigmentaire de la rétine, tandis que les yeux avec décollement de la rétine ont démontré 2 lignes hyperréflectives dans la partie détachée, correspondant aux interfaces de la couche de fibres nerveuses et de la couche plexiforme externe, et la partie attachée a démontré la présence de la troisième interface hyperréflective . Ces résultats étaient bien corrélés avec la tomographie par cohérence optique dans le domaine spectral (SD-OCT).
L’échographie à balayage B est couramment utilisée pour l’évaluation initiale et de suivi du rétinoblastome. Le rétinoblastome, un cancer de la rétine très malin trouvé chez les nourrissons et les jeunes enfants, présente généralement des zones focales de calcification au sein de la tumeur. L’échographie peut facilement détecter le calcium, représenté par des foyers hautement réfléchissants dans la tumeur ou le vitré.
Voir l’image ci-dessous.
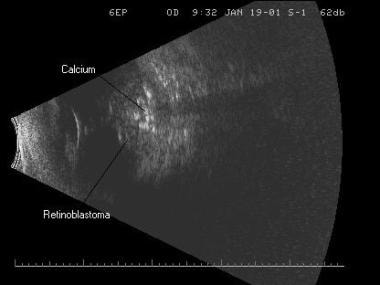 hautement réfléchissant. Notez les petites échodensités hautement réfléchissantes à l’intérieur de la tumeur, qui sont des foyers de calcium.
hautement réfléchissant. Notez les petites échodensités hautement réfléchissantes à l’intérieur de la tumeur, qui sont des foyers de calcium. Lorsqu’elles sont petites, les tumeurs sont lisses, en forme de dôme et ont une réflectivité interne faible à moyenne. À mesure que les tumeurs se développent, elles deviennent de configuration plus irrégulière et plus réfléchissantes à mesure que la quantité de calcium s’accumule. Ce cancer pédiatrique peut être unilatéral et unifocal, unilatéral et multifocal ou bilatéral. L’échographie est devenue un moyen très utile et très rentable de suivre ces tumeurs au fur et à mesure du traitement. Des mesures de la taille de la tumeur de base et l’emplacement de la tumeur sont obtenus, et ces paramètres sont surveillés de près pendant et après le traitement.
Typiquement, la présence de leucocorie (une pupille blanche) alerte le parent ou le pédiatre de cette maladie. Cependant, plusieurs autres maladies de la rétine pédiatrique sont associées à la leucocorie, telles que le vitré primaire hyperplasique persistant (PHPV), la rétinopathie de la prématurité (ROP), la maladie de Coats et le médulloépithéliome. Le PHPV, également appelé vascularisation fœtale persistante (PFV), est presque toujours une affection unilatérale dans laquelle le vitré primaire (en particulier le vaisseau hyaloïde) ne régresse pas et continue de s’étendre du nerf optique à la capsule cristalline postérieure. Échographiquement, on peut détecter le vaisseau hyaloïdal persistant très mince qui court du disque à la lentille lorsque des approches longitudinales sont utilisées. D’autres caractéristiques échographiques peuvent inclure une membrane rétrolentaire, un petit globe (petite longueur axiale) et, dans les cas graves, une traction associée ou un décollement total de la rétine.
Voir l’image ci-dessous.
 . Notez la membrane mince de faible réflectivité émanant du disque optique à la surface de la lentille postérieure. Un balayage longitudinal est nécessaire pour imager la membrane dans son intégralité, par opposition à un balayage transversal en coupe transversale, qui ne mettrait en évidence qu’un petit point faible dans la cavité vitrée centrale. Le gain le plus élevé est également nécessaire car la membrane est un signal très faible.
. Notez la membrane mince de faible réflectivité émanant du disque optique à la surface de la lentille postérieure. Un balayage longitudinal est nécessaire pour imager la membrane dans son intégralité, par opposition à un balayage transversal en coupe transversale, qui ne mettrait en évidence qu’un petit point faible dans la cavité vitrée centrale. Le gain le plus élevé est également nécessaire car la membrane est un signal très faible. La ROP est une maladie bilatérale dont la gravité peut être asymétrique, mais qui est généralement assez symétrique. Il existe différents stades de cette maladie; cependant, le stade le plus avancé (stade V) a souvent un réflexe pupillaire blanc. La maladie de stade V est définie comme un décollement total de la rétine dû à la contraction périphérique du tissu prolifératif fibrovasculaire et présente généralement une configuration en entonnoir. La configuration de ce détachement est détectée facilement par ultrasons.
La maladie de Coats est une affection unilatérale caractérisée par une télangiectasie vasculaire rétinienne et, lorsqu’elle est grave, un décollement exsudatif de la rétine. Cette maladie peut être la plus difficile à différencier du rétinoblastome. Cependant, l’échographie est très utile en raison du manque de calcium et de la présence de cholestérol dans l’espace sous-rétinien. Dans les zones de télangiectasie, la rétine est généralement épaissie.
Un médulloépithéliome est une tumeur rare qui survient principalement dans le corps ciliaire des enfants. Les caractéristiques typiques des ultrasons comprennent une configuration en forme de dôme, une réflectivité interne élevée, une vascularisation modérée et de multiples espaces kystiques.
Choroïde
Échographiquement, la choroïde est beaucoup plus épaisse que la rétine. Lorsque la rétine et la choroïde sont encore apposées, on peut voir un double pic sur l’A-scan diagnostique, un pic hautement réfléchissant représentant l’interface vitréorétinienne et un pic légèrement moins réfléchissant représentant l’interface rétinochoroïdienne. Un décollement choroïdien peut survenir spontanément, après un traumatisme ou à la suite de diverses chirurgies intraoculaires. À l’échographie, le détachement est lisse, en forme de dôme et épais. Pratiquement aucun mouvement n’est vu avec le mouvement des yeux. Lorsqu’il est étendu, on peut voir plusieurs détachements en forme de dôme, qui peuvent « s’embrasser » dans la cavité vitrée centrale. Lorsque les détachements choroïdiens sont hémorragiques plutôt que séreux (comme on le voit généralement dans les situations traumatiques), l’espace sous-choroïdal est rempli d’une multitude de points contrairement à l’espace sous-choroïdal écholucent d’un détachement choroïdien séreux.
Voir l’image ci-dessous.
 « Embrassant ». Les membranes épaisses et bulleuses se rencontrent dans la cavité vitrée centrale. L’opacité sous-jacente indique une hémorragie sous-jacente.
« Embrassant ». Les membranes épaisses et bulleuses se rencontrent dans la cavité vitrée centrale. L’opacité sous-jacente indique une hémorragie sous-jacente. La tumeur la plus fréquente de la choroïde est le mélanome malin. Bien que ceux-ci puissent survenir dans le corps ciliaire ou l’iris, ils sont le plus souvent observés dans la choroïde. Comme le rétinoblastome, l’échographie est devenue inestimable dans le diagnostic et l’évaluation de suivi des mélanomes malins uvéaux. Cette tumeur hautement cellulaire homogène se traduit par une réflectivité interne faible à moyenne et une structure interne régulière. Diagnostic A-scan et B-scan peuvent détecter la vascularisation interne dans la plupart des mélanomes.
Une découverte presque pathognomonique est une configuration de bouton de collier (c’est-à-dire une forme de champignon), mais cette forme est observée dans moins de 25% des cas. Histologiquement, le bouton du col représente la partie de la tumeur qui a traversé la membrane de Bruch, une membrane basale située entre la choroïde et la rétine.
Voir l’image ci-dessous.
 Mélanome choroïdien en forme de col-bouton. La lésion a commencé sous la forme d’un dôme, puis a traversé la membrane de Bruch pour former le bouton sur la surface antérieure du dôme. Notez le schéma diagnostique A-scan typique du mélanome, avec un pic rétinien élevé à la surface de la lésion mais une réflectivité interne faible à moyenne au sein de la lésion. La sclérotique et les tissus orbitaux sont considérés comme des pointes à droite de la lésion.
Mélanome choroïdien en forme de col-bouton. La lésion a commencé sous la forme d’un dôme, puis a traversé la membrane de Bruch pour former le bouton sur la surface antérieure du dôme. Notez le schéma diagnostique A-scan typique du mélanome, avec un pic rétinien élevé à la surface de la lésion mais une réflectivité interne faible à moyenne au sein de la lésion. La sclérotique et les tissus orbitaux sont considérés comme des pointes à droite de la lésion. Typiquement, un mélanome choroïdien a une forme de dôme lisse. Les mélanomes diffus ont une forme relativement plate et un contour irrégulier mais conservent une réflectivité interne faible à moyenne.
Voir l’image ci-dessous.
 d’un mélanome choroïdien. Il s’agit d’une tranche latérale à travers la lésion centrée à la position 5: 00 de l’œil gauche, avec 3 heures d’horloge représentées à la fois au-dessus (positions 2: 00, 3: 00 et 4: 00, respectivement, du haut) et au-dessous (positions 6: 00, 7: 00 et 8: 00) de la lésion.
d’un mélanome choroïdien. Il s’agit d’une tranche latérale à travers la lésion centrée à la position 5: 00 de l’œil gauche, avec 3 heures d’horloge représentées à la fois au-dessus (positions 2: 00, 3: 00 et 4: 00, respectivement, du haut) et au-dessous (positions 6: 00, 7: 00 et 8: 00) de la lésion. Lorsqu’une partie d’un mélanome dépasse son apport sanguin, cette partie de la tumeur peut se nécrose et saigner à l’intérieur, ou dans l’espace sous-rétinien, vitréen ou suprachoroïdal. Si l’hémorragie est étendue, le sang peut empêcher la détection échographique de la tumeur. Dans de tels cas, un examen de suivi est vital. Lorsque la tumeur saigne à l’intérieur, l’examinateur peut voir des poches hautement réfléchissantes à l’intérieur de la tumeur et une structure interne par conséquent irrégulière. Étant donné que les mélanomes plus gros produisent une atténuation acoustique interne significative, il y a une réflectivité plus faible à la base de la tumeur, appelée évidement acoustique.
Parfois, une évacuation choroïdienne est observée à la base de la tumeur. On pense que cela représente la tumeur envahissant les structures choroïdiennes plus profondes. Un mélanome peut progresser plus loin et s’étendre à travers la paroi sclérale, appelée extension extrasclérale. Cela se produit généralement le long des canaux émissaires. L’échographie est probablement la seule méthode fiable de détection de petites extensions extrasclérales postérieures.
Ces informations sont essentielles à la prise de décision et au pronostic de la gestion. Si un mélanome est traité par curiethérapie, la localisation échographique peropératoire de la plaque par rapport à la tumeur a considérablement amélioré le succès du traitement. Enfin, si des traitements épargnant les yeux peuvent être effectués, tels que la curiethérapie, l’irradiation par faisceau de protons ou la thérapie thermique transpupillaire, les ultrasons sont précieux pour surveiller la réponse tumorale en termes de taille et de réflectivité interne. Une réponse favorable est une tumeur régressant progressivement avec une réflectivité interne de plus en plus élevée. De toute évidence, une réponse défavorable est une tumeur qui continue de croître.
Les tumeurs mélanocytaires bénignes comprennent les naevus et les mélanocytomes. Comme un mélanome, la pigmentation d’un naevus peut aller de l’absence de pigmentation (amélanotique) à une pigmentation brun foncé (mélanotique). Un mélanocytome est généralement fortement pigmenté. Ils ont également une configuration en forme de dôme mais, contrairement au mélanome, ils sont très réfléchissants et n’ont pas de vascularisation interne. Malheureusement, les petits mélanomes peuvent montrer une absence de faible réflectivité interne et, par conséquent, il peut être difficile de différencier une petite lésion bénigne d’une lésion maligne de taille similaire.
Les tumeurs métastatiques peuvent se propager à la choroïde en raison de sa nature hautement vasculaire. Ces tumeurs ont un aspect échographique très différent. Cliniquement, ces tumeurs sont de couleur crème ou jaune et multilobulées. Sur le plan échographique, ces tumeurs ont généralement un contour grumeleux irrégulier, une structure interne irrégulière, une réflectivité interne moyenne à élevée et peu de preuves de vascularisation interne. Bien que les détachements exsudatifs se produisent avec des mélanomes uvéaux, les tumeurs métastatiques de taille similaire ont généralement des détachements plus étendus. L’extension extrasclérale peut également être observée avec ces tumeurs et, par conséquent, n’est pas utile dans la différenciation de la tumeur.
Voir l’image ci-dessous.
 du sein. La lésion a des bordures plutôt irrégulières, avec une réflectivité interne moyenne à élevée et irrégulière à la fois sur B-scan et sur A-scan diagnostique.
du sein. La lésion a des bordures plutôt irrégulières, avec une réflectivité interne moyenne à élevée et irrégulière à la fois sur B-scan et sur A-scan diagnostique. L’hémangiome choroïdien est une tumeur vasculaire bénigne de la choroïde. Ces tumeurs peuvent produire des détachements rétiniens exsudatifs localisés et une perte de vision ultérieure. Cliniquement, ces tumeurs sont des tumeurs en forme de dôme orange. Échographiquement, un hémangiome choroïdien est en forme de dôme et présente une réflectivité interne élevée. Un décollement séreux de la rétine sus-jacent peut être vu avec B-scan. Une forme plus diffuse d’hémangiome choroïdien est observée dans le syndrome de Sturge-Weber. Chez ces patients, la tumeur est plus étendue et moins élevée.
Voir l’image ci-dessous.
 hémangiome choroïdien avec un décollement exsudatif de la rétine associé. Cette lésion est composée de vaisseaux sanguins étroitement compactés et présente donc une réflectivité interne élevée et régulière à la fois au scanner B et au scanner A diagnostique.
hémangiome choroïdien avec un décollement exsudatif de la rétine associé. Cette lésion est composée de vaisseaux sanguins étroitement compactés et présente donc une réflectivité interne élevée et régulière à la fois au scanner B et au scanner A diagnostique. Les tumeurs choroïdiennes calciques sont facilement différenciées et détectées par B-scan. Un ostéome choroïdien apparaît cliniquement comme une lésion jaune, généralement située près du nerf optique. Ces tumeurs ne sont pas significativement élevées. Aux ultrasons, ils ont une réflectivité interne très élevée due au calcium. Leur contour est généralement plat et lisse, mais, à l’occasion, ces tumeurs ont une apparence grumeleuse. Une ombre marquée se produit postérieurement à la tumeur en raison de l’absorption par le calcium de l’énergie sonore.
Voir l’image ci-dessous.
 Ombrage causé par l’absorption acoustique par le calcium dans un ostéome choroïdien. Le calcium est si dense qu’aucun son ne peut le pénétrer pour se rendre à la structure suivante.
Ombrage causé par l’absorption acoustique par le calcium dans un ostéome choroïdien. Le calcium est si dense qu’aucun son ne peut le pénétrer pour se rendre à la structure suivante. Corps ciliaire
Le corps ciliaire est mieux visualisé avec un balayage haute résolution; cependant, la méthode d’immersion peut être utilisée, ou même la méthode de contact peut être utilisée pour évaluer les aspects les plus postérieurs du corps ciliaire. Un décollement du corps ciliaire peut s’étendre dans la choroïde périphérique et peut être vu lors d’un balayage de contact B, bien qu’il soit mieux affiché lors d’un balayage à haute résolution. Une fente réfléchissante de faible à moyenne est observée dans l’espace subciliaire.
Voir l’image ci-dessous.
 Décollement du corps ciliaire vu sur balayage haute résolution. Notez la grande fente dans l’espace subciliaire.
Décollement du corps ciliaire vu sur balayage haute résolution. Notez la grande fente dans l’espace subciliaire. Les tumeurs du corps ciliaire sont similaires à celles observées dans la choroïde. Les tumeurs du corps ciliaire les plus courantes sont les mélanomes; cependant, une variété d’autres tumeurs apparaissent dans le corps ciliaire, y compris les tumeurs métastatiques, les médulloépithéliomes et les léiomyomes.
Sclérotique
L’échographie diagnostique est probablement le meilleur moyen d’évaluer l’épaississement scléral. L’épaississement scléral se produit en cas de nanophtalmie (très petits yeux), d’hypotonie oculaire, de phthisis bulbi et de sclérite. Dans la sclérite, le degré d’épaississement scléral peut varier de léger à sévère, et il peut être focal ou diffus. Généralement, un œdème associé adjacent à la sclérotique est présent. Cela se manifeste comme une zone écholucente dans l’espace Tenon. Lorsqu’il est postérieur et adjacent au nerf optique, il forme un signe T. D’autres découvertes associées incluent une sclérotique épaissie hautement réfléchissante, des détachements rétiniens et des détachements ciliochoroïdaux.
Voir l’image ci-dessous.
 Sclérite postérieure nodulaire avec liquide dans la capsule de Tenon. Le scan à droite montre un signe T positif à l’insertion du nerf optique.
Sclérite postérieure nodulaire avec liquide dans la capsule de Tenon. Le scan à droite montre un signe T positif à l’insertion du nerf optique. Les patients myopes peuvent présenter des zones focales d’amincissement de la sclérotique. Ces zones peuvent former des staphylomes ou des poches. L’échographie est la meilleure modalité d’imagerie pour les changements staphylomateux. En cas de traumatisme, les ruptures sclérales occultes peuvent être difficiles à apprécier à l’examen clinique. L’échographie ne peut généralement pas détecter la rupture réelle; cependant, plusieurs indices échographiques peuvent aider le clinicien. Ces indices comprennent une hémorragie dans l’espace épiscléral immédiat, une choroïde épaissie ou détachée, une rétine détachée dans la zone préoccupante, une hémorragie vitreuse ou un vitré incarcéré dans la rupture.
Voir l’image ci-dessous.
 staphylomes postérieurs. L’uvea chez ce patient est devenue si mince qu’elle est bombée postérieurement dans la région maculaire et juste nasale au disque.
staphylomes postérieurs. L’uvea chez ce patient est devenue si mince qu’elle est bombée postérieurement dans la région maculaire et juste nasale au disque. Nerf optique
Les ventouses du disque optique peuvent généralement être observées à l’examen clinique. Cependant, si l’opacité des milieux empêche l’examen, le contour (y compris le degré de ventouses) peut être détecté par ultrasons. De même, les colobomes du nerf optique sont facilement imagés par ultrasons.
Voir l’image ci-dessous.
 . Notez l’indentation du disque optique, résultat de l’augmentation de la pression intraoculaire dans les maladies glaucomateuses.
. Notez l’indentation du disque optique, résultat de l’augmentation de la pression intraoculaire dans les maladies glaucomateuses. En clinique, il est essentiel de différencier le papillœdème (œdème du disque optique) du pseudopapillœdème, car le premier est associé à une pression intracrânienne élevée, tandis que le second peut ne pas avoir de pertinence systémique. Les drusen à disque optique sont des nodules calciques enfouis dans la tête du nerf optique et peuvent simuler un œdème papillaire. À l’échographie, ces nodules sont hautement réfléchissants et existent au niveau ou à l’intérieur de la tête du nerf optique.
Voir l’image ci-dessous.
 drusen. Notez l’échodensité hautement réfléchissante du calcium.
drusen. Notez l’échodensité hautement réfléchissante du calcium. Dans le véritable œdème papillaire, une augmentation de la pression intracrânienne (ICP) est transmise le long de l’espace sous-dural dans le nerf optique. Les entités cliniques pouvant provoquer une pression intracrânienne élevée comprennent les tumeurs cérébrales pseudotumorales et intracrâniennes. Lorsque le PIC est légèrement élevé, le nerf optique est légèrement élargi. Dans les cas les plus graves, on peut voir un cercle écholucent à l’intérieur de la gaine du nerf optique (séparant la gaine du nerf optique). C’est le signe dit du croissant.
Voir l’image ci-dessous.
 Augmentation du liquide sous-arachnoïdien autour du nerf optique. Notez le signe croissant positif.
Augmentation du liquide sous-arachnoïdien autour du nerf optique. Notez le signe croissant positif. La présence d’une augmentation du liquide dans la gaine est mieux confirmée avec le test à 30 degrés, qui est un test A-scan dynamique qui mesure la largeur du nerf optique dans le regard primaire et à nouveau après que le patient a déplacé le regard de 30 degrés par rapport au regard primaire. En cas d’augmentation de l’ICP, le nerf et la gaine sont étirés lorsque le globe tourne de 30 degrés, et le liquide sous-arachnoïdien est distribué sur l’étendue du nerf, ce qui entraîne des mesures inférieures à celles du regard primaire. Si l’élargissement du nerf est dû à une infiltration parenchymateuse ou à un épaississement de la gaine du nerf optique, la mesure ne changera pas lorsque le globe deviendra primaire.
Un gliome du nerf optique est un processus néoplasique qui infiltre le parenchyme du nerf optique. Aux ultrasons, il s’agit d’une masse fusiforme lisse avec une réflectivité interne faible à moyenne et régulière. Un méningiome de la gaine du nerf optique est un exemple de tumeur de la gaine du nerf optique. Contrairement à un gliome, ce processus néoplasique présente généralement une réflectivité interne irrégulière moyenne à élevée avec des zones de calcification possibles.
Résumé
Avec une compréhension des principes de l’échographie, des techniques d’examen approfondies et des caractéristiques échographiques d’une variété de pathologies intraoculaires, l’échographie B-scan de l’œil est une partie essentielle de l’arsenal diagnostique d’un ophtalmologiste. Sans cet outil, le clinicien peut ne pas être en mesure de détecter ou de gérer une variété de maladies oculaires. Cependant, comme pour toute compétence technique, l’échographie B-scan nécessite une formation, du temps et de l’expérience pour atteindre un niveau élevé de confiance et d’imagerie de qualité.