Amyotrophie spinale
Causes / Hérédité
Quelles sont les causes de l’amyotrophie spinale (amyotrophie spinale)?
La SMA est caractérisée par la perte de motoneurones, cellules nerveuses de la moelle épinière. Il est classé comme une maladie des motoneurones.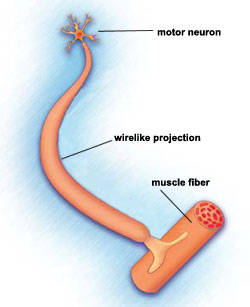
Quelles sont les causes génétiques de la SMA?
La forme la plus courante de SMA (types 1-4) est causée par un défaut (mutation) du gène SMN1 sur le chromosome 5. (Les gens ont deux gènes SMN1 — un sur chaque chromosome 5). Dans 94% des cas de SMA, cette mutation implique une délétion dans un segment appelé exon 7. Cette zone est située dans le bras long du chromosome 5, dans la région 5q13.2 (les chromosomes ont deux « bras »: un bras court, identifié par la lettre « p », et un bras long, identifié par la lettre « q »).
Une mutation du gène SMN1 entraîne une déficience d’une protéine du motoneurone appelée SMN, qui signifie « survie du motoneurone ». »Comme son nom l’indique, cette protéine est responsable de l’expression génique nécessaire au fonctionnement normal des motoneurones.
Plus rarement, une mutation dans un gène du chromosome X appelé UBE1 provoque une SMA liée à l’X. Le gène UBE1 contient des instructions pour l’enzyme 1 activant l’ubiquitine, qui aide normalement à attacher une étiquette moléculaire aux protéines pour les marquer en vue de leur destruction.
Des failles dans le gène cytoplasmique de la chaîne lourde 1 de la dynéine 1 (DYNC1H1) sur le chromosome 14 ont été trouvées pour conduire à une autre forme rare de SMA appelée SMA-LED.
Quelles sont les causes de la grande variation de la gravité des symptômes observée dans la SMA?
Normalement, les gènes SMN1 produisent une protéine SMN pleine longueur et entièrement fonctionnelle. Mais lorsque le gène SMN1 présente des mutations, comme dans la forme de SMA liée au chromosome 5, des niveaux insuffisants de protéine SMN sont produits.
Un gène voisin sur le chromosome 5, appelé SMN2, produit également la protéine SMN. La plupart des protéines fabriquées à partir d’instructions portées par les gènes SMN2 ne sont pas fonctionnelles, mais un faible pourcentage, autour de 10 à 15%, est fonctionnel.
Les personnes peuvent avoir plusieurs copies du gène SMN2. Normalement, le nombre varie entre zéro et huit copies. Dans la forme de SMA liée au chromosome 5, plus une personne a de copies du gène SMN2, plus la protéine SMN est fonctionnelle. En conséquence, plus l’évolution de la maladie est susceptible d’être douce. Avoir trois copies ou plus du gène SMN2 est associé à une manifestation moins grave de la maladie.
Les tests génétiques peuvent indiquer le nombre de gènes SMN2 d’une personne et prédire à peu près l’évolution de la SMA susceptible d’en résulter.
La gravité de la SMA peut également dépendre des modificateurs de la maladie, qui ne causent pas de maladie mais peuvent affecter (modifier) l’apparition et la gravité en influençant diverses voies biologiques. Les niveaux de la protéine plastine 3 et de la protéine ZPR1 ont été identifiés comme des modificateurs de la SMA liée au SMN et pourraient devenir des cibles thérapeutiques. En outre, les tests de ces niveaux de protéines pourraient aider à prédire la gravité de la maladie, et un aperçu des activités de ces protéines pourrait apporter un nouvel éclairage sur les processus de la maladie.

L’information génétique passe de sa forme de stockage sous forme d’ADN à un ensemble d’instructions appelées ARN, à partir desquelles les molécules de protéines sont fabriquées. La plupart des instructions d’ARN du gène SMN1 indiquent à la cellule de produire une protéine SMN pleine longueur. La plupart des instructions du gène SMN2 indiquent à la cellule de produire une protéine SMN courte.
Quel est le modèle d’héritage de SMA?
La SMA liée au chromosome 5 (types 1 à 4) suit un schéma d’hérédité connu sous le nom de récessif autosomique. (Les autosomes sont les chromosomes numérotés — c’est-à-dire tous les chromosomes sauf le X et le Y, qui déterminent le sexe.)
Les maladies récessives nécessitent deux défauts génétiques – généralement un de chaque parent, mais parfois un d’un parent et un qui se produit pendant la formation d’un fœtus. Les personnes qui n’ont qu’un seul défaut génétique pour une maladie récessive seraient porteuses et ne présenteraient généralement aucun symptôme. Souvent, une famille n’a aucune idée que certains membres sont porteurs jusqu’à ce qu’un enfant naisse avec un trouble récessif.
Si les deux parents sont porteurs de la faille du gène du chromosome 5, le risque que chaque grossesse produise un enfant atteint de la maladie est de 25%. Ce risque ne change pas, quel que soit le nombre d’enfants d’un couple.
Des tests génétiques pour la SMA liée au chromosome 5 sont disponibles pour les personnes soupçonnées d’être atteintes de la maladie, y compris les bébés à naître, et pour les porteurs de la maladie. Les tests génétiques se développent et évoluent rapidement, mais leurs implications peuvent être complexes. Il est préférable de parler avec un conseiller génétique avant de se lancer dans les tests. (Une référence de conseil génétique peut être obtenue par l’intermédiaire de votre centre de soins MDA ou de votre médecin de soins primaires).
Il est impératif de diagnostiquer la SMA le plus tôt possible, idéalement avant l’apparition des symptômes, car un retard de traitement peut aggraver l’évolution de la maladie et créer des dommages permanents aux motoneurones. La meilleure façon d’identifier la SMA avant l’apparition des symptômes est de dépister tous les nouveau-nés pour la suppression de l’exon 7 SMN1. Depuis que Spinraza (nusinersen), un traitement modificateur de la maladie, a été approuvé en 2016 par la Food and Drug Administration (FDA) des États-Unis et que le traitement précoce a montré des résultats positifs, le secrétaire du département de la Santé des États-Unis a approuvé l’ajout de SMA aux panneaux de dépistage néonatal.11 for pour plus d’informations, visitez le LIEN HYPERTEXTE « https://strongly.mda.org/sma-added-national-list-disorders-to-screen-for… »SMA Ajouté à la Liste nationale des troubles à dépister à la naissance.
La SMA liée à l’X est héritée via le chromosome X. Les femelles ont deux chromosomes X, et celles qui ont une faille génétique sur un chromosome X sont généralement considérées comme porteuses d’une maladie liée à l’X. Les mâles, cependant, n’ont pas de seconde X pour les protéger des effets complets d’une faille génétique sur le chromosome X et montrer tous les effets d’une telle faille.
De plus, la SMA peut être causée par des mutations du gène DYNC1H1 sur le chromosome 14. Cette forme est héritée de manière dominante, ce qui signifie qu’une seule mutation du gène DYNC1H1, héritée d’un parent, est suffisante pour provoquer la maladie.
Pour en savoir plus sur la génétique de la SMA et les tests génétiques pour cette maladie, consultez également:
- Le webinaire sur le conseil génétique MDA Répond aux questions clés, Quest News Online, Fév. 28, 2012
- Faits sur la génétique et les maladies neuromusculaires, MDA, Décembre 2009
- The Genie’s Out of the Bottle: Genetic testing in the 21st century, Quest Magazine (MDA), Novembre 2008
- La douleur et la promesse du Diagnostic génétique Prénatal et Néonatal, Quest Magazine (MDA), Juillet 2007