16.10: elektrofil addíció: 1,2-Versus 1,4-addíció
az izolált diének addíciós reakciói többé-kevésbé az egyszerű alkének viselkedésétől elvárt módon zajlanak. Így, ha az 1,5-hexadién egy moláris ekvivalensét egy bróm ekvivalenssel kezeljük, 5,6-dibróm-1-hexén, 1,2,5,6-tetrabromohexán és reakció nélküli dién keverékét kapjuk, a dibrómvegyület a fő termék (körülbelül 50%)
ábra
a konjugált diének hasonló reakciói viszont gyakran váratlan termékeket eredményeznek. Példa erre a bróm hozzáadása az 1,3-butadiénhez. Amint az alább látható, a 3,4-dibróm-1-butén (a várható termék) és az 1,4-dibróm-2-butén (főleg az E-izomer) nagyjából 50:50 arányú keverékét kapjuk. Ez utóbbi vegyület figyelemre méltó, mivel a fennmaradó kettős kötés olyan helyen található, ahol a reagensben nem volt kettős kötés. Ez az érdekes áthelyezés magyarázatot igényel.
CH2 = CH-CH=CH2 + Br2  |
BrCH2CHBr-CH=CH2 + | BrCH2CH=CHCH2Br |
| 3,4-dibróm-1-butén | 1,4-dibróm-2-butén |
az ilyen reakciókból várható addíciós termék az 1,2-addíció eredménye, azaz kettős kötés szomszédos szénatomjaihoz való kötődése. A váratlan termék 1,4-addícióból származik, azaz egy konjugált dién terminális szénatomjaihoz való kötésből, a fennmaradó kettős kötés eltolódásával a 2,3-helyre. (Ezek a számok a konjugált dién négy szénatomjára vonatkoznak, és nem IUPAC nómenklatúra számok.) A termékösszetételek gyakran hőmérsékletfüggőek: 40 oC-nál a fenti addíciós reakcióban a termékkeverék 85% – a az 1,4 termék, míg 0 oC-nál csak körülbelül 30% az 1,4 termék.
egy elektrofil atom vagy csoport kötése egy konjugált dién egyik végszénatomjához (az alábbi ábrán az 1.szén) allil-kation köztiterméket hoz létre. Az ilyen kationokat a töltés delokalizációja stabilizálja, és ez a delokalizáció adja az ilyen addíciós reakciók során keletkező 1,4-addíciós terméket. Amint az ábrán látható, a pozitív töltés a #2 és #4 szénatomokon oszlik el, így ezeken a helyeken kötődnek a nukleofil komponens. Megjegyezzük, hogy az allil-kation rezonancia-stabilizációja nagyobb, mint az 1,3-butadién hasonló stabilizációja, mivel az előbbiben a töltés delokalizálódik, az utóbbiban viszont létrejön és elválik.
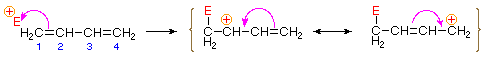
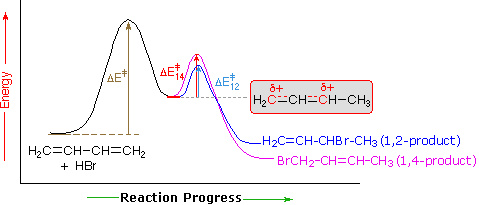
a HBR 1,3-butadiénhez történő hozzáadásának magyarázatát a következő energiadiagram mutatja. A kezdeti lépés, amelyben egy proton kötődik az 1. szénhez, a sebességmeghatározó lépés, amint azt a nagy aktiválási energia (világosszürke nyíl) jelzi. A második gyorsabb lépés a termékmeghatározó lépés, és két reakcióút van (kék színű az 1,2-addícióhoz és bíbor az 1,4-addícióhoz). Az 1,2-addíció kisebb aktivációs energiával rendelkezik, mint az 1,4 – addíció-gyorsabban fordul elő, mint az 1,4-addíció, mert a bromid nukleofil közelebb van a 2.szénhez, majd a 4. szénhez. Az 1,4-termék azonban stabilabb, mint az 1,2-termék. Alacsony hőmérsékleten a termékek visszafordíthatatlanul képződnek, és tükrözik a két versengő reakció relatív sebességét. Ezt nevezik kinetikus kontrollnak. Magasabb hőmérsékleten egyensúly alakul ki a termékek között, és a termodinamikailag kedvelt 1,4-termék dominál.
amikor egy konjugált diént megtámad egy elektrofil, a kapott termékek 1,2 és 1,4 izomerek keveréke. A kinetika és a termodinamika szabályozza a reakciót, ha két termék különböző reakciókörülmények között van. A kinetikus termék (a termék) gyorsan, a termodinamikai termék (B Termék) pedig lassabban képződik. Általában az első képződött termék a stabilabb előnyben részesített termék, de ebben az esetben a lassabb képződött termék a stabilabb termék; termék B.
Bevezetés
a nem konjugált diénekhez hasonlóan a konjugált diéneket elektrofilek támadják meg. Valójában a konjugált elektrofilek viszonylag nagyobb kinetikus reaktivitást tapasztalnak, ha elektrofilekkel reagálnak, mint a nem konjugált diének. Elektrofil hozzáadása után a konjugált dién két termék—a kinetikus termék és a termodinamikai termék-keverékét képezi, amelynek arányát a reakció körülményei határozzák meg. A több termodinamikai terméket eredményező reakció termodinamikai ellenőrzés alatt áll, és hasonlóképpen, egy olyan reakció, amely több kinetikus terméket eredményez, kinetikus ellenőrzés alatt áll.
alapvető reakció
részletes mechanizmus
következtetés
a konjugált diének (két kettős kötést tartalmazó szénhidrogének) reaktivitása a kettős kötés helyétől és a reakció hőmérsékletétől függően változik.Ezek a reakciók mind termodinamikai, mind kinetikai termékeket eredményezhetnek. Az izolált kettős kötések termodinamikailag kevésbé stabil diéneket biztosítanak, mint a konjugált diének. Ezek azonban kinetikailag reakcióképesebbek elektrofilek és más reagensek jelenlétében. Ez annak az eredménye, Markovnikov mellett az egyik kettős kötések. A kettős kötés megnyitása után karbokáció alakul ki. Ennek a karbokációnak két rezonancia szerkezete van, és az összeadás bármelyik pozitív szénatomnál előfordulhat.
gyakorlati problémák
- írja ki az 1,2 kiegészítés és az 1,4 – kiegészítés a) HBr és Br termékeit. b)DBr 1,3-ciklo-hexadiénre. Mi a szokatlan az 1,2-és 1,4-HX hozzáadásával a szubsztituált ciklikus 1,3-diénekhez?
- az 1,2-addíciós termék gyorsabban képződik magasabb hőmérsékleten, még akkor is, ha az 1,4-addíciós termék van túlsúlyban ilyen körülmények között?
- miért az 1,4-addíciós termék termodinamikailag stabilabb termék?
- a következő radikális kationok közül melyik nem ésszerű rezonancia szerkezet?
5. 1 ekvivalens bróm hozzáadása 2,4-hexadiénhez 0 C fokon 4,5-dibróm-2-hexén plusz egy izomer. Az alábbiak közül melyik az izomer:
- 5,5-dibróm-2-hexén
- 2,5-dibróm-3-hexén
- 2,2-dibróm-3-hexén
- 2,3-dibróm-4-hexén
6. Az alábbiak közül melyik lesz a kinetikusan kedvelt termék az ábrázolt reakcióból?
7. HBR hozzáadása 2,3-dimetil-1,3-ciklohexadiénhez peroxidok hiányában vagy jelenlétében fordulhat elő. Mindegyik esetben két izomer c8h13br terméket kapunk. Az alábbiak közül melyik a közös termék mindkét reakcióból?
8. és 9.
8. A fenti reakcióban a kinetikailag szabályozott termék:
- 3-klór-1-butén
- 1-klór-2-butén
9. A 8. kérdéses reakció esetében melyik az 1,4-kiegészítés eredménye?
- 3-klór-1-butén
- 1-klór-2-butén
válaszok a problémákra
1. A) ugyanaz a termék mindkét adagolási módhoz.
B) mind a cisz, mind a transz izomerek képződnek.
a HX hozzáadása szubsztituált cikloalka – 1,3 – diénekhez 1,2-vagy 1,4-módon ugyanazt a terméket adja, mint a szimmetria.
2. Igen. a kinetikus termék továbbra is gyorsabban képződik, de ebben az esetben elegendő energia lesz a termodinamikai termék kialakításához, mivel a termodinamikai termék még mindig stabilabb.
3. Az 1,4 – termék termodinamikailag stabilabb, mivel a kettős kötés mindkét oldalán két alkilcsoport van. Ez a forma stabilitást biztosít a teljes szerkezet számára.
4. Ezek az izomerek életképesek.
5. D
6. C
7. D
8. A
9. B
közreműködők
-
William Reusch, Emeritus professzor (Michigan State U.), A Szerves Kémia virtuális tankönyve
-
Jim Clark (Chemguide.co.uk)
- Natasha Singh