Atra Oktatás
bár minden nap többet tanulunk a Parkinson-kór patofiziológiájáról, még mindig nagyrészt idiopátiásnak tekintik (ismeretlen okból). Valószínűleg magában foglalja a gazdaszervezet érzékenységének és a környezeti tényezők kölcsönhatását. Az esetek kis százaléka genetikailag összekapcsolódik, és a genetikai tényezőket intenzíven tanulmányozzák.
fiziológiailag a Parkinson-kórhoz kapcsolódó tünetek számos neurotranszmitter, nevezetesen a dopamin elvesztésének következményei. A tünetek idővel súlyosbodnak, mivel a betegség által érintett sejtek egyre inkább elvesznek. A betegség lefolyása nagyon változó, egyes betegeknél az életkor előrehaladtával nagyon kevés tünet jelentkezik, másoknál pedig a tünetek gyorsan előrehaladnak.
a Parkinson-kórt egyre inkább komplex neurodegeneratív betegségnek tekintik, amelynek progressziója van. Erős bizonyíték van arra, hogy először a vagus ideg hátsó motoros magját, a szaglóhagymákat és a magot érinti, majd a locus coeruleust, végül pedig a substantia nigra-t. Az agy kortikális területeit egy későbbi szakaszban érinti. Ezeknek a különféle neuronális rendszereknek a károsodása felelős a sokrétű patofiziológiai változásokért, amelyek nemcsak a motoros rendszert, hanem a kognitív és neuropszichológiai rendszereket is károsítják (Kwan & Whitehill, 2011).
a dopamin szerepe
a dopamin, mint más neurotranszmitterek, kémiai üzeneteket továbbít az egyik idegsejtből a másikba a szinapszison keresztül, amely a preszinaptikus sejt és a posztszinaptikus receptor közötti tér. A dopamin a preszinaptikus membránban lévő membrán tároló vezikulákból választódik ki a szinapszisba. Áthalad a szinapszison és kötődik a posztszinaptikus membránhoz, ahol aktiválja a dopamin receptorokat. A szinapszisban maradt fel nem használt dopamin felszívódik a preszinaptikus sejtbe; miután visszatért a preszinaptikus sejtbe, a felesleges dopamint újracsomagolják a tároló vezikulákba, és ismét felszabadítják a szinapszisba.
a szinapszison belül, ahogy a dopamin egyik sejtből a másikba jut, két enzim, a MAO (monoamin-oxidáz) és a COMT (katekol-o-metil-transzferáz) lebontja és inaktívvá teszi. Az egyik terápiás stratégia MAO inhibitort vezet be a szinapszisba, amely megszakítja a MAO enzim működését és megakadályozza a dopamin lebontását. Ez lehetővé teszi, hogy több dopamin maradjon a szinapszisban, és növeli annak valószínűségét, hogy kötődik a posztszinaptikus membránhoz.
kémiai szinaptikus átvitel
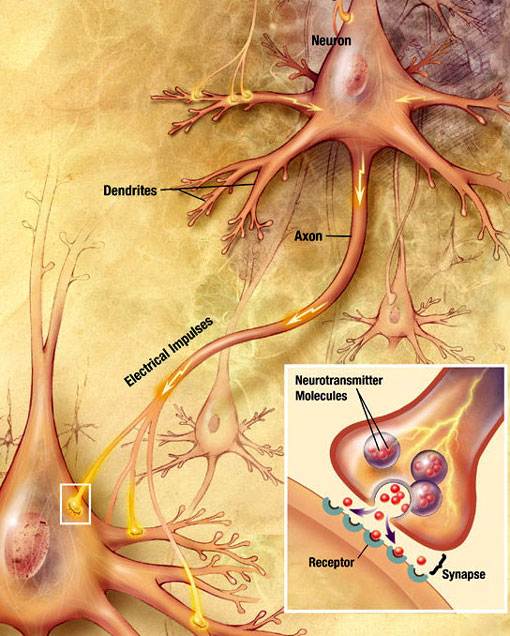
egy akciós potenciálnak nevezett elektrokémiai hullám az idegsejt axonja mentén halad. Amikor az akciós potenciál eléri a preszinaptikus terminált, kis mennyiségű neurotranszmitter molekula felszabadulását idézi elő, amelyek a posztszinaptikus neuron membránjában található kémiai receptor molekulákhoz kötődnek, a szinaptikus hasadék másik oldalán. Forrás: Wikimedia Commons.
progresszív Dopaminvesztés
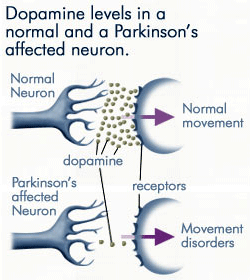
mivel a Parkinson-kór által érintett neuronok egyre kevesebb dopamint termelnek, sokkal kevesebb dopamin áll rendelkezésre a posztszinaptikus membrán dopamin receptoraihoz való kötődéshez. Forrás: anti-agingfirewalls.com.
bár a dopamin sejtvesztést nem lehet közvetlenül mérni, a neurológiailag normális embereknél és a főemlősöknél végzett mérések a dopamin lassú progresszív elvesztését mutatják az életkorral. Parkinson-kórban a veszteség sokkal nagyobb arányban fordul elő, és mind a biokémiai mérések, mind a képalkotó vizsgálatok azt sugallják, hogy a dopamin jelentősen csökken a motoros tünetek megjelenéséig. Ebben a nézetben a Parkinson-kór a normál öregedéssel megfigyelt sejthalál gyorsított változata (Cookson, 2009). Ezt szemlélteti az alábbi grafikon, amely bemutatja a dopaminerg neuronok csökkenését a normális öregedés során, idiopátiás PD-ben, környezeti vagy genetikai tényezők által okozott PD-ben, valamint a korai kezdetű PD-ben.
a dopamin depléció alakulása Parkinson-kórban
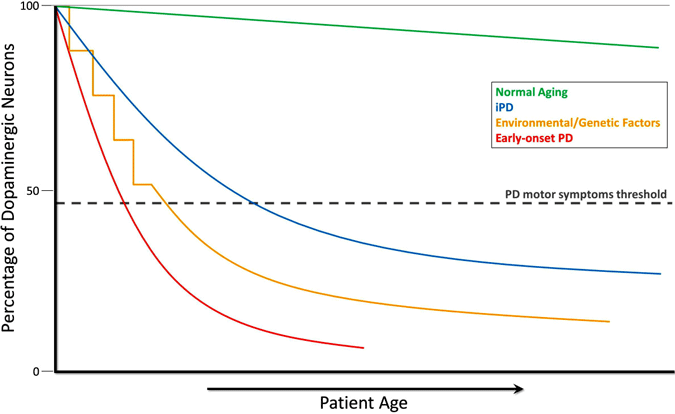
a normál öregedés során (zöld vonal) kicsi, de lassú dopaminerg degeneráció jelentkezik motoros tünetek nélkül. Az idiopátiás PD (IPD, kék vonal) ismeretlen eredetű, de úgy gondolják, hogy fokozatosan fejlődik, a dopaminerg neuronok lassú degenerációjával, ami a klasszikus PD motoros tünetekhez vezet az élet későbbi szakaszában. A dopamin neurodegeneráció egy másik modellje, amely PD motoros tünetekhez vezet, magában foglalja a környezeti toxikus anyagok ismételt expozícióját az idő múlásával, a dopaminerg neuronveszteség genetikai hajlamával kombinálva (sárga vonal). A PARKIN gén mutációi által okozott korai PD (piros vonal) a dopaminerg neuronok rohamos csökkenését vonja maga után, a PD motoros tünetei pedig évtizedekkel az idiopátiás PD tünetei előtt jelentkezhetnek. A PD motoros tünetek kialakulásának még egy (nem bemutatott) forgatókönyve magában foglalja a méhen belüli környezeti toxikus anyagokat vagy genetikai tényezőket, amelyek atipikusan alacsony számú dopaminerg neuronhoz vezetnek születéskor és fokozott érzékenység a PD fejlődésére (Haas et al., 2012).
a dopamin neuronok degenerációja különösen nyilvánvaló a substantia nigra Pars compacta nevű részén. A pars compacta dopaminvesztesége jelentősen növeli a bazális ganglionok általános gerjesztő képességét,* megzavarja az önkéntes motoros kontrollt és a PD jellegzetes tüneteit okozza. A motoros funkció normalizálódása kezdetben levodopa kezeléssel látható (Gasparini et al., 2013).
* a bazális ganglionok fő összetevői a striatum (caudate nucleus és putamen), a globus pallidus, a substantia nigra, a nucleus accumbens és a subthalamic nucleus.
a PD súlyosságának növekedésével a dopamin kimerülése további változásokhoz vezet a bazális ganglionokban, beleértve más bazális ganglion neurotranszmitterek, például a glutamát, a GABA és a szerotonin megváltozott működését (Gasparini et al., 2013). Bár a dopamint termelő neuronok relatív sebezhetősége van a substantia nigra-ban, a Parkinson-kórban nem minden dopaminsejt érintett; az agy egyes részein a dopamint termelő neuronok viszonylag megkíméltek (Cookson, 2009).
a nigrostriatális út
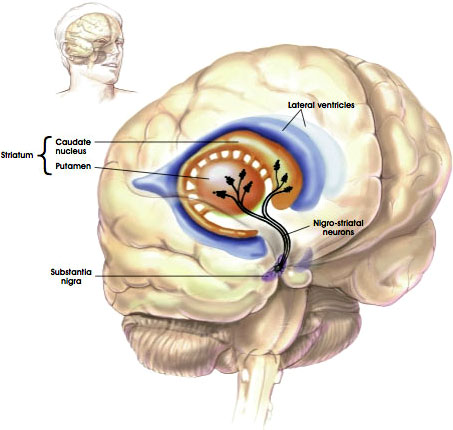
forrás: NIH, n. d.
a Lewy-testek és az alfa-szinuklein
a Lewy-testek kóros fehérje aggregátumok és zárványok, amelyek Parkinson-kórban szenvedő emberek idegsejtjeiben fejlődnek ki. Az aggregációk általában oldhatatlan fibrilláris aggregátumokból állnak, amelyek rosszul összehajtott fehérjéket tartalmaznak. A Lewy-testekben számos molekulát azonosítottak, de a fő összetevő az alfa-szinuklein nevű fehérje.
Lewy-testek (alfa-szinuklein zárványok)
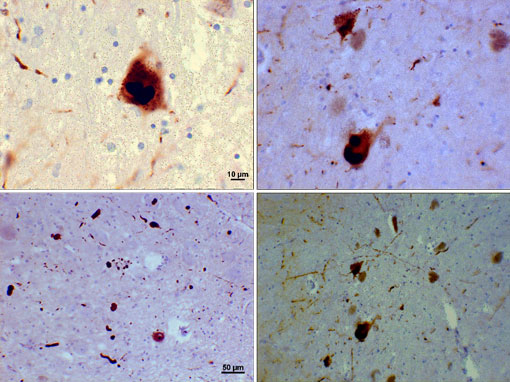
Fotomikrográf a substantia nigra régióiról egy Parkinson-kórban szenvedő betegben, amely Lewy-testeket és Lewy-neuritokat mutat különböző nagyításokban. A felső panelek az alfa-szinuklein intraneuronális zárványok 60-szoros nagyítását mutatják Lewy testek. Az alsó panelek 20 db-os nagyítású képek, amelyek szálszerű Lewy neuritokat és különböző méretű lekerekített Lewy-testeket mutatnak. Képek Suraj Rajan jóvoltából.
a Lewy patológia az agy számos régióját felöleli, és egyes jelentések szerint a substantia nigra nem az első hely, ahol a Lewy testek kialakulnak a Parkinson-kórban. A zárványok és aggregátumok valószínűleg a bonyolult események kaszkádjának végső szakaszát szimbolizálják. Egy korábbi szakasz közvetlenül kapcsolódhat a rendellenesség patogeneziséhez, mint maguk a zárványok, amelyek diagnosztikai jellemzőket jelenthetnek vagy nem.
a Lewy-testek a “Lewy-testekkel járó demenciában” is megfigyelhetők, ami arra utal, hogy ezek a feltételek közös patológiával és esetleg közös etiológiával állnak kapcsolatban egymással. Sem a sejtvesztés, sem a Lewy-testek képződése nem teljesen specifikus a PD-re, de mindkettő szükséges a PD diagnosztizálásához a jelenlegi meghatározások szerint (Cookson, 2009).
a neurodegeneratív rendellenességek, mint például az Alzheimer-kór, a frontális-temporális degeneráció, a prionbetegség, a Huntington-kór és a motoneuron betegségek egyre inkább felismerik, hogy közös sejtes és molekuláris mechanizmusokkal rendelkeznek, beleértve a fehérje aggregációt és a befogadást testképződés az idegrendszer bizonyos területein (Jellinger, 2011).
gyulladás és immunválasz
úgy tűnik, hogy a dopaminerg degeneráció kiváltó oka multifaktoriális—mind az endogén, mind a környezeti elemek befolyásolják. A gyulladást és az immunválaszokat egyre inkább a dopaminerg degeneráció fontos közvetítőinek tekintik. Nagy populációs vizsgálatok azt sugallták, hogy a nem szteroid gyulladáscsökkentő gyógyszereket (NSAID-ok) szedő egyéneknek kisebb az idiopátiás PD kialakulásának kockázata, ami arra utal, hogy a gyulladáscsökkentő gyógyszerek ígéretes betegségmódosító kezelés lehetnek a Parkinson-kórban szenvedő betegek számára (Barcia, 2013).
az új vizsgálati fázisok gyulladáscsökkentő kezeléseket tartalmaztak-kifejezetten objektív biomarker keresése a PD—ben szenvedő betegek gyulladásos változásainak csökkentését célzó kezelésekben. A kutatók neuroimaging eszközöket használnak egy releváns biomarker kifejlesztésére azzal a szándékkal, hogy ezt nagy klinikai képalkotó vizsgálatokban teszteljék. Ezeknek a vizsgálatoknak az eredménye adatokat szolgáltat a PD gyulladáscsökkentő kezelésének progressziójának tesztelésére és figyelemmel kísérésére, és segít azonosítani az időben történő terápiás ablakot a gyulladásos mediált dopaminerg degeneráció megállítására vagy legalábbis lassítására (Barcia, 2013).
parkinsonizmus
a parkinsonizmus, más néven “atipikus Parkinson—kór”, “másodlagos Parkinson-kór” vagy “Parkinson-szindróma”, olyan neurológiai szindróma, amelyben a beteg a Parkinson-kórhoz kapcsolódó néhány tünetet mutat-tremor, merevség, bradykinesia és poszturális instabilitás. De a parkinsonizmus nem Parkinson-kór. Úgy gondolják, hogy a parkinsonizmust nem a Parkinson-kór okozza, és a betegek általában rosszul reagálnak a farmakológiai beavatkozásra. A parkinsonizmusnak gyakran azonosítható oka van, például toxinoknak való kitettség, metamfetamin, trauma, többszörös stroke, egyéb idegrendszeri rendellenességek vagy betegség. Általában a Lewy-testek nem láthatók a parkinsonizmusban.
a parkinsonizmus kifejezés olyan rendellenességekkel is összefügg, mint a progresszív szupranukleáris bénulás, a többszörös rendszer atrófia, a Lewy-test demencia, a corticobasalis degeneráció, az érrendszeri parkinsonizmus, a gyógyszer által kiváltott parkinsonizmus és a fertőzés és más okok miatt másodlagos parkinsonizmus (Hohler et al., 2012). A reverzibilis parkinsonizmus egy formája előfordulhat bizonyos neuroleptikus gyógyszerek, különösen a reszerpin, az antipszichotikumok (haloperidol) és a metoklopramid használatából. Bizonyos toxinoknak való kitettség, súlyos szén-monoxid-mérgezés, higanymérgezés szintén parkinsonizmushoz vezethet.
a parkinsonizmus tüneteinek megjelenése az 1980-as évek elején olyan kábítószerfüggők csoportjában, akik szennyezett szintetikus opiát-adagot fogyasztottak, az MPTP kémiai anyag felfedezéséhez vezetett, amely parkinsonizmus szindrómát okoz nem emberi főemlősökben, valamint emberekben. Az MPTP előállítható a heroin egy formájának előállításakor (az MPTP neurotoxinná alakul, amely szelektíven elpusztítja a dopamin sejteket a substantia nigra-ban). Ezek az esetek ritkák, és leginkább a hosszú távú kábítószer-használókat érintik.
a metamfetaminnal való visszaélés a parkinsonizmushoz is kapcsolódik. Kísérleti állatokban a metamfetaminnak való kitettség károsítja a striatum * dopaminerg rostjait, valamint a substantia nigra sejttesteit, visszhangozva a PD-ben szenvedő humán betegeknél megfigyelt degenerációt. A striatumban lévő dopaminerg terminálok szelektív károsodását humán metamfetamin-használóknál is megfigyelték, bár eddig nincs bizonyíték arra, hogy a metamfetamin-visszaélés károsítja a dopaminerg sejttesteket a substantia nigra-ban (Granado et al., 2013).
*a bazális ganglionok legnagyobb magja, a striatum a caudate magból és a putamenből áll.
feltételezték, hogy a metamfetamin használata hajlamosíthatja a felhasználókat a PD jövőbeli fejlődésére. Ezt a hipotézist alátámasztotta a legújabb epidemiológiai munka, amely azt jelzi, hogy a metamfetamin-használóknak fokozott a PD kialakulásának kockázata. Ez összhangban van a metamfetamin perzisztens neurotoxikus hatásával kísérleti állatokban (Granado et al., 2013).
a parkinsonizmusban szenvedő betegeket gyakran nehéz kezelni járóbetegként. A tünetek összetettsége, a hozzáadott kognitív és autonóm deficitek, a legtöbb PD gyógyszerre adott rossz válasz és a viszonylag gyors állapotcsökkenés hozzájárulnak a betegek kezelésének kihívásaihoz, különösen a betegség előrehaladtával (Hohler et al., 2012).