Veraflox(pradofloxacin)猫用経口懸濁液
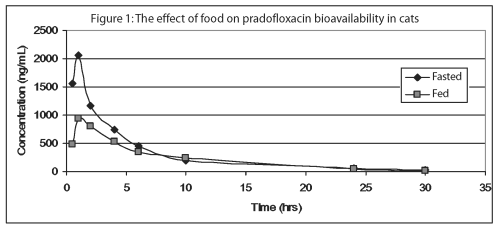
全薬物濃度の約30%が、150-1500ng/mLの薬物濃度で血漿タンパク質に結合しています。 経口懸濁液を2.5mg/kgから10mg/kgの範囲の用量で絶食した猫に投与すると、薬物濃度の用量に比例した増加が観察される。 短い除去の半減期が原因で、多数の毎日の管理に続く最低のpradofloxacinの蓄積があります。
薬力学:
薬力学は、病原体Pasteurella multocida、Staphylococcus pseudintermedius、およびStreptococcus sppを示したin vitro感受性を用いて決定された。 pradofloxacin MIC90を≤0.015から0.12ug/mL持っていました。 薬物動態指標(Cmax/MIC90とAUC/MIC90)は、絶食猫と0.12ug/mLのプラドフロキサシンMIC90値から遊離薬物定常状態プラドフロキサシン薬物動態パラメータの線形回帰分析 予測された平均Cmax/MIC9 0およびAUC/MIC9 0値についての9 5%信頼区間は、それぞれ1 5〜1 7および7 0〜8 1であった。 プラドフロキサシン液体製剤の7.5mg/kg体重の経口用量を絶食猫に投与すると、Cmax/MIC90およびAUC/MIC90値の大きさは、製品の有効性を予測すると結論された。 さらに、有効性は7.5mg/kgの体重で投薬され、自由選択を与えられた猫のために、または投薬の二時間以内に、実地調査で示されました。
:
VERAFLOXは殺菌性があり、グラム陰性、グラム陽性、嫌気性菌に対して活性があります。
2008年から2009年にかけての米国のフィールドスタディにおける猫の皮膚感染(創傷および膿瘍)から単離されたpasteurella multocida、Streptococcus canis、staphylococcus aureus、Staphylococcus felis、およびstaphylococcus pseudintermediusに対するプラドフロキサシンの最小阻害濃度(MICs)を表3に示した。 二つのプラドフロキサシン治療失敗例から二つの分離株のみがプラドフロキサシンMICs(非溶血性ブドウ球菌)を上昇させた。 aureus−MIC=2μ g/ml;e.coli−MIC=4μ g/ml)。
表3. 2008年に米国で臨床試験でVERAFLOXで治療された猫から単離された病原体に対するVERAFLOXの活性。
|
病気 |
病原体 |
臨床治療成績 |
分離株の数 |
サンプルコレクション(処置に関連している時間) |
MIC50μ g/mL |
MIC90μ g/mL |
マイクレンジμ g/mL |
|
皮膚感染症 |
パステウレラ・ムルトシダ |
成功 |
前処理 |
≤0.004 – 0.03 |
|||
|
失敗 |
前処理 |
≤0.004 – 0.015 |
|||||
|
イヌレンサ球菌 |
成功 |
前処理 |
0.03 – 0.25 |
||||
|
失敗 |
前処理 |
0.06 – 0.12 |
|||||
|
黄色ブドウ球菌 |
成功 |
前処理 |
0.015 – 0.12 |
||||
|
失敗 |
|||||||
|
フェリスブドウ球菌 |
成功 |
前処理 |
0.03 – 0.12 |
||||
|
失敗 |
前処理 |
||||||
|
黄色ブドウ球菌 |
成功 |
前処理 |
0.03 – 0.06 |
||||
|
失敗 |
前処理 |
有効性
VERAFLOXの臨床的有効性は、マルチサイト(16サイト)のフィールドスタディで実証されました。 このマスクされた無作為化試験では、VERAFLOXの有効性をプラセボ対照(有効成分を含まないビヒクル)と比較した。 この研究に登録された282匹の猫のうち、190匹を7.5mg/kgで1日1回VERAFLOXで治療しました(3.4mg/lb)体重を7日間連続して、92は0.3mL/kg体重で7日間連続してプラセボで一日一回治療した。 有効性のデータベースは182匹の猫を含んでいた:66の偽薬(車)扱われた猫および116のVERAFLOX扱われた猫。 この有効性データベースの分析は、表4に要約されるように、1 5日目のVERAFLOX群で治癒率がより大きかったことを示した。 研究治癒率は、治療開始後約15日後に決定した。 一次有効性エンドポイント(研究治療法)の統計的評価は、VERAFLOXが73.4%のVERAFLOX研究治療法に対して38.9%のプラセボ研究治療法とプラセボとは異なることを示した。
表4:15日目の症例分類
|
治療グループ |
パーセントの治療法 |
|
ヴェラフロックス = 116 |
73.4% |
|
プラセボ N= 66 |
38.9% |
|
P値 |
動物の安全性
対象動物の安全性試験:32匹の健康な12週齢の子猫に、0、7.9、23.7、または39.5mg/kg(推奨用量の0、1、3、および5倍)の用量で21日間連続してVERAFLOXを一日一回投与した安全性を評価した。 追加の対照(0X)および高用量(5X)動物を、治療中止後4 5日間維持した。
好中球、リンパ球、単球は対照群と比較して3X群および5X群で統計的に有意な減少が認められた。 治療期間中、一つの3X猫と三つの5x猫は、基準範囲以下の絶対好中球数を持っていました。 骨髄抑制(骨髄性形成不全)と一致する骨髄細胞診の結果は、3倍の好中球減少猫および5倍の好中球減少猫のうちの二つで見られた。 3X猫は、予定された安楽死の前の研究の最終日に好中球減少性であったが、5x猫の絶対好中球値は、治療中または治療の中止後に正常に戻った。
最も頻度の高い異常な臨床所見は軟便であった。 これは治療群と対照群の両方で見られたが、3Xおよび5Xの子猫でより頻繁に観察された。
眼の安全性研究: 眼の安全性は、経口投与されたカプセル中のプラドフロキサシンを使用して20の健康な成猫において、30mg/kgおよび50mg/kgの用量で一日一回23日間 眼科検査,Ergs,光コヒーレンストモグラフィーでは効果は見られなかった。 プラドフロキサシンの50mg/kg/日を受けた猫は、軽度の体重減少を示した。 プラドフロキサシンの30および50mg/kg/日を受けた猫は、研究を通じて過唾液分泌および嘔吐を示した。 プラドフロキサシン処理猫では、白血球数の用量依存的な減少が認められた。 プラドフロキサシンの30mg/kg/日を受けている猫は、エンロフロキサシン処理された猫(本研究で使用される比較器)とは異なるタイプの光および電子顕微鏡上で最小限の光受容体変性を示した。
パイロット毒性試験:経口毒性試験では、4匹の猫にプラドフロキサシンを50mg/kg/日で25日間投与した。 すべての猫は嘔吐と過唾液分泌を示した。 ある猫は、研究の5日目にフルオロキノロン誘発性の神経学的徴候(運動性の低下、驚異的な、および発声)を示した。
保管条件
30°C(86°F)以下に保管してください。
初回開封後、VERAFLOXは60日間の使用中の安定性を実証しました。
|
コード番号 |
びんのサイズ |
|
15 mL |
|
|
30 mL |
FDAによって承認される灘141-344
84364593 / 84364607, R.0
ドイツ製
©2012Bayer HealthCare LLC
Bayer、Bayer Cross、VERAFLOXはバイエルの登録商標です。
VERAFLOXは以下の米国特許6,323,213によって保護されています。
Bayer HealthCare LLC,Animal Health Division,Shawnee Mission,Kansas66201,U.S.a.