18.6:에폭사이드의 반응:고리-개방
에폭사이드의 반응:고리-개방 반응-엔 1 대 엔 2,레지오선택성 및 입체선택성
에폭사이드의 비엔지매틱 고리-개방 반응은 이 장에서 이미 본 많은 개념들에 대한 좋은 개요를 제공한다. 링 개방 반응은 에폭 사이드의 성질 및 반응 조건에 따라 엔 2 또는 엔 1 메커니즘에 의해 진행될 수 있습니다. 에폭시 드가 비대칭 인 경우,제품의 구조는 어떤 메커니즘이 지배적인지에 따라 달라질 것입니다. 메탄올에서 비대칭적인 에폭사이드가 용매분해될 때,링-오프닝은 엔 2 메커니즘에 의해 발생하며,치환된 탄소가 적은 친핵성 공격 부위이며,이는 우리가 산물로 지칭할 것이다.:
이미지 120.반대로,산성 메탄올에서 용매 분해가 일어날 때,반응은 실질적인 엔 1 특성을 갖는 메커니즘에 의해 일어나고,더 많은 치환 된 탄소가 공격 부위이다. 그 결과 제품이 우세합니다.
이미지 122.이 두 가지 모두 레지오선택적 반응의 좋은 예이다. 레지오 선택 반응에서,두 개(또는 그 이상)의 상이한 헌법 이성질체가 생성물로서 가능하지만,하나는 우선적으로(또는 때로는 독점적으로)형성된다.
먼저 기본 사례를 살펴 보겠습니다. 이탈 기는 알콕시드 음이온인데,이는 링 개통 전에 산소를 프로토네이트할 수 있는 산이 없기 때문이다. 알콕시드는 빈약한 떠나는 그룹이고,따라서 반지는 친핵체에서’강요’없이 열리기 확률이 낮습니다.
이미지 124.이 이온 중 하나는 음전하를 띤 메톡 사이드 이온과 음전하를 띤 메톡 사이드 이온입니다. 친핵성 치환 반응이 빈약한 떠나는 그룹 및 강력한 친핵성을 관련시킬 때,엔 2 기계장치에 의해 진행하는 것은 아주 확률이 높습니다.
친전 사일러스는 어떻습니까? 에폭사이드에는 2 개의 친전자성 탄소가 있지만,엔 2 반응에서 친핵성에 대한 가장 좋은 표적은 방해가 가장 적은 탄소이다. 이것은 관찰 된 지역 화학적 결과를 설명합니다. 다른 엔 2 반응에서와 마찬가지로 친 핵성 공격은 후면에서 일어나며,그 결과 친 전자 성 탄소에서 반전이 발생합니다.
아마 산 촉매 에폭시 드 고리 개방 반응을 묘사하는 가장 좋은 방법은 하이브리드,또는 교차,사이 엔 2 과 엔 1 메커니즘. 첫째,산소가 양성자화되어 좋은 탈퇴 그룹을 만듭니다(아래 1 단계). 그런 다음 탄소-산소 결합이 깨지기 시작하고(2 단계)양전하가 더 많은 치환 된 탄소에 축적되기 시작합니다(탄화 안정성에 관한 섹션 8.4 에서 논의 된 것을 상기하십시오).
이미지 126.(3 단계)완전한 탄화 중간체가 형성되기 전에 친핵체는 친 전자 성 탄소를 공격한다.
이미지 128.왜냐하면 탄소-산소 결합은 여전히 어느 정도 제자리에 있고,산소 블록은 앞쪽에서 공격하기 때문이다. 그러나 공지 사항,,어떻게 지역 화학 결과 기본 촉매 반응에서 다른: 산 촉매 작용 과정에서는,친핵체는 양전하의 더 중대한 정도를 보전되기 이 탄소이기 때문에 대용한 탄소를 공격한다.
실시예 18.6.1
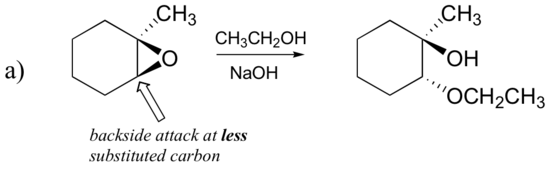
아래 도시된 에폭사이드가 다음과 같이 처리될 때 발생하는 고리 개방 반응의 주요 생성물(들)을 예측한다:
- 에탄올 및 소량의 수산화 나트륨
- 에탄올 및 소량의 황산
힌트:지역 화학과 입체 화학을 모두 고려하십시오!
답변
이미지 430.팩스:86-755-8211500