16.10: Elektrofil Tillegg: 1,2-Versus 1,4-Tillegg
Addisjonsreaksjoner av isolerte diener fortsetter mer eller mindre som forventet fra oppførselen til enkle alkener. Således, hvis en molar ekvivalent av 1,5-heksadien behandles med en ekvivalent av brom, oppnås en blanding av 5,6-dibromo-1-heksen, 1,2,5,6-tetrabromohexan og uomsatt dien, med dibromoforbindelsen som hovedproduktet (ca. 50%)
fig
Lignende reaksjoner av konjugerte diener, derimot, gir ofte uventede produkter. Tilsetningen av brom til 1,3-butadien er et eksempel. Som vist nedenfor oppnås en omtrent 50: 50 blanding av 3,4-dibromo-1-buten (forventet produkt) og 1,4-dibromo-2-buten (hovedsakelig E-isomeren). Den sistnevnte forbindelsen er bemerkelsesverdig ved at den gjenværende dobbeltbindingen er funnet på et sted der det ikke var dobbeltbinding i reaktanten. Denne interessante flyttingen krever en forklaring.
CH2=CH-CH=CH2 + Br2  |
BrCH2CHBr-CH=CH2 + | BrCH2CH=CHCH2Br |
| 3,4-dibromo-1-buten | 1,4-dibromo-2-buten |
det forventede addisjonsproduktet fra reaksjoner av denne typen er resultatet av 1,2-addisjon, dvs. binding til tilstøtende karboner av en dobbeltbinding. Det uventede produktet kommer fra 1,4-tillegg, dvs. binding ved de terminale karbonatomer av en konjugert dien med et skifte av gjenværende dobbeltbinding til 2,3-stedet. (Disse tallene refererer til de fire karbonene i den konjugerte dien og er ikke iupac-nomenklaturnumre.) Produktblandinger er ofte temperaturavhengige: ved 40 oC er 85% av produktblandingen i tilleggsreaksjonen ovenfor 1,4-produktet, mens ved 0 oC er bare ca. 30% 1,4-produktet.
Binding av et elektrofilt atom eller gruppe til et av karbonatomene i en konjugert dien (karbon #1 i figuren nedenfor) genererer et allylkation-mellomprodukt. Slike kationer stabiliseres ved ladningsdelokalisering, og det er denne delokaliseringen som står for 1,4-addisjonsproduktet produsert i slike addisjonsreaksjoner. Som vist i diagrammet fordeles den positive ladningen over karboner #2 og # 4, så det er på disse stedene at nukleofile komponentbindinger. Merk at resonansstabilisering av allylkation er større enn sammenlignbar stabilisering av 1,3-butadien, fordi ladning er delokalisert i den tidligere, men skapt og separert i sistnevnte.
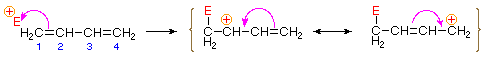
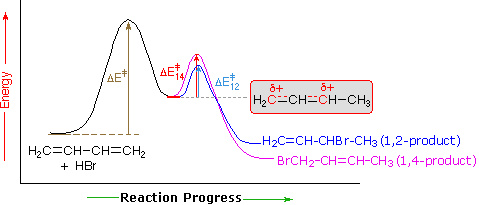
en forklaring på temperaturpåvirkningen er vist i følgende energidiagram for tilsetning Av HBr til 1,3-butadien. Det første trinnet der et proton bindes til karbon # 1 er det hastighetsbestemmende trinnet, som angitt av den store aktiveringsenergien (lysegrå pil). Det andre raskere trinnet er produktets bestemmende trinn ,og det er to reaksjonsbaner(farget blå for 1,2-tillegg og magenta for 1,4-tillegg). 1,2-tillegget har en mindre aktiveringsenergi enn 1,4-tillegg-det skjer raskere enn 1,4-tillegg, fordi bromidnukleofilen er nærmere karbon # 2 og deretter karbon #4. 1,4-produktet er imidlertid mer stabilt enn 1,2-produktet. Ved lave temperaturer dannes produktene irreversibelt og reflekterer de relative prisene for de to konkurrerende reaksjonene. Dette kalles kinetisk kontroll. Ved høyere temperaturer etableres likevekt mellom produktene, og det termodynamisk favoriserte 1,4-produktet dominerer.
når en konjugert dien angripes av en elektrofil, er de resulterende produktene en blanding av 1,2 og 1,4 isomerer. Kinetikk og Termodynamikk styrer en reaksjon når det er to produkter under forskjellige reaksjonsforhold. Det Kinetiske produktet (Produkt A) vil bli dannet raskt, Og Det Termodynamiske produktet (Produkt B) vil bli dannet sakte. Vanligvis er det første produktet dannet det mer stabile favoriserte produktet, men i dette tilfellet er det langsommere produktet dannet det mer stabile produktet; Produkt B.
Introduksjon
som ikke-konjugerte diener, konjugerte diener er utsatt for angrep av elektrofiler. Faktisk opplever konjugerte elektrofiler relativt større kinetisk reaktivitet når de reageres med elektrofiler enn ikke-konjugerte diener gjør. Ved elektrofil tilsetning danner den konjugerte dien en blanding av to produkter—det kinetiske produktet og det termodynamiske produktet—hvis forhold bestemmes av reaksjonsbetingelsene. En reaksjon som gir mer termodynamisk produkt er under termodynamisk kontroll, og på samme måte er en reaksjon som gir mer kinetisk produkt under kinetisk kontroll.
Grunnleggende Reaksjon
Detaljert Mekanisme
Konklusjon
reaktiviteten av konjugerte diener (hydrokarboner som inneholder to dobbeltbindinger) varierer avhengig av plasseringen av dobbeltbindinger og reaksjonstemperaturen.Disse reaksjonene kan produsere både termodynamiske og kinetiske produkter. Isolerte dobbeltbindinger gir diener med mindre stabilitet termodynamisk enn konjugerte diener. Imidlertid er de mer reaktive kinetisk i nærvær av elektrofiler og andre reagenser. Dette er et resultat Av Markovnikov tillegg til en av de doble obligasjoner. En karbokasjon dannes etter at en dobbeltbinding er åpnet. Denne karbokasjonen har to resonansstrukturer, og tillegg kan forekomme ved en av de positive karbonene.
Praksis Problemer
- Skriv ut produktene av 1,2 tillegg og 1,4-tillegg av a) HBr Og Br. b) DBr til 1,3-cyclo-heksadien. Hva er uvanlig om produktene av 1,2 – og 1,4-tillegg AV HX til usubstituerte sykliske 1,3-diener?
- dannes 1,2-tilleggsproduktet raskere ved høyere temperaturer, selv om det er 1,4-tilleggsproduktet som dominerer under disse forholdene?
- Hvorfor er 1,4-tilleggsproduktet det termodynamisk mer stabile produktet?
- ut av følgende radikale kationer hvilken er ikke en rimelig resonansstruktur?
5. Tilsetning av 1 ekvivalent Brom til 2,4-heksadien ved 0 grader C gir 4,5-dibromo-2-heksen pluss en isomer. Hvilken av følgende er at isomer:
- 5,5-dibromo-2-heksen
- 2,5-dibromo-3-heksen
- 2,2-dibromo-3-heksen
- 2,3-dibromo-4-heksen
6. Hvilket av følgende vil være det kinetisk favoriserte produktet fra den avbildede reaksjonen?
7. Tilsetning Av HBr til 2,3-dimetyl-1,3-cykloheksadien kan forekomme ved fravær eller tilstedeværelse av peroksider. I hvert tilfelle oppnås to isomere c8h13br-produkter. Hvilket av følgende er et vanlig produkt fra begge reaksjonene?
8. og 9.
8. Det kinetisk kontrollerte produktet i ovennevnte reaksjon er:
- 3-Klor-1-Buten
- 1-Klor-2-Buten
9. For reaksjonen i spørsmål 8, hvilken er resultatet av 1,4-tillegg?
- 3-Klor-1-Buten
- 1-Klor-2-Buten
Svar på Problemer
1. A) Samme produkt for begge modi av tillegg.
både cis-og trans-isomerer dannes.
Tilsetning AV HX til usubstituerte cycloalka-1,3-diener på enten 1,2 – eller 1,4 – måte gir det samme produktet fordi symmetri.
2. Ja. Det Kinetiske Produktet vil fortsatt dannes raskere, men i dette tilfellet vil det være nok energi til å danne det termodynamiske produktet fordi det termodynamiske produktet fortsatt er mer stabilt.
3. 1,4-produktet er mer termodynamisk stabilt fordi det er to alkylgrupper på hver side av dobbeltbindingen. Dette skjemaet gir stabilitet til den generelle strukturen.
4. Alle disse isomerer er levedyktige.
5. D
6. C
7. D
8. En
9. B
Bidragsytere
-
William Reusch, Professor Emeritus (Michigan State U.), Virtuell Lærebok For Organisk Kjemi
-
Jim Clark Chemguide.co.uk)
- Natasha Singh