Artikkel
John Plante*, Chelsea Eason, Alan Snyder, Dirk Elston
Institutt For Dermatologi Og Dermatologisk Kirurgi, Medical University Of South Carolina, Charleston, South Carolina
Lichen planopilaris (LPP) er en primær cicatricial alopecia preget av kløe, Ømhet, follikulære spines og Erytem I Den Aktive Fasen1-3. Selv om den nøyaktige etiologien er ukjent, involverer patogenesen kronisk, lymfocyttmediert betennelse som til slutt kan føre til irreversibelt, arrdannende hårtap gjennom selektiv ødeleggelse av hårsekken1, 2. Tre varianter av LPP eksisterer og inkluderer den klassiske formen, frontal fibrosing alopecia (FFA) og Graham-Little-Piccardi-Lassueur syndrom (progressiv alopecia i hodebunnen, axillae, brows og pubis)2. LPP viser seg ofte ildfast mot standard terapi og følger en uforutsigbar, relapsing kurs, ofte fører til en alvorlig redusert livskvalitet 1, 2,4, 5. Her diskuterer vi videre vår siste studie om bruk av tofacitinib i behandlingen AV tilbakevendende LPP6.
Tallrike terapier har blitt brukt til å behandle LPP med variabel suksess1-3,5,7-9. Siden tilgjengelige behandlinger ikke vanligvis fører til gjenvekst, er ledelsen rettet mot å redusere frekvensen av hårtap, kontrollere symptomer og redusere betennelse2,9. Førstelinjeterapier inkluderer intralesional og høypotente topiske kortikosteroider, men disse kan resultere i hodebunnsatrofi og kompromittere suksessen til fremtidig hårtransplantasjon. Andre topikale midler har mindre risiko for atrofi og inkluderer kalsinevrinhemmerne takrolimus og pimecrolimus2. Selv om det ikke kontrollerer den underliggende inflammatoriske prosessen, kan både aktuell og oral minoxidil også brukes til å maksimere veksten hos pasienter som også lider av arvelig mønster alopecia-nesten 50% av befolkningen9,10. Andre systemiske behandlinger inkluderer hydroksyklorokin, mykofenolatmofetil, ciklosporin, metotreksat, thalidomid, doksycyklin, retinoider, pioglitazon, 5-alfa reduktasehemmere og kortsiktig prednisolon1,2,9. Nyere studier har antydet potensialet for lavdose oral naltrexon, blodplate-rike plasma injeksjoner, og ikke-farmakologiske intervensjoner som excimer laser, men ingen har vært jevnt effektiv5, 7, 8. Mens hårstykker og extensions kan øke volumet og dekke alopecic områder, må forsiktighet utvises for å unngå trekkraft9.
i en nylig publisert studie undersøkte vi potensialet for topiske og orale (systemiske) formuleringer av tofacitinib6. Tofacitinib er En janus kinase (JAK) 1/3-hemmer med effekt mot flere immunmedierte dermatologiske tilstander, inkludert atopisk dermatitt, alopecia areata og vitiligo 11-14. Dens immunmodulerende aktivitet medieres gjennom hemming AV JAK / STAT signalveien 12, 13. I LPP har interferoner vært involvert i å legge til rette for lymfocytisk rekruttering og tap av utbulende epitelcelleimmunprivilegium1. Gjennom tofacitinibs effekter PÅ jak / STAT-banen, kan denne interferonmedierte betennelsen reduseres, og dermed forbedre symptomene og forhindre ytterligere follikulær destruksjon1, 11-13.
vi undersøkte det terapeutiske potensialet til tofacitinib ved behandling av refraktær LPP gjennom en retrospektiv kartgjennomgang6. Til forfatterens kunnskap er dette den andre studien som undersøker tofacitinibs bruk I lpp-ledelse1. Vår studie inkluderte ni pasienter som hadde mislyktes annen terapi-tre brukte aktuell, fem brukte oral og en brukte begge formuleringene.
en gunstig innledende respons ble oppnådd hos alle unntatt en pasient. Den gjenværende forsøkspersonen responderte dårlig på topikal behandling, men bedret seg med systemisk tofacitinibbehandling. Selv om det absolutte antall pasienter er lite, var det en trend mot bedre klinisk respons hos de som fikk systemisk i forhold til de som fikk lokal behandling. Tiden til en gunstig respons varierte fra 1 til 7 måneder, med 5 og 8 pasienter som viste bedring i løpet av henholdsvis de første 3 og 5 månedene av behandlingen.
vårt nåværende praksismønster er å behandle raskt progressiv sykdom med en kort kur med prednison eller ciklosporin og deretter forsøke å gå over til aktuell kalsinevrinhemmerbehandling når det er mulig (Figur 1). En undergruppe av pasienter vil oppnå remisjon av sykdommen med pioglitazon i doser på 15-45 mg daglig. Pasienter bør informeres om merket indikasjon, blandede data angående effekt og boksadvarsel om blærekreft ved langvarig bruk. Vår praksis er ikke å fortsette pioglitazon etter maksimalt 9 måneder med økende doser i trinn. Tilleggsmidler inkluderer naltrekson i en dose på 5 mg daglig og n-acetylcystein i doser på 600-1200 mg tre ganger daglig. Excimer laser, håndholdt smalbånd UVB eller lav intensitet laser cap terapi brukes ofte som tilleggsbehandling hos de med delvis respons. Hydroksyklorokin kan noen ganger være til nytte, men de fleste pasientene som er henvist til vår klinikk, har allerede sviktet hydroksyklorokinbehandling. De som ikke responderer kan kreve behandling med metotreksat, mykofenolatmofetil eller tofacitinib. Resultatene fra vår siste studie gir ytterligere støtte til ideen om at både aktuell og systemisk tofacitinib kan være levedyktige tilleggsbehandlingsmodaliteter i refraktære tilfeller. Hårforstyrrelser reagerer ofte sakte, og vi revurderer med 3 måneders intervaller for å bestemme respons på terapi og behov for eskalering.
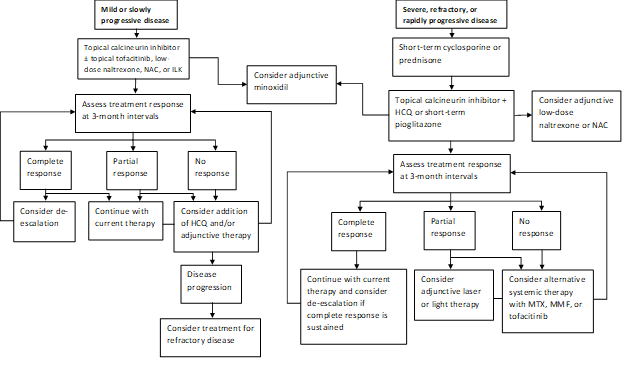
Figur 1: Trinnvis Behandlingsalgoritme FOR LPP
NAC, n-acetylcystein; ILK, intralesional kortikosteroider; HCQ, hydroksyklorokin; MTX, metotreksat, MMF, mykofenolatmofetil
når man vurderer tofacitinibs bruk i praksis, må utøvere balansere fordelene med denne medisinen med risikoen. Vår kohort opplevde bare mindre laboratorieavvik (en på aktuell og to på systemisk terapi) som ikke krever intervensjon. Leverandører bør imidlertid være oppmerksomme på de potensielle bivirkningene ved forskrivning av denne medisinen, inkludert økt risiko for infeksjon, cytopenier, hyperlipidemi, lever-og nyreavvik, samt potensialet for tromboemboliske hendelser14-16. Selv om topikal formulering har vist lavere plasmakonsentrasjoner enn den systemiske motparten, er det fortsatt rapportert mindre bivirkninger og unormale laboratorieverdier ved topikal behandling13.
mens våre resultater er lovende, må de tolkes etter å ha vurdert flere begrensninger. Vi brukte en retrospektiv studiedesign, og var ikke i stand til å benytte et validert mål på sykdoms alvorlighetsgrad som Lichen Planopilaris Activity Index (LPPAI)1,3. LPPAI er egnet for prospektive studier og gir et standardisert verktøy som leverandører kan direkte sammenligne resultater på tvers av ulike behandlingsmodaliteter. Tegn og symptomer som erytem, ømhet, tilstedeværelse av follikulære spines og berørt område ble brukt til å vurdere terapeutisk respons, men fremtidige studier bør også inkludere et mål på livskvalitet. Muligheten for observatørskjevhet kan ikke utelukkes da vår studie var avblindet og ikke-randomisert.
i tillegg brukte hele vår kohort tofacitinib supplement, noe som gjør det vanskelig å vurdere stoffets uavhengige bidrag. I en tidligere studie ble en del (N=5) av kohorten brukt tofacitinib som monoterapi, og de fleste forsøkspersonene oppnådde gunstige resultater, men denne studien ble også begrenset av den lille prøvestørrelsen og retrospektiv design1.
Nåværende studier er begrenset av deres små utvalgsstørrelser og retrospektive studiedesign, og veldesignede prospektive studier er sårt trengte. Vi anbefaler en trinnvis tilnærming til terapi for å minimere risikoen for bivirkninger. Risikoen for permanent arrdannelse må veies opp mot risikoen for alvorlige bivirkninger i lys av individuelle pasientfaktorer og komorbiditet, og pasientene bør være aktive partnere i beslutningsprosessen. Hårtransplantasjon kan vurderes når sykdomskontroll er oppnådd og betennelse avtar. Det er viktig å merke seg at aggressiv behandling som prednison eller ciklosporin vanligvis er nødvendig i ukene etter transplantasjon for å unngå utbrudd av sykdom. Gradvis slitasje av transplanterte hår kan forventes, selv etter vellykket transplantasjon, men data tyder på at pasientene generelt er fornøyd med resultatene og finner at transplantasjon forbedrer livskvaliteten.
Forkortelser
LPP, lichen planopilaris; FFA, frontal fibrosing alopecia; JAK, Janus kinase; STAT, signaltransduser og aktivator av transkripsjonsproteiner; Lppai, Lichen Planopilaris Aktivitetsindeks.
Interessekonflikter
forfatterne erklærer ingen interessekonflikter.
- Yang CC, Khanna T, Sallee B, Et al. Tofacitinib til behandling av lichen planopilaris: en case-serie. Dermatol Ther. 2018; 31 (6): e12656. doi: 10.1111 / dth.12656
- Babahosseini H, Tavakolpour S, Mahmoudi H, Et al. Lichen planopilaris: retrospektiv studie på egenskaper og behandling av 291 pasienter. J Dermatolog Behandle. 2019; 30(6): 598–604. doi:10.1080/09546634.2018.1542480
- C, C. D., Cho BK, Et al. Hydroksyklorokin og lichen planopilaris: effekt og innføring Av Lichen Planopilaris Activity Index scoring system. J Am Acad Dermatol. 2010; 62(3): 387-392. doi: 10.1016 / j.jaad.2009.08.054
- Alirezaei P, Ahmadpanah M, Rezanejad A, et al. Sammenlignet Med Kontroller Har Personer Med Lavplanopilaris Mer Depresjon, Lavere Selvtillit og Lavere Livskvalitet. Neuropsykobiologi. 2019; 78(2): 95-103. doi:10.1159/000499135
- Jha AK. Blodplaterikt plasma som tilleggsbehandling hos lichen planopilaris. J Am Acad Dermatol. 2019; 80 (5): e109-e110. doi: 10.1016 / j.jaad.2018.09.013
- Plante J, Eason C, Snyder A, et al. Tofacitinib i behandling av lichen planopilaris: en retrospektiv gjennomgang . J Am Acad Dermatol. 2020; S0190-9622 (20)30979-8. doi:10.1016 / j.jaad.2020.05.104
- Lajevardi V, Salarvand F, Ghiasi M, Et al. Effekt og sikkerhet av oral lavdose naltrekson versus placebo hos pasienter med lichen planopilaris: en randomisert kontrollert klinisk studie . J Dermatolog Behandle. 2020; 1-5. doi:10.1080/09546634.2020.1774488
- Lee B, Elston DM. Bruken av naltrexon i dermatologiske forhold. J Am Acad Dermatol. 2019; 80(6): 1746-1752. doi: 10.1016 / j.jaad.2018.12.031
- Bolduc C, Sperling lc, Shapiro J. Primær arrdannelse: Lymfocytisk primær cicatricial alopecias, inkludert kronisk kutan lupus erythematosus, lichen planopilaris, frontal fibrosing alopecia Og Graham-Little syndrom. J Am Acad Dermatol. 2016; 75(6): 1081-1099.
- Vano-Galvan S, Trindade De Carvalho L, Saceda-Corralo D, Et al. Oral minoxidil forbedrer bakgrunnen hår tykkelse i lichen planopilaris . J Am Acad Dermatol. 2020; S0190-9622 (20)30566-1. doi: 10.1016 / j.jaad.2020.04.026
- Tegtmeyer K, Zhao J, Maloney NJ, Et al. Off-label studier på tofacitinib i dermatologi: en gjennomgang . J Dermatolog Behandle. 2019; 1–11. doi: 10.1080/09546634.2019.1673877
- Montilla AM, Gomez-Garcia F, Gomez-Arias PJ, et al. Scoping Gjennomgang På Bruk AV Legemidler Rettet MOT JAK / STAT Vei I Atopisk Dermatitt, Vitiligo, Og Alopecia Areata. Dermatol Ther (Heidelb). 2019; 9(4): 655–683. doi: 10.1007 / s13555-019-00329-y
- Hosking ER, Juhasz M, Mesinkovska NA. Aktuelle Janus kinasehemmere: en gjennomgang av applikasjoner i dermatologi. J Am Acad Dermatol. 2018; 79(3): 535–544. doi: 10.1016 / j.jaad.2018.04.018
- Shreberk-Hassidim R, Ramot Y, Zlotogorski A. Janus kinasehemmere i dermatologi: en systematisk gjennomgang. J Am Acad Dermatol. 2017; 76(4): 745-753.e19. doi: 10.1016 / j.jaad.2016.12.004
- xeljanz / xeljanz XR (tofacitinib) . New York, NY: Pfizer Laboratories Divisjon Av Pfizer Inc. https://labeling.pfizer.com/showlabeling.aspx?id=959; 2019. Tilgjengelig 7.Juli 2020.
- FDA. Sikkerhetsstudie finner risiko for blodpropp i lungene og død med høyere dose tofacitinib (Xeljanz, Xeljanz XR) hos pasienter med revmatoid artritt; FDA for å undersøke. https://www.fda.gov/drugs/drug-safety-and-availability/safety-trial-finds-risk-blood-clots-lungs-and-death-higher-dose-tofacitinib-xeljanz-xeljanz-xr; 2019. Tilgjengelig 6.Juli 2020.