tert-Butyl lithium Eller t-BuLi
Ben Valsler
Denne uken snakker Katrina Krä til en forsker som håper å temme et farlig reagens med salte løsningsmidler.
Katrina Krä
det er noen kjemikalier du virkelig ikke vil rote med – dioxygen difluorid, for eksempel, som reagerer voldsomt med alle slags forbindelser selv ved -180°C; eller kvikksølvazid, som ikke bare detonerer ved den minste provokasjon, men også spytter ut giftige kvikksølvforbindelser når det eksploderer. Heldigvis er disse kjemiske kuriositeter, noe forskere laget en gang, men det er usannsynlig at de noen gang gjør igjen (med god grunn). Imidlertid er andre farlige forbindelser bare så nyttige at kjemikere ikke kan holde hendene av dem. En av dem er tert-butyl litium, også kalt t-BuLi: en stift for syntetiske kjemikere som har en ganske pyroforisk side til den.
Som hovedgruppe organometallisk kjemiker Har Eva Hevia fra University Of Strathclyde ikke bare jobbet med t-BuLi, men også med mange andre alkyllitiumforbindelser.

Kilde: ©
Eva Hevia
Organolithium forbindelser er mye brukt over hele verden – og det er ikke bare i akademia-i mai industrielle og kommersielle situasjoner disse reagensene er avgjørende. Jeg tror det er 90-95 prosent av legemidler som er produsert av farmasøytiske selskaper, de krever, i hvert fall i ett trinn av deres syntese, bruken av disse reagensene. Så implikasjonene for samfunnet, og også for økonomien, er enorme.
Katrina Krä
disse forbindelsene forblir populære delvis På grunn av den store polariteten over litium-karbonbindingen, noe som gjør dem ekstremt reaktive.
Eva Hevia
men selvfølgelig kommer reaktivitet alltid med en handel. Handelen her er at disse reagensene noen ganger lider av lave selektiviteter; noen ganger begrenser de mye typen underlag som de kan være kompatible med. Så for å prøve å overvinne disse begrensningene, må du i mange tilfeller bruke disse reagensene under svært lave temperaturer, med løsemidler som er relativt giftige, og du må alltid bruke dem i fravær av luft eller fuktighet fordi de dekomponerer veldig raskt. Og faktisk er mange av dem pyroforiske, så du må være veldig forsiktig med hvordan du manipulerer disse reagensene. Dette kan være spesielt utfordrende når vi ser på reaksjoner i større skala i et industriscenario.
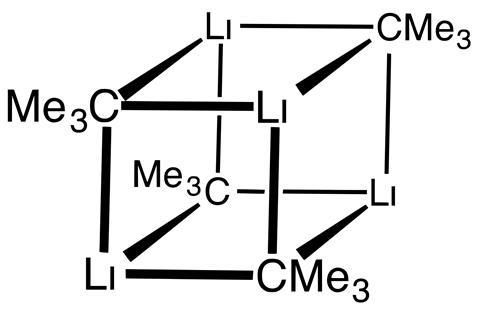
tert-butyl litium
Kilde: Smokefoot, CC-BY-SA 4.0
Katrina Krä
Litium er et av de elementene som virkelig ønsker å kvitte seg med en av sine elektroner, som den skyver mot nabokarbonet. Men det som virkelig gjør t-BuLi reaktiv, sammenlignet med sin mye vennligere lineære fetter n-butyllitium, er at tertiært karbon ikke liker å håndtere litiums overskuddselektron. Å være omgitt av tre metylgrupper som allerede mildt elektron donerer pluss den ekstra elektronen betyr at det sentrale karbonet har mye lokalisert negativ ladning. Følgelig er t-BuLi svært grunnleggende og plukker protoner fra alt det kan nå: fra litt sure organiske forbindelser til vanlige løsningsmidler som tetrahydrofuran eller dietyleter, og selvfølgelig vann.
selv små mengder vann (som vanndamp i luft) og oksygen er nok til å gi en voldsom reaksjon. Ved kontakt med luft brister t-BuLi spontant i lyse oransje flammer. Siden t-BuLi også reagerer med de fleste løsningsmidler, selger kjemiske selskaper det som en fortynnet løsning i ureaktiv heksan eller pentan, som begge også er brannfarlige. Dette betyr at hvis det er en organolithium brann, er det vanligvis en slags brannfarlig løsemiddel i blandingen også.

Kilde: © bilde gjengitt Av Naveen Sangji
sheharbano Sangjis tragiske ulykke førte til kriminelle anklager Og en endring i laboratoriesikkerhetskulturen
det tragiske tilfellet AV ucla-student Sheri Sangji, som døde i 2009 fra store forbrenninger etter at et eksperiment med store mengder t-BuLi gikk galt, bør minne hver kjemiker om at denne forbindelsen må behandles med respekt. Forskere som arbeider med t-BuLi må overholde strenge sikkerhetstiltak: bruk bare små mengder og utføre reaksjoner under utelukkelse av luft og fuktighet mens iført ikke-brennbare klær og har både en bekymret labmate og en nøddusj i nærheten er de minste minimumskravene for å håndtere t-BuLi trygt.
mens alkyllitium er kraftige reagenser, er de også utsatt for sidereaksjoner, og danner ubrukelige biprodukter. Dette, i tillegg til sikkerhetsbekymringene, er grunnen til at kjemikere vanligvis utfører reaksjoner ved -78°C og opprettholder en inert gassatmosfære i reaksjonskarene for å holde ut luft og fuktighet.
Eva Hevia
og jeg antar at den ultimate utfordringen i denne typen kjemi er hvordan vi kan bruke dem i en normal atmosfære, uten tilstedeværelse av argon eller nitrogengass – under luft-og hvordan vi kan gjøre disse reagensene kompatible med løsemidler som er miljømessig godartet. Og det vi har funnet er at hvis vi bruker dype eutektiske løsningsmidler som et alternativbe media – og et dypt eutektisk løsningsmiddel er en ny type løsemiddel, relatert til ioniske væsker, som er miljømessig godartede, bestående av komponenter som er bionedbrytbare og biorenewable – hvis vi bruker denne typen løsemidler, kan vi aktivere organolithium løsemidler på en slik måte at reaksjonene skjer ekstremt raskt ved romtemperatur. Fordi de er veldig raske, trenger du ikke å bruke en inert atmosfære, og du kan gjøre disse reaksjonene kompatible med vann eller fuktighet.
Katrina Krä
Dype eutektiske løsemidler er blandinger av forskjellige salter som er flytende ved romtemperatur. Mens de fleste ioniske forbindelser har et meget høyt smeltepunkt (natriumklorid for eksempel klokker inn på like over 800 grader), blander de riktige saltene i de riktige mengdene en eutektisk – en blanding som smelter ved en mye lavere temperatur enn de enkelte komponentene. Disse ganske uvanlige løsningsmidlene er giftfri og ganske billig – En av Forbindelsene Hevia ‘ s team bruker er kolinklorid, et kyllingforadditiv.
i dype eutektiske løsningsmidler er organolitiumreaksjoner mye raskere enn i noe annet løsningsmiddel. Dette vil tyde på at allerede svært reaktive alkyllitiumforbindelser blir mer reaktive i den salte løsningsmiddelblandingen, som virker counterintuitive. Hvordan hadde Hevias team ikke behov for å kontrollere reaksjonen ved å kjøle den eller gjennomføre den under inert atmosfære?
Eva Hevia
når du arbeider i disse systemene, er hovedfienden av reaksjonene hydrolyse eller dekomponering av ditt organometalliske reagens. Så vi aktiverer det på en måte som vi kan overvinne denne nedbrytningsveien. Samtidig justerer vi deres selektivitet, så vi finner i typen reaksjoner som vi ser på at vi får bedre selektivitet enn når vi bruker konvensjonelle løsningsmidler.
Katrina Krä
fordi de består av ioner, er dype eutektiske løsningsmidler veldig gode til å stabilisere ladede eller svært polare molekyler; men nøyaktig hvordan de virker deres magi er ikke klart ennå. Hevia mener at de salte løsningsmidlene også kan temme andre mer spirituelle organometalliske reagenser.
Eva Hevia
Noe av vårt første arbeid har vist at Vi kan bruke Grignardreagenser som også er veldig grunnleggende og svært viktige i syntese. Og noe av arbeidet som for tiden gjennomgår i våre forskningsgrupper viser at disse løsningsmidlene også gir stort potensial for organo-sink-reagenser som igjen er mye ansatt i mange karbon-karbonbindingsdannende prosesser, og de er også svært reaktive i nærvær av luft og fuktighet. Så jeg tror det er to måter å se på dette arbeidet: for det første utvikler vi nye metoder for å bruke disse reagensene under miljømessige gunstige forhold, men for det andre – og dette er noe jeg virkelig vil understreke-aktiverer vi disse organometalliske reagensene, enten dette er organo-litiium,- sink eller-magnesium, for å få dem til å fungere enda bedre enn når vi bruker inerte atmosfæreforhold eller flyktige organiske løsemidler.
Katrina Krä
selv om kjemikere fortsatt trenger å håndtere t-BuLi og dets brødre med forsiktighet, kan dype eutektiske løsemidler hjelpe dem til å veilede t-BuLi ‘ s kanonkule reaktivitet med mer pillignende presisjon.
Ben Valsler
Det Var Katrina Krä, snakket Med Eva Hevia fra University Of Strathclyde om tert-butyl litium eller t-BuLi. Neste uke Er Brian Clegg tilbake med en familie av forbindelser med noen om bruk.
Brian Clegg
De er bemerkelsesverdig konstruktive – sjelden direkte i bruk selv, men hver er en viktig bidragsyter av byggeklosser til andre forbindelser. Dessverre kan noen av disse sluttproduktene brukes i kjemiske våpen.
Ben Valsler
Bli Med Brian neste uke for å finne ut mer. Inntil da, gi oss beskjed hvis det er noe du vil at vi skal dekke-e-post [email protected] eller tweet @chemistryworld. Jeg Er Ben Valsler, takk for at du lyttet.