16.10: elektrofiele additie: 1,2 – Versus 1,4-additie
additie reacties van geïsoleerde dienenen verlopen min of meer zoals verwacht uit het gedrag van eenvoudige alkenen. Als een molair equivalent van 1,5-hexadieen wordt behandeld met een equivalent van broom, wordt een mengsel van 5,6-dibroom-1-hexeen, 1,2,5,6-tetrabroomhexaan en niet-gereageerde dieen verkregen, waarbij de dibroomverbinding het belangrijkste product is (ongeveer 50%)
fig
soortgelijke reacties van geconjugeerde dieen daarentegen vaak onverwachte producten opleveren. De toevoeging van broom aan 1,3-butadieen is een voorbeeld. Zoals hieronder getoond, wordt een ongeveer 50:50 mengsel van 3,4-dibroom-1-buteen (het verwachte product) en 1,4-dibroom-2-buteen (voornamelijk het E-isomeer) verkregen. De laatste verbinding is opmerkelijk omdat de resterende dubbele binding wordt gevonden op een plaats waar er geen dubbele binding in de reactant. Deze interessante verhuizing vraagt om uitleg.
CH2=CH-CH=CH2 + Br2  |
BrCH2CHBr-CH=CH2 + | BrCH2CH=CHCH2Br |
| 3,4-dibromo-1-buteen | 1,4-dibromo-2-buteen |
De verwachte toevoeging product uit de reacties van deze soort is het resultaat van 1,2-aanvulling, d.w.z. het verlijmen van de aangrenzende koolstofatomen van de dubbele binding. Het onverwachte product komt van 1,4-additie, dat wil zeggen binding aan de terminale koolstofatomen van een geconjugeerd dieen met een verschuiving van de resterende dubbele binding naar de 2,3-locatie. (Deze getallen verwijzen naar de vier koolstofatomen van de geconjugeerde dieen en zijn geen IUPAC-nomenclatuurnummers.) Productsamenstellingen zijn vaak temperatuurafhankelijk: bij 40 oC is 85% van het productmengsel in de bovenstaande additie het 1,4 product, terwijl bij 0 oC slechts ongeveer 30% het 1,4 product is.
de binding van een elektrofiel atoom of groep aan een van de eindkoolstofatomen van een geconjugeerd dieen ( koolstof #1 in de onderstaande figuur) genereert een allylkation-tussenproduct. Dergelijke kationen worden gestabiliseerd door ladingdelokalisatie, en het is deze delokalisatie die voor het 1,4-toevoegingsproduct verantwoordelijk is dat in dergelijke toevoegingsreacties wordt geproduceerd. Zoals getoond in het diagram, wordt de positieve lading verdeeld over koolstof #2 en #4 dus is het op deze plaatsen dat de nucleofiele component bindt. Merk op dat de resonantiestabilisatie van het allylkation groter is dan een vergelijkbare stabilisatie van 1,3-butadieen, omdat lading in het eerste wordt gedelokaliseerd, maar in het laatste wordt gecreëerd en gescheiden.
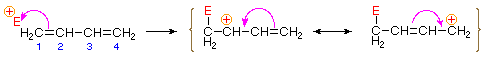
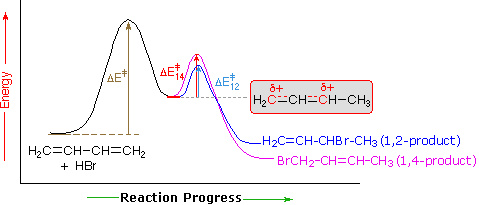
een verklaring voor de invloed van de temperatuur wordt getoond in het volgende energiediagram voor de toevoeging van HBr aan 1,3-butadieen. De eerste stap waarin een proton bindt aan koolstof # 1 is de snelheidsbepalende stap, zoals aangegeven door de grote activeringsenergie (lichtgrijze pijl). De tweede snellere stap is de productbepalende stap, en er zijn twee reactiepaden (gekleurd blauw voor 1,2-toevoeging en magenta voor 1,4-toevoeging). De 1,2-additie heeft een kleinere activeringsenergie dan 1,4-additie-het komt sneller voor dan 1,4-additie, omdat het bromide-nucleofiel dichter bij koolstof # 2 ligt dan bij koolstof # 4. Het 1,4-product is echter stabieler dan het 1,2-product. Bij lage temperaturen worden de producten irreversibel gevormd en weerspiegelen ze de relatieve snelheid van de twee concurrerende reacties. Dit wordt kinetische controle genoemd. Bij hogere temperaturen wordt het evenwicht tussen de producten tot stand gebracht en domineert het thermodynamisch favoriete 1,4-product.
wanneer een geconjugeerd dieen wordt aangevallen door een elektrofiel, zijn de resulterende producten een mengsel van 1,2 en 1,4 isomeren. Kinetiek en thermodynamica regelen een reactie wanneer er twee producten onder verschillende reactieomstandigheden zijn. Het kinetische product (Product A) zal snel worden gevormd, en het thermodynamische product (Product B) zal langzamer worden gevormd. Gewoonlijk is het eerst gevormde product het stabielere product, maar in dit geval is het tragere product het stabielere product; Product B.
Inleiding
net als niet-geconjugeerde dienenzijn geconjugeerde dienen onderhevig aan aanvallen door elektrofielen. In feite ervaren geconjugeerde elektrofielen relatief grotere kinetische reactiviteit wanneer ze met elektrofielen reageren dan niet-geconjugeerde dienes. Na elektrofiele toevoeging vormt het geconjugeerde dieen een mengsel van twee producten—het kinetische product en het thermodynamische product—waarvan de verhouding wordt bepaald door de reactieomstandigheden. Een reactie die meer thermodynamisch product oplevert, staat onder thermodynamische controle, en ook een reactie die meer kinetisch product oplevert, staat onder kinetische controle.
fundamentele reactie
gedetailleerd mechanisme
conclusie
de reactiviteit van geconjugeerde diënen (koolwaterstoffen die twee dubbele bindingen bevatten) varieert afhankelijk van de locatie van de dubbele bindingen en de temperatuur van de reactie.Deze reacties kunnen zowel thermodynamische als kinetische producten produceren. Geïsoleerde dubbele bindingen geven dienes minder stabiliteit thermodynamisch dan geconjugeerde dienes. Nochtans, zijn zij meer reactief kinetisch in aanwezigheid van elektrofielen en andere reagentia. Dit is een gevolg van Markovnikov toevoeging aan een van de dubbele bindingen. Een carbocatie wordt gevormd na het openen van een dubbele binding. Deze carbocatie heeft twee resonantiestructuren en toevoeging kan optreden bij een van de positieve koolstof.
praktische problemen
- schrijf de producten van 1,2 toevoeging en 1,4-toevoeging van A) HBr en Br. b) DBr tot 1,3-cyclo-hexadieen. Wat is ongewoon aan de producten van 1,2 – en 1,4 – toevoeging van HX aan ongesubstitueerde cyclische 1,3-dienes?
- wordt het 1,2-aanvullend product bij hogere temperaturen sneller gevormd, ook al overheerst het 1,4-aanvullend product onder deze omstandigheden?
- Waarom is het 1,4-additie-product het thermodynamisch stabielere product?
- welke van de volgende radicale kationen is geen redelijke resonantiestructuur?
5. Toevoeging van 1-equivalent Broom aan 2,4-hexadieen bij 0 ° C geeft 4,5-dibroom-2-hexeen plus een isomeer. Welke van de volgende isomeren:
- 5,5-dibroom-2-hexeen
- 2,5-dibroom-3-hexeen
- 2,2-dibroom-3-hexeen
- 2,3-dibroom-4-hexeen
6. Welk van de volgende zal het kinetisch favoriete product van de afgebeelde reactie zijn?
7. Toevoeging van HBr aan 2,3-dimethyl-1,3-cyclohexadieen kan voorkomen in afwezigheid of aanwezigheid van peroxiden. In beide gevallen worden twee isomere c8h13br-producten verkregen. Welk van de volgende is een gemeenschappelijk product van beide reacties?
8. en 9.
8. Het kinetisch gecontroleerde product in de bovenstaande reactie is:
- 3-chloor-1-Buteen
- 1-chloor-2-buteen
9. Voor de reactie in vraag 8, welke is het resultaat van 1,4-optelling?
- 3-chloor-1-Buteen
- 1-chloor-2-buteen
antwoorden op problemen
1. A) hetzelfde product voor beide wijzen van toevoeging.
B) Er zullen zowel cis-als trans-isomeren ontstaan.
toevoeging van de HX aan ongesubstitueerde cycloalka-1,3-dienenop 1,2-of 1,4-wijze geeft hetzelfde product op basis van symmetrie.
2. Bevestigend. het kinetische Product zal zich nog steeds sneller vormen, maar in dit geval zal er genoeg energie zijn om het thermodynamische product te vormen omdat het thermodynamische product nog stabieler is.
3. Het 1,4-product is thermodynamischer stabiel omdat er twee alkylgroepen zijn aan elke kant van de dubbele binding. Deze vorm biedt stabiliteit aan de algemene structuur.
4. Al deze isomeren zijn levensvatbaar.
5. D
6. C
7. D
8. A
9. B
bijdragers
-
William Reussch, emeritus hoogleraar (Michigan State U.), Virtual Textbook of Organic Chemistry
-
Jim Clark (Chemguide.co.uk)
- Natasha Singh