Artikel
John Plante*, Chelsea Eason, Alan Snyder, Dirk Elston
Afdeling Dermatologie en Dermatologische Chirurgie, Medische Universiteit van South Carolina in Charleston, South Carolina
Lichen planopilaris (LPP) is een primaire littekens alopecia gekenmerkt door jeuk, gevoeligheid, folliculaire stekels en rode vlekken in de actieve fase1-3. Hoewel de precieze etiologie onbekend is, impliceert de pathogenese chronische, lymfocyt-gemedieerde ontsteking die uiteindelijk tot onomkeerbare, met littekens bedekken haar verlies door zijn selectieve vernietiging van de haarfollicle1,2 kan leiden. Drie varianten van LPP bestaan en omvatten de klassieke vorm, frontale fibroserende alopecia (FFA), en Graham-Little-Piccardi-lassueur syndroom (progressieve alopecia van de hoofdhuid, oksels, wenkbrauwen, en pubis)2. LPP blijkt vaak ongevoelig voor standaard therapieën en volgt een onvoorspelbare, relapsing cursus, vaak leidend tot een ernstig verminderde kwaliteit van leven1,2,4,5. Hier bespreken we verder onze recente studie over het gebruik van tofacitinib bij de behandeling van recalcitrante LPP6.
talrijke therapieën zijn gebruikt voor de behandeling van LPP met variabel succes1-3,5,7-9. Aangezien momenteel beschikbare behandelingen niet typisch tot haar regrowth leiden, wordt het beheer gericht naar het verminderen van het tarief van haarverlies, het controleren van symptomen,en het verminderen van ontsteking2, 9. Eerstelijnsbehandelingen omvatten intralesional en hoog-potentie actuele corticosteroids, maar deze kunnen in scalp atrophy resulteren en het succes van toekomstige haartransplantatie compromitteren. Andere topische middelen hebben minder risico op atrofie en omvatten de calcineurineremmers tacrolimus en pimecrolimus2. Hoewel het niet het onderliggende ontstekingsproces controleert, kan zowel actuele als mondelinge minoxidil ook worden gebruikt om haarhergroei in patiënten te maximaliseren die ook aan geërfde patroonalopecia lijden-bijna 50% van de bevolking 9, 10. Aanvullende systemische therapieën omvatten hydroxychloroquine, mycofenolaatmofetil, cyclosporine, methotrexaat, thalidomide, doxycycline, retinoïden, pioglitazon, 5-alfa-reductaseremmers en kortdurende prednisolone1,2,9. Recente studies hebben het potentieel van lage-dosis orale naltrexon, bloedplaatjes-rijke plasma injecties, en niet-farmacologische interventies zoals excimer laser gesuggereerd, maar geen zijn uniform effectief geweest 5,7,8. Hoewel haarstukken en extensies volume kunnen verhogen en alopecische gebieden kunnen bedekken, moet voorzichtigheid worden betracht om tractie te vermijden9.
in een recent gepubliceerde studie onderzochten we het potentieel van topische en orale (systemische) formuleringen van tofacitinib6. Tofacitinib is een Janus kinase (JAK) 1/3 inhibitor met werkzaamheid tegen verscheidene immune-gemedieerde dermatologic voorwaarden, met inbegrip van atopic dermatitis, alopecia areata, en vitiligo11-14. Zijn immunomodulerende activiteit wordt gemedieerd door remming van de Jak / STAT signalerende pathway12, 13. Bij LPP werden interferonen betrokken bij het vergemakkelijken van de rekrutering van lymfocyten en het verlies van bobbel epitheliale cel immuunprivilege1. Door de effecten van tofacitinib op de Jak/STAT-route kan deze door interferon gemedieerde ontsteking worden verminderd, waardoor de symptomen worden verbeterd en verdere folliculaire destructie1, 11-13 wordt voorkomen.
we onderzochten het therapeutisch potentieel van tofacitinib bij de behandeling van refractair LPP door middel van een retrospectieve chart review6. Voor zover de auteurs weten, is dit de tweede studie die het gebruik van tofacitinib in LPP-Beheer onderzoekt1. Onze studie omvatte negen patiënten die andere therapie hadden gefaald – drie gebruikte topische, vijf gebruikte orale, en een gebruikte beide formuleringen.
bij alle patiënten, op één na, werd een gunstige initiële respons bereikt. De resterende patiënt reageerde slecht op topische therapie, maar verbeterde met systemische tofacitinib therapie. Hoewel het absolute aantal patiënten klein is, was er een trend naar een betere klinische respons bij systemische patiënten in vergelijking met lokale patiënten. De tijd tot een gunstige respons varieerde van 1 tot 7 maanden, waarbij 5 en 8 patiënten verbetering vertoonden binnen respectievelijk de eerste 3 en 5 maanden van de behandeling.
ons huidige praktijkpatroon is om snel progressieve ziekte te behandelen met een kort verloop van prednison of ciclosporine en dan te proberen over te schakelen naar lokale calcineurineremmertherapie indien mogelijk (figuur 1). Een subgroep van patiënten zal remissie van hun ziekte bereiken met pioglitazon in doses van 15-45 mg per dag. Patiënten moeten worden geïnformeerd over de geëtiketteerde indicatie, gemengde gegevens over de werkzaamheid en een waarschuwing in een box voor blaaskanker bij langdurig gebruik. Het is onze praktijk om pioglitazon niet voort te zetten na maximaal 9 maanden met toenemende doses. Adjuvante middelen omvatten naltrexon in een dosis van 5 mg per dag en N-acetylcysteïne in doses van 600-1200 mg driemaal daags. Excimer laser, hand-held smal-band UVB, of lage intensiteit laser GLB therapie wordt vaak gebruikt als adjuvante therapie in die met een gedeeltelijke reactie. Hydroxychloroquine kan af en toe van nut zijn, maar de meeste van de patiënten die naar onze kliniek worden verwezen hebben al gefaald hydroxychloroquine therapie. Bij patiënten die niet reageren, kan behandeling met methotrexaat, mycofenolaatmofetil of tofacitinib nodig zijn. De resultaten van onze recente studie geven extra steun aan het idee dat zowel topische als systemische tofacitinib levensvatbare adjuvante behandelingsmodaliteiten kunnen zijn in refractaire gevallen. Haaraandoeningen reageren vaak langzaam, en we herevalueren met intervallen van 3 maanden om de respons op therapie en de behoefte aan escalatie te bepalen.
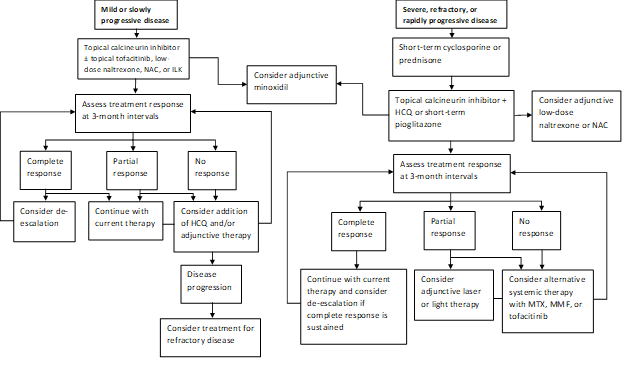
figuur 1: stapsgewijs behandelingsalgoritme voor LPP
NAC, N-acetylcysteïne; ILK, intralesionale corticosteroïden; HCQ, hydroxychloroquine; MTX, methotrexaat, MMF, mycofenolaatmofetil
wanneer het gebruik van tofacitinib in de praktijk wordt overwogen, moeten artsen de voordelen van dit geneesmiddel afwegen tegen de risico ‘ s. Onze cohort ervoer slechts kleine laboratoriumafwijkingen (één op topische en twee op systemische therapie) waarvoor geen interventie nodig was. Providers moeten zich echter bewust zijn van de mogelijke bijwerkingen bij het voorschrijven van dit medicijn, waaronder een verhoogd risico op infectie, cytopenieën, hyperlipidemie, lever-en nierafwijkingen, evenals het potentieel voor trombo-embolische gebeurtenissen14-16. Hoewel de topische formulering lagere plasmaconcentraties heeft laten zien dan de systemische tegenhanger, zijn er nog steeds kleine bijwerkingen en laboratoriumafwijkingen gemeld bij topische therapie13.
hoewel onze resultaten veelbelovend zijn, moeten ze worden geïnterpreteerd na een aantal beperkingen in aanmerking te hebben genomen. We gebruikten een retrospectieve studieopzet en waren niet in staat om een gevalideerde maat voor de ernst van de ziekte te gebruiken, zoals de korstmos Planopilaris Activity Index (lppai)1,3. De LPPAI is geschikt voor prospectieve studies en biedt een gestandaardiseerde tool waarmee providers direct resultaten kunnen vergelijken over verschillende behandelingsmodaliteiten. Tekenen en symptomen zoals erytheem, gevoeligheid, aanwezigheid van folliculaire stekels, en getroffen gebied werden gebruikt om de therapeutische respons te beoordelen, maar toekomstige studies moeten ook een maat voor de kwaliteit van leven omvatten. De mogelijkheid van vooringenomenheid van de waarnemer kan niet worden uitgesloten omdat onze studie werd gedeblokkeerd en niet-gerandomiseerd.
bovendien gebruikte onze gehele cohort tofacitinib als adjuvans, waardoor het moeilijk werd om de onafhankelijke bijdrage van het geneesmiddel te beoordelen. In een eerdere studie bereikte een deel (N=5) van het cohort dat tofacitinib als monotherapie gebruikte, en de meeste proefpersonen gunstige resultaten, maar deze studie werd ook beperkt door de kleine steekproefgrootte en retrospectieve opzet1.
de huidige studies zijn beperkt door hun kleine steekproefomvang en retrospectieve studieontwerpen, en goed ontworpen prospectieve studies zijn hard nodig. Wij adviseren een stapsgewijze benadering van de therapie om het risico op bijwerkingen te minimaliseren. Het risico op permanente littekenvorming moet worden afgewogen tegen het risico op ernstige bijwerkingen in het licht van individuele patiëntfactoren en comorbiditeiten, en patiënten moeten actieve partners zijn in de besluitvorming. Haartransplantatie kan worden overwogen zodra de ziekte onder controle is en de ontsteking is afgenomen. Het is belangrijk op te merken dat agressieve therapie zoals prednison of cyclosporine meestal nodig is tijdens de weken na transplantatie om opflakkeringen van de ziekte te voorkomen. Geleidelijke uitputting van getransplanteerde haren is te verwachten, zelfs na succesvolle transplantatie, maar gegevens suggereren patiënten zijn over het algemeen tevreden met de resultaten en vinden dat transplantatie verbetert de kwaliteit van leven.
Afkortingen
LPP, lichen Planopilaris; FFA, frontale fibroserende alopecia; JAK, Janus kinase; STAT, signal transducer and activator of transcription proteins; LPPAI, Lichen Planopilaris Activity Index.
belangenconflicten
de auteurs verklaren geen belangenconflicten.
- Yang CC, Khanna T, Sallee B, et al. Tofacitinib voor de behandeling van lichen planopilaris: een casusreeks. Dermatol Ther. 2018; 31 (6): e12656. doi: 10.1111 / dth.12656
- Babahosseini H, Tavakolpour S, Mahmoudi H, et al. Lichen planopilaris: retrospectieve studie naar de kenmerken en behandeling van 291 patiënten. J Dermatolog Treat. 2019; 30(6): 598–604. doi:10.1080/09546634.2018.1542480
- Chiang C, Sah D, Cho BK, et al. Hydroxychloroquine and lichen planopilaris: efficacy and introduction of Lichen Planopilaris Activity Index scoring system. J Am Acad Dermatol. 2010; 62(3): 387-392. doi: 10.1016 / j. jaad.2009.08.054
- Alirezaei P, Ahmadpanah M, Rezanejad A, et al. In vergelijking met controles, individuen met korstmos Planopilaris hebben meer Depressie, een lager gevoel van eigenwaarde, en een lagere kwaliteit van leven. Neuropsychobiologie. 2019; 78(2): 95-103. doi:10.1159/000499135
- Jha AK. Bloedplaatjes-rijk plasma als een adjuvante behandeling in lichen planopilaris. J Am Acad Dermatol. 2019; 80 (5): e109-e110. doi: 10.1016 / j. jaad.2018.09.013
- Plante J, Eason C, Snyder A, et al. Tofacitinib in the treatment of lichen planopilaris: a retrospective review . J Am Acad Dermatol. 2020; S0190-9622(20)30979-8. doi:10.1016 / j.jaad.2020.05.104
- Lajevardi V, Salarvand F, Ghiasi M, et al. De werkzaamheid en veiligheid van orale lage dosis naltrexon versus placebo bij patiënten met lichen planopilaris: een gerandomiseerd gecontroleerd klinisch onderzoek . J Dermatolog Treat. 2020; 1-5. doi:10.1080/09546634.2020.1774488
- Lee B, Elston DM. Het gebruik van naltrexon in dermatologische aandoeningen. J Am Acad Dermatol. 2019; 80(6): 1746-1752. doi: 10.1016 / j. jaad.2018.12.031
- Bolduc C, Sperling LC, Shapiro J. primaire cicatriciale alopecia: Lymfocytaire primaire cicatriciale alopecia ‘ s, waaronder chronische cutane lupus erythematosus, lichen planopilaris, frontale fibroserende alopecia, en Graham-Little syndroom. J Am Acad Dermatol. 2016; 75(6): 1081-1099.
- Vano-Galvan S, Trindade de Carvalho L, Saceda-Corralo D, et al. Mondelinge minoxidil verbetert de dikte van het achtergrondhaar in korstmos planopilaris . J Am Acad Dermatol. 2020; S0190-9622 (20)30566-1. doi: 10.1016 / j. jaad.2020.04.026
- Tegtmeyer K, Zhao J, Maloney NJ, et al. Off-label studies over tofacitinib in dermatologie: een overzicht . J Dermatolog Treat. 2019; 1–11. doi: 10.1080/09546634.2019.1673877
- Montilla AM, Gomez-Garcia F, Gomez-Arias PJ, et al. Scoping beoordeling op het gebruik van Drugs gericht Jak / STAT Pathway in atopische Dermatitis, Vitiligo, en alopecia Areata. Dermatol Ther (Heidelb). 2019; 9(4): 655–683. doi: 10.1007 / s13555-019-00329-y
- Hosking AM, Juhasz M, Mesinkovska NA. Actuele Janus kinase inhibitors: een overzicht van toepassingen in dermatologie. J Am Acad Dermatol. 2018; 79(3): 535–544. doi: 10.1016 / j. jaad.2018.04.018
- Shreberk-Hassidim R, Ramot Y, Zlotogorski A. Janus kinase inhibitors in dermatology: a systematic review. J Am Acad Dermatol. 2017; 76(4): 745-753.e19. doi: 10.1016 / j. jaad.2016.12.004
- Xeljanz / Xeljanz XR (tofacitinib) . New York, NY: Pfizer Laboratories Division of Pfizer Inc. https://labeling.pfizer.com/showlabeling.aspx?id=959; 2019. Geopend Op 7 Juli 2020.
- FDA. De veiligheidsstudie vindt risico van bloedstolsels in de longen en dood met hogere dosis tofacitinib (Xeljanz, Xeljanz XR) bij patiënten van reumatoïde artritis; FDA te onderzoeken. https://www.fda.gov/drugs/drug-safety-and-availability/safety-trial-finds-risk-blood-clots-lungs-and-death-higher-dose-tofacitinib-xeljanz-xeljanz-xr; 2019. Geopend Op 6 Juli 2020.