ATrain Education
hoewel we elke dag meer leren over de pathofysiologie van de ziekte van Parkinson, wordt het nog steeds beschouwd als grotendeels idiopathisch (met onbekende oorzaak). Het impliceert waarschijnlijk de interactie van gastheergevoeligheid en omgevingsfactoren. Een klein percentage van de gevallen is genetisch gekoppeld en genetische factoren worden intensief bestudeerd.Fysiologisch gezien zijn de symptomen geassocieerd met de ziekte van Parkinson het gevolg van het verlies van een aantal neurotransmitters, met name dopamine. Symptomen verergeren na verloop van tijd als meer en meer van de cellen getroffen door de ziekte verloren gaan. Het verloop van de ziekte is zeer variabel, met sommige patiënten vertonen zeer weinig symptomen als ze ouder worden en anderen waarvan de symptomen snel vorderen.Parkinson wordt in toenemende mate gezien als een complexe neurodegeneratieve ziekte met een opeenvolging van progressie. Er is sterk bewijs dat het eerst van invloed op de dorsale motorische kern van de nervus vagus en de olfactorische bollen en kern, dan de locus coeruleus, en uiteindelijk de substantia nigra. Corticale gebieden van de hersenen worden beïnvloed in een later stadium. Schade aan deze verschillende neuronale systemen zijn verantwoordelijk voor de veelzijdige pathofysiologische veranderingen die niet alleen het motorische systeem, maar ook de cognitieve en neuropsychologische systemen aantasten (Kwan & Whitehill, 2011).De rol van Dopamine
Dopamine zendt, net als andere neurotransmitters, chemische berichten van de ene zenuwcel naar de andere over de synaps, een ruimte tussen de presynaptische cel en de postsynaptische receptor. Dopamine wordt uitgescheiden in de synaps vanuit membraanopslagblaasjes in het presynaptische membraan. Het passeert de synaps en bindt zich aan het postsynaptische membraan, waar het dopaminereceptoren activeert. Ongebruikte dopamine die in de synapse achterblijft, wordt terug geabsorbeerd in de presynapse cel; eenmaal terug in de presynapse cel wordt de overtollige dopamine opnieuw verpakt in opslagblaasjes en weer vrijgegeven in de synapse.Wanneer dopamine van de ene cel naar de andere reist, kan het binnen de synaps worden afgebroken en inactief worden gemaakt door twee enzymen, MAO (monoamine-oxidase) en COMT (catechol-o-methyltransferase). Eén therapeutische strategie introduceert een MAO-remmer in de synaps, die de werking van het Mao-enzym onderbreekt en de afbraak van dopamine voorkomt. Dit laat meer dopamine toe om in de synaps te blijven en verhoogt de waarschijnlijkheid dat het aan het postsynaptic membraan zal binden.
chemische synaptische transmissie
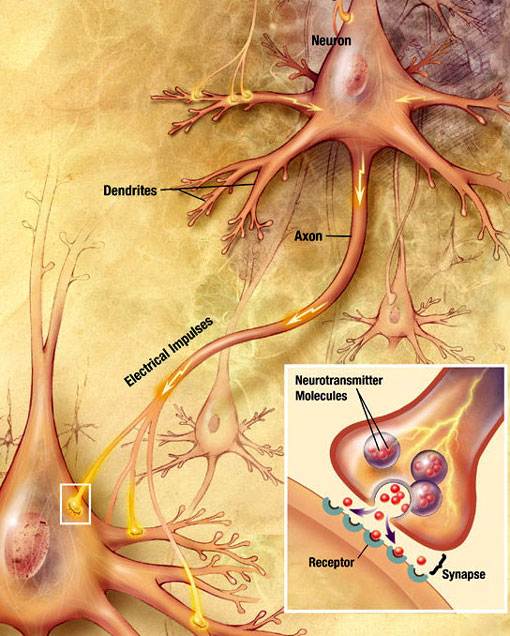
een elektrochemische golf, een actiepotentiaal genaamd, reist langs het axon van een neuron. Wanneer het actiepotentieel de presynaptische terminal bereikt, veroorzaakt het de afgifte van een kleine hoeveelheid neurotransmittermoleculen, die aan chemische receptormoleculen in het membraan van het postsynaptische neuron, aan de andere kant van de synaptische gespleten binden. Bron: Wikimedia Commons.
progressief verlies van Dopamine
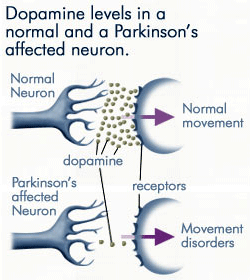
omdat steeds minder dopamine wordt aangemaakt door de neuronen met de ziekte van Parkinson, is er veel minder dopamine beschikbaar om zich te binden aan de dopaminereceptoren op het postsynaptische membraan. Bron: anti-agingfirewalls.com.
hoewel het verlies van dopamine-cellen niet direct kan worden gemeten, blijkt uit metingen bij neurologisch normale mensen en bij niet-menselijke primaten een langzaam progressief verlies van dopamine met de leeftijd. Bij de ziekte van Parkinson komt het verlies aan een veel groter tarief voor en zowel biochemische maatregelen als beeldvormingsstudies suggereren dat er een significante afname van dopamine is tegen de tijd dat motorische symptomen verschijnen. In deze visie is de ziekte van Parkinson een versnelde versie van de celdood die wordt gezien bij normale veroudering (Cookson, 2009). Dit wordt geïllustreerd in de grafiek hieronder, die de daling van dopaminerge neuronen tijdens het normale verouderen toont, in idiopathische PD, in PD door milieu of genetische factoren wordt veroorzaakt, en in vroeg-begin PD.
ontwikkeling van dopaminerge neuronen bij de ziekte van Parkinson
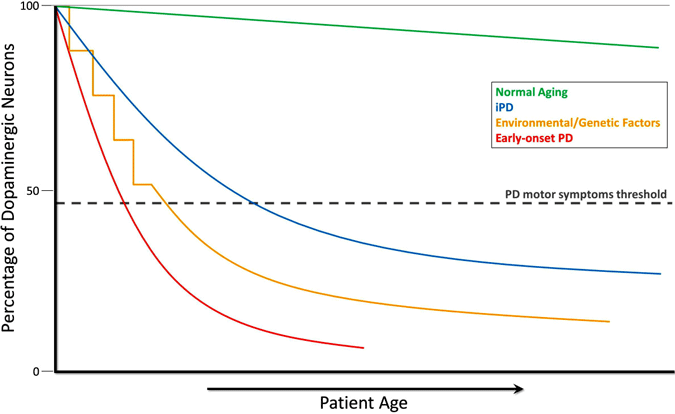
tijdens normale veroudering (groene lijn) treedt een kleine maar langzame dopaminerge degeneratie op zonder motorische symptomen. Idiopathische PD (IPD, blauwe lijn) is van onbekende oorsprong, maar wordt verondersteld zich geleidelijk te ontwikkelen, met een langzame degeneratie van dopaminerge neuronen die tot de klassieke PD motorische symptomen later in het leven leiden. Een ander model van dopamine neurodegeneratie leidt tot PD motor symptomen impliceert herhaalde blootstelling aan milieu toxicanten na verloop van tijd in combinatie met een genetische aanleg voor dopaminerge neuron verlies (gele lijn). Vroeg-begin PD (rode lijn), Zoals veroorzaakt door mutaties in het Parkin-gen, impliceert een steile daling van dopaminerge neuronen, en de motorsymptomen van PD kunnen decennia voorafgaand aan die in idiopathische PD voorstellen. Nog een scenario (niet getoond) van PD motorische symptoomontwikkeling impliceert mogelijke In utero omgevingstoxicanten of genetische factoren die leiden tot een atypisch laag aantal dopaminerge neuronen bij de geboorte en verhoogde gevoeligheid voor PD ontwikkeling (Haas et al., 2012).
degeneratie van dopamine neuronen is bijzonder duidelijk in een deel van de substantia nigra, de pars compacta genaamd. Significant, het verlies van dopamine in de pars compacta verhoogt de algehele prikkelende aandrijving in de basale ganglia, * het verstoren van vrijwillige motorische controle en het veroorzaken van de karakteristieke symptomen van PD. Normalisatie van de motorische functie wordt in eerste instantie gezien bij behandeling met levodopa (Gasparini et al., 2013).*De hoofdbestanddelen van de basale ganglia zijn het striatum (caudate nucleus en putamen), de globus pallidus, de substantia nigra, de nucleus accumbens en de subthalamic nucleus.
naarmate de ernst van de PD toeneemt, leidt de dopamine-depletie tot verdere veranderingen in de basale ganglia-routes, waaronder een veranderde functie van andere basale ganglia-neurotransmitters zoals glutamaat, GABA en serotonine (Gasparini et al., 2013). Hoewel er een relatieve kwetsbaarheid is van dopamine-producerende neuronen in de substantia nigra, worden niet alle dopamine-cellen aangetast bij de ziekte van Parkinson; in sommige delen van de hersenen worden de dopamine-producerende neuronen relatief gespaard (Cookson, 2009).
de Nigrostriatale route
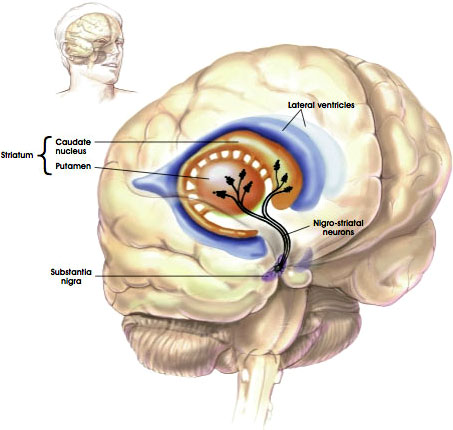
bron: NIH, n. d.
Lewy-lichamen en alfa-synucleïne
Lewy-lichamen zijn abnormale aggregaten en insluitsels van eiwitten die zich ontwikkelen in zenuwcellen bij mensen met de ziekte van Parkinson. De aggregaties bestaan gewoonlijk uit onoplosbare fibrillaire aggregaten die misfolded proteã nen bevatten. Een groot aantal molecules zijn geà dentificeerd in Lewy-organismen maar een proteã ne genoemd alpha-synucleã ne is de belangrijkste component.
Lewy-lichamen(alfa-synucleïne-insluitsels)
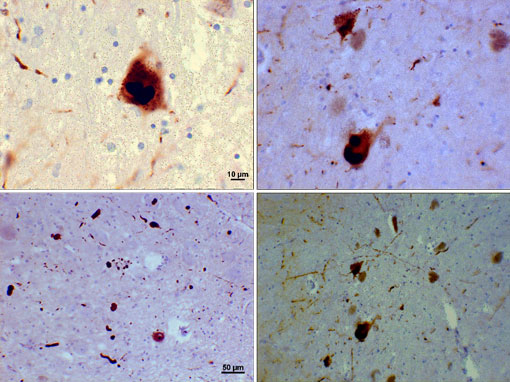
Fotomicrografie van gebieden van substantia nigra bij een Parkinson-patiënt met Lewy-lichamen en Lewy-neurieten in verschillende vergrotingen. De bovenste panelen tonen een 60x vergroting van de alfa-synucleïne intraneuronale insluitingen die worden samengevoegd tot Lewy-lichamen. De onderste panelen zijn 20 × vergrotingsbeelden die strengenachtige Lewy neurieten en afgeronde Lewy lichamen van verschillende grootte laten zien. Afbeeldingen met dank aan Suraj Rajan.Lewy pathologie omvat vele gebieden van de hersenen en sommige rapporten suggereren dat de substantia nigra niet de eerste plaats is waar Lewy-lichamen ontstaan bij de ziekte van Parkinson. Insluitsels en aggregaten symboliseren waarschijnlijk het eindstadium van een cascade van ingewikkelde gebeurtenissen. Een eerder stadium kan directer aan de pathogenese van de wanorde dan de insluitsels zelf worden gebonden, die al dan niet kenmerkende stempels kunnen vertegenwoordigen.Lewy-lichamen worden ook gezien bij “dementie met Lewy-lichamen”, wat suggereert dat deze aandoeningen aan elkaar gerelateerd zijn door gedeelde pathologie en mogelijk door gedeelde etiologie. Noch celverlies noch de vorming van Lewy-lichamen is absoluut specifiek voor PD, maar beide zijn vereist voor een diagnose van PD onder de huidige definities (Cookson, 2009).
neurodegeneratieve aandoeningen zoals de ziekte van Alzheimer, frontale temporale degeneratie, prionziekte, Huntingtons chorea en motoneuronziekten worden in toenemende mate erkend als gemeenschappelijke cellulaire en moleculaire mechanismen, waaronder eiwitaggregatie en inclusie-lichaamsvorming in bepaalde gebieden van het zenuwstelsel (Jellinger, 2011).
ontsteking en immuunrespons
de trekker van dopaminerge degeneratie lijkt multifactorieel beïnvloed te zijn door zowel endogene als omgevingselementen. Ontstekingen en immuunreacties worden steeds meer beschouwd als belangrijke mediatoren van dopaminerge degeneratie. Grote populatiestudies hebben gesuggereerd dat individuen die niet-steroïde anti-inflammatoire geneesmiddelen (NSAID ‘ s) hebben minder risico op het ontwikkelen van idiopathische PD, wat suggereert dat anti-inflammatoire geneesmiddelen een veelbelovende ziekte-modificerende behandeling voor parkinsonpatiënten kan zijn (Barcia, 2013).
nieuwe onderzoeksfasen betroffen ontstekingsremmende behandelingen-specifiek op zoek naar een objectieve biomarker in behandelingen gericht op het verminderen van inflammatoire veranderingen bij patiënten met PD. De onderzoekers gebruiken neuroimaging hulpmiddelen om een relevante biomarker met de intentie te ontwikkelen om dit in grote klinische weergavestudies te testen. Het resultaat van deze studies zal gegevens leveren om de progressie van anti-inflammatoire behandelingen voor PD te testen en te monitoren en zal helpen om het tijdig therapeutisch venster te identificeren om te stoppen, of op zijn minst langzaam, inflammatoire-gemedieerde dopaminerge degeneratie (Barcia, 2013).Parkinsonisme
Parkinsonisme
Parkinsonisme, ook bekend als” atypische Parkinson”,” secundair Parkinson “of” syndroom van Parkinson”, is een neurologisch syndroom waarbij een patiënt enkele van de symptomen vertoont die geassocieerd worden met de ziekte van Parkinson—tremor, rigiditeit, bradykinesie en posturale instabiliteit. Maar parkinsonisme is niet de ziekte van Parkinson. Parkinsonisme wordt niet verondersteld te worden veroorzaakt door de ziekte van Parkinson en patiënten reageren meestal slecht op farmacologische interventie. Parkinsonisme heeft vaak een identificeerbare oorzaak, zoals blootstelling aan toxines, methamfetamine, trauma, meerdere beroertes, andere aandoeningen van het zenuwstelsel, of ziekte. Over het algemeen worden Lewy-lichamen niet gezien in parkinsonisme.De term parkinsonisme wordt ook geassocieerd met aandoeningen zoals progressieve supranucleaire verlamming, atrofie van meerdere systemen, Lewy body dementie, corticobasale degeneratie, vasculair parkinsonisme, geneesmiddelgeïnduceerd parkinsonisme en parkinsonisme secundair aan infectie en andere oorzaken (Hohler et al ., 2012). Een vorm van reversibel parkinsonisme kan optreden door het gebruik van bepaalde neuroleptica, met name reserpine, antipsychotica (haloperidol) en metoclopramide. Blootstelling aan bepaalde toxines, ernstige koolmonoxide vergiftiging, en kwikvergiftiging kan ook leiden tot parkinsonisme.
het optreden in het begin van de jaren tachtig van parkinsonismesymptomen bij een groep drugsverslaafden die een besmette partij van een synthetisch opiaat hadden geconsumeerd, leidde tot de ontdekking van het chemische MPTP als een agens dat parkinsonismesyndroom veroorzaakt bij zowel niet-menselijke primaten als bij mensen. MPTP kan worden geproduceerd bij het maken van een vorm van heroïne (MPTP wordt omgezet in een neurotoxine dat selectief dopamine cellen vernietigt in de substantia nigra). Deze gevallen zijn zeldzaam en hebben vooral langdurige drugsgebruikers getroffen.Methamfetaminemisbruik is ook in verband gebracht met parkinsonisme. Bij proefdieren beschadigt blootstelling aan methamfetamine dopaminerge vezels in het striatum* en de cellichamen in de substantia nigra, wat de degeneratie weergeeft die is waargenomen bij patiënten met PD bij mensen. Selectieve schade aan dopaminerge terminals in het striatum is ook waargenomen bij gebruikers van menselijke methamfetamine, hoewel er tot nu toe geen bewijs is dat misbruik van methamfetamine de dopaminerge cellichamen in de substantia nigra beschadigt (Granado et al., 2013).
* de grootste kern van de basale ganglia, het striatum bestaat uit de caudate nucleus en het putamen.Er wordt verondersteld dat het gebruik van methamfetamine gebruikers kan predisponeren voor de toekomstige ontwikkeling van PD. Deze hypothese wordt ondersteund door recent epidemiologisch onderzoek dat erop wijst dat methamfetaminegebruikers een verhoogd risico hebben op het ontwikkelen van PD. Dit komt overeen met de aanhoudende neurotoxische effecten van methamfetamine bij proefdieren (Granado et al., 2013).Patiënten met parkinsonisme zijn vaak moeilijk te behandelen als poliklinische patiënten. De complexiteit van hun symptomen, de toegevoegde cognitieve en autonome tekorten, de slechte reactie op de meeste PD medicijnen, en de relatief snelle daling van de status bijdragen aan de uitdagingen in het beheer van deze patiënten, vooral als de ziekte vordert (Hohler et al., 2012).