spinale spieratrofie
oorzaken/overerving
wat veroorzaakt spinale spieratrofie (SMA)?
SMA wordt gekenmerkt door het verlies van motorische neuronen, zenuwcellen in het ruggenmerg. Het is geclassificeerd als een motor neuron ziekte.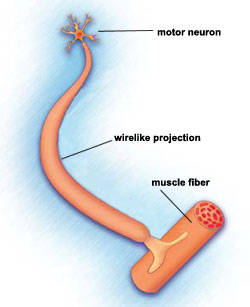
Wat zijn de genetische oorzaken van SMA?
de meest voorkomende vorm van SMA (type 1-4) wordt veroorzaakt door een defect (mutatie) in het SMN1-gen op chromosoom 5. (Mensen hebben twee SMN1 genen — een op elk chromosoom 5). In 94% van alle SMA-gevallen gaat deze mutatie gepaard met een deletie in een segment dat exon 7 wordt genoemd. Dit gebied bevindt zich in de lange arm van chromosoom 5, in het 5q13.2 Gebied (chromosomen hebben twee “armen”: een korte, geïdentificeerd door de letter “p,” en een lange, geïdentificeerd door de letter “q”).
een mutatie in het SMN1-gen leidt tot een deficiëntie van het motorneuron-eiwit SMN, wat staat voor “survival of motorneuron”.”Zoals de naam al aangeeft, is dit eiwit verantwoordelijk voor genexpressie die nodig is voor de normale motorneuronfunctie.
in zeldzame gevallen veroorzaakt een mutatie in een X-chromosoomgen genaamd UBE1 X-gebonden SMA. Het UBE1 gen draagt instructies voor ubiquitin-activerend enzym 1, dat normaal helpt een moleculaire markering aan proteã nen vast te maken om hen voor vernietiging te merken.
fouten in het cytoplasmatische dynein 1 heavy chain 1 (DYNC1H1) gen op chromosoom 14 hebben geleid tot een andere zeldzame vorm van SMA genaamd SMA-LED.
Wat is de oorzaak van de grote variatie in ernst van de symptomen bij SMA?
normaal produceren SMN1-genen volledig functionele SMN-eiwitten. Maar wanneer het SMN1-gen mutaties heeft, zoals in de chromosoom 5-gerelateerde vorm van SMA, worden onvoldoende niveaus van SMN-eiwit geproduceerd.
een naburig gen op chromosoom 5, genaamd SMN2, produceert ook SMN-eiwit. Het grootste deel van de proteã ne gemaakt van instructies gedragen door SMN2 genen is niet functioneel, maar een klein percentage, rond 10 tot 15% is functioneel.
mensen kunnen meerdere kopieën van het SMN2-gen hebben. Normaal varieert het aantal exemplaren tussen nul en acht. In de chromosoom 5-verwante vorm van SMA, meer SMN2 genkopieën een persoon heeft, is de meer functionele SMN proteã ne beschikbaar. Als gevolg daarvan, hoe milder de ziekte verloop is waarschijnlijk. Het hebben van drie of meer exemplaren van het gen SMN2 wordt geassocieerd met een minder strenge ziektemanifestatie.
genetische tests kunnen vertellen hoeveel SMN2-genen een persoon heeft en ruwweg het verloop van SMA voorspellen dat waarschijnlijk zal resulteren.
de ernst van SMA kan ook afhangen van ziektemodificatoren, die geen ziekte veroorzaken, maar het begin en de ernst kunnen beïnvloeden (wijzigen) door verschillende biologische routes te beïnvloeden. Niveaus van zowel plastin 3-eiwit als ZPR1-eiwit zijn geïdentificeerd als modifiers van SMN-gerelateerde SMA en kunnen therapeutische doelwitten worden. Bovendien kan het testen van deze eiwitniveaus helpen om de ernst van de ziekte te voorspellen, en het inzicht in de activiteiten van deze eiwitten kan nieuw licht werpen op ziekteprocessen.

de genetische informatie beweegt van zijn opslagvorm als DNA aan een reeks Die instructies als RNA wordt bekend, waaruit eiwitmolecules worden gemaakt. De meeste instructies van RNA van het gen SMN1 vertellen de cel om volledige SMN-proteã ne te maken. De meeste instructies van het SMN2 gen vertellen de cel om korte SMN proteã ne te maken.
Wat is het overervingspatroon van SMA?
chromosoom 5-gerelateerde SMA (type 1 tot en met 4) volgt een overervingspatroon dat autosomaal recessief wordt genoemd. (De autosomen zijn de genummerde chromosomen-dat wil zeggen alle chromosomen behalve de x en de Y, die het geslacht bepalen.)
recessieve ziekten vereisen twee genfouten — meestal één van elke ouder, maar soms één van één ouder en één die optreedt als een foetus wordt gevormd. De mensen die slechts één genfout voor een recessieve ziekte hebben worden gezegd dragers te zijn en vertonen gewoonlijk geen symptomen. Vaak heeft een familie geen idee dat sommige leden dragers zijn totdat een kind wordt geboren met een recessieve aandoening.
als beide ouders dragers zijn van de chromosoom 5 genfout, is het risico dat elke zwangerschap een kind met de ziekte voortbrengt 25%. Dit risico verandert niet, hoeveel kinderen een stel ook heeft.
genetische tests op chromosoom 5-gerelateerde SMA zijn beschikbaar voor degenen die ervan worden verdacht de ziekte te hebben, met inbegrip van ongeboren baby ‘ s, en voor dragers van de ziekte. Genetische tests breiden zich uit en veranderen snel, maar de implicaties ervan kunnen complex zijn. Het is het beste om te praten met een genetische counselor voordat u begint met testen. (Een erfelijkheidsadvies verwijzing kan worden verkregen via uw MDA Care Center of uw huisarts).
het is noodzakelijk om SMA zo vroeg mogelijk te diagnosticeren, idealiter vóór het optreden van de symptomen, omdat vertraging in de behandeling het verloop van de ziekte kan verergeren en permanente schade aan motorische neuronen kan veroorzaken. De beste manier om SMA te identificeren voordat de symptomen verschijnen is om alle pasgeborenen te screenen voor de SMN1 exon 7 verwijdering. Aangezien Spinraza (nusinersen), een ziekte-modificerende therapie, werd goedgekeurd in 2016 door de Amerikaanse Food and Drug Administration (FDA) en vroege behandeling positieve resultaten toonde, keurde de secretaris van het Amerikaanse Ministerie van Volksgezondheid de toevoeging van SMA aan pasgeboren screeningpanels goed.Zie voor meer informatie de hyperlink ” https://strongly.mda.org/sma-added-national-list-disorders-to-screen-for…”SMA toegevoegd aan de nationale lijst van aandoeningen om op te screenen bij de geboorte.
X-gebonden SMA wordt geërfd via het X-chromosoom. De wijfjes hebben twee chromosomen van X, en die met een genfout op één chromosoom van X worden gewoonlijk beschouwd dragers van een X-verbonden ziekte. Mannetjes hebben echter geen tweede X om hen te beschermen tegen de volledige effecten van een genfout op het X-chromosoom en tonen de volledige effecten van een dergelijke fout.
bovendien kan SMA worden veroorzaakt door mutaties in het DYNC1H1 gen op chromosoom 14. Deze vorm wordt dominant geërfd, wat betekent dat slechts één DYNC1H1 genmutatie, geërfd van één ouder, voldoende is om de ziekte te veroorzaken.
om meer te lezen over de genetica van SMA en genetische tests voor deze ziekte, zie ook:
- MDA genetische Counseling webinar beantwoordt belangrijke vragen, Quest News Online, Feb. 28, 2012
- Facts About Genetics and Neuromuscular Diseases, MDA, December 2009
- The Genie ‘ S Out of the Bottle: Genetic testing in the 21st century, Quest Magazine (MDA), November 2008
- the Pain and Promise of Prenatal and Newborn Genetic Diagnostic, Quest Magazine (MDA), juli 2007