rdzeniowy zanik mięśni
przyczyny/dziedziczenie
co powoduje rdzeniowy zanik mięśni (SMA)?
SMA charakteryzuje się utratą neuronów ruchowych, komórek nerwowych w rdzeniu kręgowym. Jest klasyfikowany jako choroba neuronu ruchowego.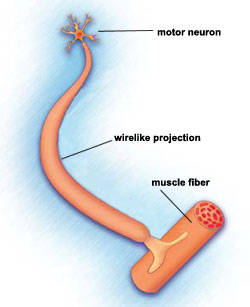
jakie są genetyczne przyczyny SMA?
najczęstszą formą SMA (typy 1-4) jest spowodowana defektem (mutacją) w genie SMN1 na chromosomie 5. (Ludzie mają dwa geny SMN1 — po jednym na każdym chromosomie 5). W 94% wszystkich przypadków SMA mutacja ta wiąże się z delecją w segmencie znanym jako ekson 7. Obszar ten znajduje się w długim ramieniu chromosomu 5, w regionie 5q13.2 (chromosomy mają dwa „ramiona”: krótkie, identyfikowane literą „p” i długie, identyfikowane literą „q”).
mutacja w genie SMN1 prowadzi do niedoboru białka neuronu ruchowego zwanego SMN, co oznacza ” przetrwanie neuronu ruchowego.”Jak sama nazwa wskazuje, białko to jest odpowiedzialne za ekspresję genów niezbędną do prawidłowego funkcjonowania neuronu ruchowego.
rzadziej mutacja w genie chromosomu X o nazwie UBE1 powoduje X-linked SMA. Gen UBE1 zawiera instrukcje dla enzymu aktywującego ubikwitynę 1, który zwykle pomaga przyczepić znacznik molekularny do białek, aby oznaczyć je do zniszczenia.
wady cytoplazmatycznego genu łańcucha ciężkiego dynein 1 (DYNC1H1) na chromosomie 14 doprowadziły do innej rzadkiej formy SMA zwanej SMA-LED.
co powoduje szerokie zróżnicowanie nasilenia objawów obserwowane w SMA?
normalnie geny SMN1 wytwarzają pełnowymiarowe i w pełni funkcjonalne białko SMN. Ale gdy gen SMN1 ma mutacje, jak w postaci SMA związanej z chromosomem 5, powstają niewystarczające poziomy białka SMN.
sąsiedni gen na chromosomie 5, zwany SMN2, również wytwarza białko SMN. Większość białka wytworzonego z instrukcji przekazywanych przez geny SMN2 nie jest funkcjonalna, ale niewielki odsetek, około 10 do 15% jest funkcjonalny.
ludzie mogą mieć wiele kopii genu SMN2. Zwykle liczba ta waha się od zera do ośmiu egzemplarzy. W postaci SMA związanej z chromosomem 5, im więcej kopii genu SMN2 osoba ma, tym bardziej funkcjonalne białko SMN jest dostępne. W rezultacie, łagodniejszy przebieg choroby może być. Posiadanie trzech lub więcej kopii genu SMN2 wiąże się z mniej ciężką manifestacją choroby.
testy genetyczne mogą określić, ile genów SMN2 ma dana osoba i z grubsza przewidzieć przebieg SMA, który prawdopodobnie spowoduje.
nasilenie SMA może również zależeć od modyfikatorów choroby, które nie powodują choroby, ale mogą wpływać na (modyfikować) początek i nasilenie poprzez wpływanie na różne szlaki biologiczne. Poziomy zarówno białka plastin 3, jak i białka ZPR1 zostały zidentyfikowane jako modyfikatory SMA związanego z SMN i mogą stać się celami terapeutycznymi. Ponadto, testowanie tych poziomów białka może pomóc przewidzieć nasilenie choroby, a wgląd w aktywność tych białek może rzucić nowe światło na procesy chorobowe.

informacja genetyczna przenosi się z formy przechowywania jako DNA do zestawu instrukcji znanych jako RNA, z którego wytwarzane są cząsteczki białka. Większość instrukcji RNA z genu SMN1 mówi komórce, aby produkowała pełnowymiarowe białko SMN. Większość instrukcji z genu SMN2 mówi komórce, aby produkować krótkie białko SMN.
jaki jest wzór dziedziczenia SMA?
SMA związane z chromosomem 5 (typy od 1 do 4) podąża za wzorcem dziedziczenia znanym jako autosomalny recesywny. (Autosomy są numerowanymi chromosomami-to znaczy wszystkimi chromosomami z wyjątkiem X i Y, które określają płeć.)
choroby recesywne wymagają dwóch wad genów — zwykle po jednej od każdego rodzica, ale czasami po jednej od jednego rodzica i jednej, która występuje w miarę formowania się płodu. Ludzie, którzy mają tylko jedną wadę genu dla choroby recesywnej, są nosicielami i zwykle nie wykazują żadnych objawów. Często rodzina nie ma pojęcia, że niektórzy członkowie są nosicielami, dopóki dziecko nie urodzi się z zaburzeniem recesywnym.
jeśli oboje rodzice są nosicielami wady genu chromosomu 5, ryzyko każdej ciąży rodzi dziecko z chorobą wynosi 25%. To ryzyko nie zmienia się bez względu na to, ile dzieci ma Para.
dostępne są badania genetyczne na obecność SMA związanego z chromosomem 5 dla osób podejrzewanych o chorobę, w tym nienarodzonych dzieci, oraz dla nosicieli choroby. Badania genetyczne szybko się rozwijają i zmieniają, ale ich implikacje mogą być złożone. Najlepiej porozmawiać z doradcą genetycznym przed rozpoczęciem badań. (Skierowanie do poradnictwa genetycznego można uzyskać za pośrednictwem Centrum Opieki MDA lub lekarza podstawowej opieki zdrowotnej).
konieczne jest zdiagnozowanie SMA tak wcześnie, jak to możliwe, najlepiej przed wystąpieniem objawów, ponieważ opóźnienie w leczeniu może pogorszyć przebieg choroby i spowodować trwałe uszkodzenie neuronów ruchowych. Najlepszym sposobem identyfikacji SMA przed pojawieniem się objawów jest sprawdzenie wszystkich noworodków pod kątem usunięcia z eksonu 7 SMN1. Ponieważ Spinraza (Nusinersen), terapia modyfikująca przebieg choroby, została zatwierdzona w 2016 r.przez Amerykańską Agencję Żywności i Leków (FDA), a wczesne leczenie wykazało pozytywne wyniki, Sekretarz Departamentu Zdrowia USA zatwierdził dodanie SMA do paneli przesiewowych noworodków.1 Aby uzyskać więcej informacji, odwiedź hiperłącze ” https://strongly.mda.org/sma-added-national-list-disorders-to-screen-for…”SMA dodane do Krajowej listy zaburzeń do ekranu przy urodzeniu.
X-linked SMA jest dziedziczona przez chromosom X. Kobiety mają dwa chromosomy X, a te z wadą genu na jednym chromosomie X są zwykle uważane za nosicieli choroby X-linked. Mężczyźni jednak nie mają drugiego X, aby chronić je przed pełnym wpływem wady genu na chromosom X i pokazać pełne skutki takiej wady.
dodatkowo, SMA może być spowodowane mutacjami w genie DYNC1H1 na chromosomie 14. Ta forma jest dominująco dziedziczona, co oznacza, że tylko jedna mutacja genu DYNC1H1, dziedziczona od jednego rodzica, jest wystarczająca do wywołania choroby.
aby przeczytać więcej o genetyce SMA i badaniach genetycznych tej choroby, zobacz również:
- MDA poradnictwo genetyczne Webinar odpowiedzi na kluczowe pytania, Quest News Online, luty. 28, 2012
- fakty o genetyce i chorobach nerwowo-mięśniowych, MDA, grudzień 2009
- The Genie ’ s Out of the Bottle: Genetic testing in the 21st century, Quest Magazine (MDA), listopad 2008
- the Pain and Promise of Prenatal and Newborn Genetic Diagnosis, Quest Magazine (MDA), lipiec 2007