16.10: adição eletrofílica: 1,2-Versus 1,4-adição
as reações de adição de dienos isolados procedem mais ou menos como esperado do comportamento de alcenos simples. Assim, se um molar equivalente a 1,5-hexadiene é tratada com um equivalente de bromo uma mistura de 5,6-dibromo-1-hexeno, 1,2,5,6-tetrabromohexane e não reagiu dieno é obtido, com o dibromo composto a ser o produto principal (cerca de 50%)
fig
reações Semelhantes de dienos conjugados, por outro lado, muitas vezes, dar inesperado produtos. A adição de bromo ao 1,3-butadieno é um exemplo. Como se pode ver a seguir, obtém-se uma mistura de aproximadamente 50:50 de 3,4-dibromo-1-buteno (o produto esperado) e 1,4-dibromo-2-buteno (principalmente o isómero E). O último composto é notável em que a ligação dupla restante é encontrada em um local onde não havia ligação dupla no reagente. Esta interessante relocalização requer uma explicação.
CH2=CH-CH=CH2 + Br2  |
BrCH2CHBr-CH=CH2 + | BrCH2CH=CHCH2Br |
| 3,4-dibromo-1-buteno | 1,4-dibromo-2-buteno |
O esperado, além de produtos de reações deste tipo é o resultado de 1,2-além de, por exemplo, a ligação para o adjacente de carbonos da dupla ligação. O produto inesperado provém da adição de 1,4, ou seja, da ligação aos átomos de carbono terminais de um dieno conjugado com uma mudança da ligação dupla restante para a 2,3-localização. (Estes números referem-se aos quatro carbonos do dieno conjugado e não são números de nomenclatura IUPAC.) As composições do produto dependem frequentemente da temperatura: a 40 oC, 85% da mistura do produto na reação de adição acima é o 1,4 produto, enquanto a 0 oC, apenas cerca de 30% é o 1,4 produto.
ligação de um átomo eletrofílico ou grupo a um dos átomos de carbono final de um dieno conjugado ( carbono #1 na figura abaixo) gera um intermediário de catião alilo. Tais catiões são estabilizados pela deslocalização da carga, e é essa deslocalização que responde pelo produto de 1,4-adição produzido em tais reações de adição. Como mostrado no diagrama, a carga positiva é distribuída sobre os carbons #2 e # 4 por isso é nesses locais que os componentes nucleofílicos se ligam. Note que a estabilização da ressonância do cátion alilo é maior do que a estabilização comparável do 1,3-butadieno, porque a carga é deslocalizada no primeiro, mas criada e separada no segundo.
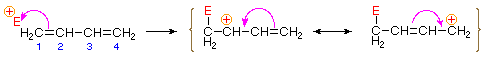
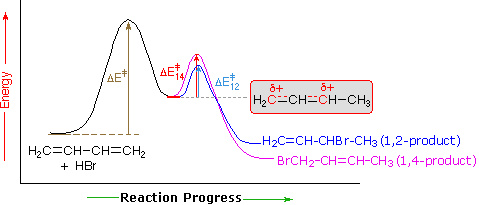
Uma explicação para a influência da temperatura é mostrado no seguinte diagrama de energia para a adição de HBr ao 1,3-butadieno. O passo inicial em que um próton se liga ao carbono #1 é o passo de determinação da taxa, como indicado pela grande energia de ativação (seta cinza claro). O segundo passo mais rápido é o passo de determinação do produto, e há dois caminhos de reação (azul colorido para 1,2-adição e magenta para 1,4-adição). A adição 1,2 tem uma energia de ativação menor que 1,4-adição – ela ocorre mais rápido do que 1,4 adição, porque o nucleófilo brometo é mais próximo do carbono #2, em seguida, do carbono #4. No entanto, o 1,4-produto é mais estável do que o 1,2-produto. A baixas temperaturas, os produtos são formados irreversivelmente e refletem as taxas relativas das duas reações concorrentes. Isto é chamado de controle cinético. A temperaturas mais elevadas, o equilíbrio é estabelecido entre os produtos, e o produto de 1,4 é favorecido termodinamicamente.
Quando um dieno conjugado é atacado por um electrophile, os produtos resultantes são uma mistura de 1,2 e 1,4 isómeros. A cinética e a termodinâmica controlam uma reacção quando existem dois produtos em condições de reacção diferentes. O produto cinético (Produto A) será formado rapidamente, e o produto termodinâmico (Produto B) será formado mais lentamente. Normalmente, o primeiro produto formado é o produto favorecido mais estável, mas neste caso, o produto mais lento formado é o produto mais estável; produto B.
introdução
como os dienos não conjugados, os dienos conjugados são sujeitos a ataque por eletrofílicos. De fato, eletrófilos conjugados experimentam uma reatividade cinética relativamente maior quando reagiram com eletrófilos do que dienos não conjugados. Após adição eletrofílica, o dieno conjugado forma uma mistura de dois produtos—o produto cinético e o produto termodinâmico—cuja relação é determinada pelas condições de reação. Uma reação que produz mais Produto termodinâmico está sob controle termodinâmico, e da mesma forma, uma reação que produz mais Produto cinético está sob controle cinético.
Básica Reação
Detalhada do Mecanismo de
Conclusão
A reatividade dos dienos conjugados (hidrocarbonetos que contêm duas ligações duplas) varia em função da localização das ligações duplas e a temperatura da reação.Estas reacções podem produzir produtos termodinâmicos e cinéticos. Ligações duplas isoladas fornecem dienos com menos estabilidade termodinamicamente do que dienos conjugados. No entanto, eles são mais reativos cineticamente na presença de eletrófilos e outros reagentes. Isto é resultado da adição de Markovnikov a uma das ligações duplas. Um carbocation é formado após uma ligação dupla é aberta. Esta carbocação tem duas estruturas de ressonância e adição pode ocorrer em qualquer um dos carbonos positivos.
Practice Problems
- Write out the products of 1,2 addition and 1,4-addition of a) HBr and Br. b) DBr a 1,3-ciclo-hexadieno. O que é incomum sobre os produtos de 1,2 – e 1,4 – adição de HX para 1,3-dienos cíclicos não-substituídos?O produto de 1,2-adição é formado mais rapidamente a temperaturas mais elevadas, apesar de ser o produto de 1,4-adição que predomina nestas condições?
- por que é o produto de 1,4-adição o produto termodinamicamente mais estável?
- de entre os seguintes catiões radicais, qual não é uma estrutura de ressonância razoável?
5. A adição de 1 equivalente de bromo a 2,4-hexadieno a 0 graus C dá 4,5-dibromo-2-hexeno mais um isómero. Qual dos seguintes elementos é esse isómero:
- 5,5-dibromo-2-hexeno
- 2,5-dibromo-3-hexeno
- 2,2-dibromo-3-hexeno
- 2,3-dibromo-4-hexeno
6. Qual dos seguintes será o produto cineticamente favorecido da reação representada?
7. A adição de HBr a 2,3-dimetil-1,3-ciclo-hexadieno pode ocorrer na ausência ou presença de peróxidos. Em cada caso, são obtidos dois produtos isoméricos C8H13Br. Qual dos seguintes é um produto comum de ambas as reações?
8. e 9.
8. O cineticamente controlada produto acima reação é:
- 3-Cloro-1-Buteno
- 1-Cloro-2-Buteno
9. Para a reação em questão 8, Qual é o resultado de 1,4-adição?
- 3-Cloro-1-Buteno
- 1-Cloro-2-Buteno
Respostas para os Problemas
1. A) o mesmo produto para ambos os modos de adição.
B) ambos os isómeros cis e trans se formarão.
a adição do HX a cicloalka-1,3-dienos não-substituídos em 1,2 – ou 1,4-maneira dá o mesmo produto becasuse de simetria.
2. Sim. o produto cinético ainda se formará mais rápido, mas neste caso haverá energia suficiente para formar o produto termodinâmico porque o produto termodinâmico é ainda mais estável.
3. O 1,4-produto é mais termodinamicamente estável porque existem dois grupos alquilo em cada lado da dupla ligação. Este formulário proporciona estabilidade à estrutura global.
4. Todos estes isómeros são viáveis.
5. D
6. C
7. D
8. A
9. B
Contribuintes
-
William Reusch, Professor Emérito (Michigan State U.), Livro Virtual de Química Orgânica
-
Jim Clark (Chemguide.co.reino unido)
- Natasha Singh