articol
John Plante*, Chelsea Eason, Alan Snyder, Dirk Elston
Departamentul de Dermatologie și Chirurgie Dermatologică, Universitatea de Medicină din Carolina de Sud, Charleston, Carolina de Sud
Lichen planopilaris (LPP) este o alopecie cicatricială primară caracterizată prin prurit, sensibilitate, spini foliculari și eritem în faza Activă1-3. Deși etiologia exactă este necunoscută, patogeneza implică inflamația cronică, mediată de limfocite, care poate duce în cele din urmă la pierderea ireversibilă,cicatrizantă a părului prin distrugerea selectivă a foliculului de păr1, 2. Există trei variante ale LPP și includ forma clasică, alopecia fibroasă frontală (FFA) și sindromul Graham-Little-Piccardi-Lassueur (alopecia progresivă a scalpului, axilelor, sprâncenelor și pubisului)2. LPP se dovedește adesea refractară la terapiile standard și urmează un curs imprevizibil, recidivant, ducând frecvent la o calitate a vieții grav diminuată1,2,4,5. Aici vom discuta în continuare studiul nostru recent privind utilizarea tofacitinib în tratamentul lpp6 recalcitrant.
numeroase terapii au fost utilizate pentru a trata LPP cu succes variabil1-3,5,7-9. Deoarece tratamentele disponibile în prezent nu duc de obicei la regenerarea părului, managementul este îndreptat spre scăderea ratei de cădere a părului, controlul simptomelor și reducerea inflamației2, 9. Terapiile de primă linie includ corticosteroizi topici intralezionali și cu potență ridicată, dar acestea pot duce la atrofia scalpului și pot compromite succesul viitorului transplant de păr. Alți agenți topici prezintă un risc mai mic de atrofie și includ inhibitorii de calcineurină tacrolimus și pimecrolimus2. Deși nu controlează procesul inflamator de bază,atât minoxidilul topic,cât și cel oral pot fi, de asemenea, utilizate pentru a maximiza regenerarea părului la pacienții care suferă, de asemenea, de alopecie moștenită – aproape 50% din populație9, 10. Terapiile sistemice suplimentare includ hidroxiclorochină, micofenolat de mofetil, ciclosporină, metotrexat, talidomidă, doxiciclină, retinoizi, pioglitazonă, inhibitori ai 5-alfa reductazei și prednisolon pe termen scurt1,2,9. Studii recente au sugerat potențialul naltrexonei orale cu doze mici, injecțiilor cu plasmă bogată în trombocite și intervențiilor non-farmacologice, cum ar fi laserul excimer,dar niciuna nu a fost uniform eficientă5,7, 8. În timp ce bucățile de păr și extensiile pot crește volumul și pot acoperi zonele alopecice, trebuie să se acorde atenție pentru a evita tracțiunea9.
într-un studiu recent publicat, am investigat potențialul formulărilor topice și orale (sistemice) ale tofacitinib6. Tofacitinib este un inhibitor Janus kinase (JAK) 1/3 cu eficacitate împotriva mai multor afecțiuni dermatologice mediate imun, inclusiv dermatita atopică, alopecia areata și vitiligo 11-14. Activitatea sa imunomodulatoare este mediată prin inhibarea căii de semnalizare JAK/STAT12, 13. În LPP, interferonii au fost implicați în facilitarea recrutării limfocitare și pierderea privilegiului imun al celulelor epiteliale umflate1. Prin efectele tofacitinib asupra căii JAK / STAT, această inflamație mediată de interferon poate fi redusă, îmbunătățind astfel simptomele și prevenind distrugerea foliculară1,11-13.
am explorat potențialul terapeutic al tofacitinibului în tratamentul LPP refractar printr-o analiză retrospectivă a diagramei6. Din cunoștințele autorilor, acesta este al doilea studiu care investighează utilizarea tofacitinib în managementul LPP1. Studiul nostru a inclus nouă pacienți care nu au reușit alte terapii-trei au folosit topic, cinci au folosit oral și unul a folosit ambele formulări.
un răspuns inițial favorabil a fost obținut la toți pacienții, cu excepția unui singur pacient. Subiectul rămas a răspuns slab la terapia topică, dar s-a îmbunătățit cu terapia sistemică cu tofacitinib. Deși numărul absolut de pacienți este mic, a existat o tendință spre un răspuns clinic mai bun la cei tratați sistemic comparativ cu cei tratați topic. Timpul până la un răspuns favorabil a variat de la 1 la 7 luni, 5 și 8 pacienți demonstrând îmbunătățiri în primele 3 și, respectiv, 5 luni de tratament.
modelul nostru actual de practică este de a trata boala rapid progresivă cu un curs scurt de prednison sau ciclosporină și apoi încercați să treceți la terapia topică cu inhibitor de calcineurină atunci când este posibil (Figura 1). Un subgrup de pacienți va obține remisia bolii lor cu pioglitazonă în doze de 15-45 mg pe zi. Pacienții trebuie informați cu privire la indicația marcată, datele mixte privind eficacitatea și avertizarea în cutie despre cancerul vezicii urinare cu utilizare prelungită. Practica noastră este să nu continuăm pioglitazona după maximum 9 luni cu doze crescătoare în trepte. Agenții adjuvanți includ naltrexona la o doză de 5 mg pe zi și N-acetilcisteina la doze de 600-1200 mg de trei ori pe zi. Laserul Excimer, UVB cu bandă îngustă de mână sau terapia cu capac cu laser de mică intensitate este adesea folosită ca terapie adjuvantă la cei cu răspuns parțial. Hidroxiclorochina poate fi ocazional benefică, dar majoritatea pacienților referiți la clinica noastră au eșuat deja în terapia cu hidroxiclorochină. Cei care nu răspund pot necesita tratament cu metotrexat, micofenolat de mofetil sau tofacitinib. Rezultatele studiului nostru recent oferă un sprijin suplimentar ideii că atât tofacitinibul topic, cât și cel sistemic pot fi modalități viabile de tratament adjuvant în cazurile refractare. Tulburările de păr răspund adesea lent și reevaluăm la intervale de 3 luni pentru a determina răspunsul la terapie și nevoia de escaladare.
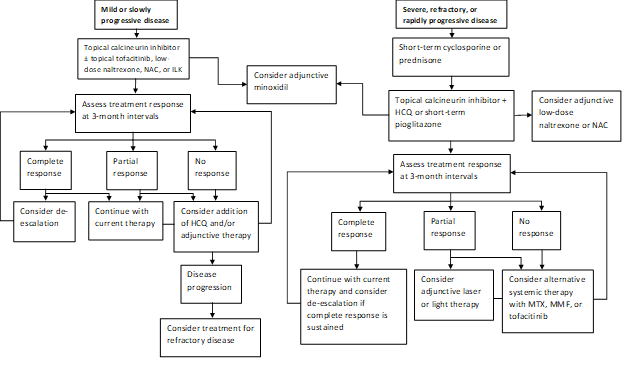
Figura 1: algoritm de tratament în trepte pentru LPP
NAC, N-acetilcisteină; ILK, corticosteroizi intralezionali; HCQ, hidroxiclorochină; MTX, metotrexat, MMF, micofenolat mofetil
când se ia în considerare utilizarea tofacitinib în practică, practicienii trebuie să echilibreze beneficiile acestui medicament cu riscurile sale. Cohorta noastră a prezentat doar anomalii minore de laborator (una pe actualitate și două pe terapie sistemică) care nu au necesitat intervenție. Cu toate acestea, furnizorii ar trebui să fie conștienți de efectele secundare potențiale atunci când prescriu acest medicament, inclusiv un risc crescut de infecție, citopenii, hiperlipidemie, anomalii hepatice și renale, precum și potențialul evenimentelor tromboembolice14-16. În timp ce formularea topică a demonstrat concentrații plasmatice mai mici decât omologul său sistemic, evenimentele adverse minore și anomaliile de laborator au fost încă raportate în cazul terapiei topice13.
deși rezultatele noastre sunt promițătoare, ele trebuie interpretate după luarea în considerare a mai multor limitări. Am utilizat un proiect de studiu retrospectiv și nu am putut utiliza o măsură validată a severității bolii, cum ar fi indicele de activitate Lichen Planopilaris (Lppai)1,3. LPPAI este potrivit pentru studii prospective și oferă un instrument standardizat prin care Furnizorii pot compara direct rezultatele în diferite modalități de tratament. Semne și simptome precum eritemul, sensibilitatea, prezența coloanei vertebrale foliculare și zona afectată au fost utilizate pentru a evalua răspunsul terapeutic, dar studiile viitoare ar trebui să includă și o măsură a calității vieții. Posibilitatea de părtinire a observatorilor nu poate fi exclusă, deoarece studiul nostru a fost deblocat și non-randomizat.
în plus, întreaga noastră cohortă a folosit tofacitinib adjuvant, ceea ce face dificilă evaluarea contribuției independente a medicamentului. Într-un studiu anterior, o porțiune (n=5) din cohortă a utilizat tofacitinib ca monoterapie, iar majoritatea subiecților au obținut rezultate favorabile, dar acest studiu a fost, de asemenea, limitat de dimensiunea mică a eșantionului și de designul retrospectiv1.
studiile actuale sunt limitate de dimensiunile mici ale eșantioanelor și de proiectele de studiu retrospective, iar studiile prospective bine concepute sunt foarte necesare. Vă recomandăm o abordare treptată a terapiei pentru a minimiza riscul de efecte adverse. Riscul de cicatrizare permanentă trebuie evaluat în raport cu riscul de evenimente adverse grave, având în vedere factorii și comorbiditățile individuale ale pacientului, iar pacienții trebuie să fie parteneri activi în luarea deciziilor. Transplantul de păr poate fi luat în considerare odată ce controlul bolii a fost atins și inflamația a scăzut. Este important să rețineți că terapia agresivă, cum ar fi prednisonul sau ciclosporina, este de obicei necesară în săptămânile următoare transplantului pentru a evita apariția bolilor. Este de așteptat o uzură treptată a firelor de păr transplantate, chiar și după transplantul reușit, dar datele sugerează că pacienții sunt în general mulțumiți de rezultate și constată că transplantul îmbunătățește calitatea vieții.
abrevieri
LPP, lichen planopilaris; FFA, alopecia fibroasă frontală; JAK, Janus kinaza; STAT, Traductor de semnal și activator al proteinelor de transcripție; Lppai, Indicele de activitate Lichen Planopilaris.
conflicte de interese
autorii nu declară niciun conflict de interese.
- Yang CC, Khanna T, Sallee B, și colab. Tofacitinib pentru tratamentul lichen planopilaris: o serie de cazuri. Dermatol Ther. 2018; 31 (6): e12656. doi: 10.1111 / dth.12656
- Babahosseini H, Tavakolpour S, Mahmoudi H, și colab. Lichen planopilaris: studiu retrospectiv privind caracteristicile și tratamentul a 291 de pacienți. J Dermatolog Trata. 2019; 30(6): 598–604. doi:10.1080/09546634.2018.1542480
- Chiang C, Sah D, Cho BK și colab. Hidroxiclorochina și lichen planopilaris: eficacitatea și introducerea sistemului de notare a indicelui de activitate Lichen Planopilaris. Sunt Acad Dermatol. 2010; 62(3): 387-392. doi: 10.1016 / j. jaad.2009.08.054
- Alirezaei P, Ahmadpanah M, Rezanejad A, și colab. În comparație cu controalele, persoanele cu Lichen Planopilaris au mai multă depresie, o stimă de sine mai scăzută și o calitate a vieții mai scăzută. Neuropsihobiologie. 2019; 78(2): 95-103. doi:10.1159/000499135
- Jha AK. Plasma bogată în trombocite ca tratament adjuvant în lichen planopilaris. Sunt Acad Dermatol. 2019; 80(5): e109-e110. doi: 10.1016 / j. jaad.2018.09.013
- Plante J, Eason C, Snyder A, și colab. Tofacitinib în tratamentul lichen planopilaris: o revizuire retrospectivă . Sunt Acad Dermatol. 2020; S0190-9622(20)30979-8. doi:10.1016 / j. jaad.2020.05.104
- Lajevardi V, Salarvand F, Ghiasi M, și colab. Eficacitatea și siguranța administrării orale a unei doze mici de naltrexonă versus placebo la pacienții cu lichen planopilaris: un studiu clinic randomizat controlat . J Dermatolog Trata. 2020; 1-5. doi:10.1080/09546634.2020.1774488
- Lee B, Elston DM. Utilizările naltrexonei în condiții dermatologice. Sunt Acad Dermatol. 2019; 80(6): 1746-1752. doi: 10.1016 / j. jaad.2018.12.031
- Bolduc C, Sperling LC, Shapiro J. alopecie cicatricială primară: Alopecie cicatricială primară limfocitară, inclusiv lupus eritematos cutanat cronic, lichen planopilaris, alopecie fibroasă frontală și sindromul Graham-Little. Sunt Acad Dermatol. 2016; 75(6): 1081-1099.
- Vano-Galvan s, Trindade de Carvalho L, Saceda-Corralo D și colab. Minoxidilul Oral îmbunătățește grosimea părului de fundal în lichen planopilaris . Sunt Acad Dermatol. 2020; S0190-9622(20)30566-1. doi: 10.1016 / j. jaad.2020.04.026
- Tegtmeyer K, Zhao J, Maloney NJ și colab. Studii Off-label privind tofacitinib în dermatologie: o revizuire . J Dermatolog Trata. 2019; 1–11. doi: 10.1080/09546634.2019.1673877
- Montilla AM, Gomez-Garcia F, Gomez-Arias PJ și colab. Revizuirea domeniului privind utilizarea medicamentelor care vizează calea JAK / STAT în dermatita atopică, Vitiligo și Alopecia areata. Dermatol Ther (Heidelb). 2019; 9(4): 655–683. doi: 10.1007 / s13555-019-00329-y
- Hosking AM, Juhasz M, Mesinkovska NA. Inhibitori actuali ai Janus kinazei: o revizuire a aplicațiilor în dermatologie. Sunt Acad Dermatol. 2018; 79(3): 535–544. doi: 10.1016 / j. jaad.2018.04.018
- Shreberk-Hassidim R, Ramot Y, zlotogorski A. Janus inhibitori ai kinazei în dermatologie: o revizuire sistematică. Sunt Acad Dermatol. 2017; 76(4): 745-753.e19. doi: 10.1016 / j. jaad.2016.12.004
- Xeljanz/Xeljanz XR (tofacitinib) . New York, NY: Divizia Pfizer Laboratories a Pfizer Inc. https://labeling.pfizer.com/showlabeling.aspx?id=959; 2019. Accesat La 7 Iulie 2020.
- FDA. Studiul de siguranță constată riscul formării cheagurilor de sânge în plămâni și moartea cu o doză mai mare de tofacitinib (Xeljanz, Xeljanz XR) la pacienții cu artrită reumatoidă; FDA pentru a investiga. https://www.fda.gov/drugs/drug-safety-and-availability/safety-trial-finds-risk-blood-clots-lungs-and-death-higher-dose-tofacitinib-xeljanz-xeljanz-xr; 2019. Accesat La 6 Iulie 2020.