ATrain Education
även om vi lär oss mer varje dag om patofysiologin av Parkinsons sjukdom, anses den fortfarande i stor utsträckning idiopatisk (av okänd orsak). Det involverar sannolikt interaktionen mellan värdkänslighet och miljöfaktorer. En liten andel av fallen är genetiskt kopplade och genetiska faktorer studeras intensivt.
fysiologiskt är symtomen associerade med Parkinsons sjukdom resultatet av förlusten av ett antal neurotransmittorer, särskilt dopamin. Symtomen förvärras med tiden eftersom fler och fler av de celler som drabbats av sjukdomen går förlorade. Sjukdomsförloppet är mycket varierande, med vissa patienter som uppvisar mycket få symtom när de åldras och andra vars symtom utvecklas snabbt.
Parkinsons ses alltmer som en komplex neurodegenerativ sjukdom med en sekvens av progression. Det finns starka bevis för att det först påverkar den dorsala motorkärnan i vagusnerven och luktlökarna och kärnan, sedan locus coeruleus och så småningom substantia nigra. Kortikala områden i hjärnan påverkas i ett senare skede. Skador på dessa olika neuronala system står för de mångfacetterade patofysiologiska förändringarna som orsakar försämringar inte bara för motorsystemet utan också för de kognitiva och neuropsykologiska systemen (Kwan & Whitehill, 2011).
rollen av dopamin
dopamin, som andra neurotransmittorer, överför kemiska meddelanden från en nervcell till en annan över synapsen, ett utrymme mellan den presynaptiska cellen och den postsynaptiska receptorn. Dopamin utsöndras i synapsen från membranlagringsvesiklar i det presynaptiska membranet. Den korsar synapsen och binder till det postsynaptiska membranet, där det aktiverar dopaminreceptorer. Oanvänd dopamin kvar i synapsen absorberas tillbaka i den presynaptiska cellen; en gång tillbaka i den presynaptiska cellen packas överskottet av dopamin i lagringsvesiklar och släpps en gång till i synapsen.
inom synapsen, när dopamin reser från en cell till en annan, kan den brytas ner och göras inaktiv av två enzymer, MAO (monoaminoxidas) och COMT (katekol-O-metyltransferas). En terapeutisk strategi introducerar en MAO-hämmare i synapsen, som avbryter verkan av MAO-enzymet och förhindrar nedbrytning av dopamin. Detta gör att mer dopamin kan förbli i synapsen och ökar sannolikheten för att det kommer att binda till det postsynaptiska membranet.
kemisk synaptisk överföring
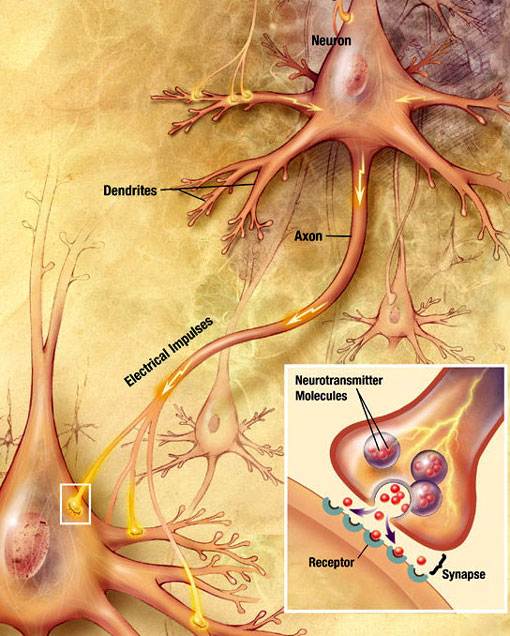
en elektrokemisk våg som kallas en åtgärdspotential färdas längs axonen i en neuron. När åtgärdspotentialen når den presynaptiska terminalen, provocerar den frisättningen av en liten mängd neurotransmittormolekyler, vilka binder till kemiska receptormolekyler belägna i membranet i den postsynaptiska neuronen, på motsatt sida av den synaptiska klyftan. Källa: Wikimedia Commons.
progressiv förlust av dopamin
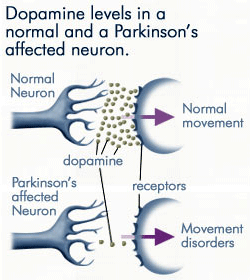
eftersom mindre och mindre dopamin produceras av neuronerna som påverkas av Parkinsons sjukdom, är mycket mindre dopamin tillgängligt för att binda till dopaminreceptorerna på det postsynaptiska membranet. Källa: anti-agingfirewalls.com.
även om dopamincellförlust inte kan mätas direkt, visar mätningar hos neurologiskt normala människor och hos icke-mänskliga primater en långsam progressiv förlust av dopamin med åldern. Vid Parkinsons sjukdom sker förlusten i mycket högre takt och både biokemiska åtgärder och avbildningsstudier tyder på att det finns en signifikant minskning av dopamin när motoriska symtom uppträder. Enligt denna uppfattning är Parkinsons sjukdom en accelererad version av celldöd som ses med normal åldrande (Cookson, 2009). Detta illustreras i diagrammet nedan, som visar nedgången av dopaminerga neuroner under normal åldrande, i idiopatisk PD, i PD orsakad av miljö-eller genetiska faktorer och i tidig PD.
utveckling av Dopaminutarmning vid Parkinsons sjukdom
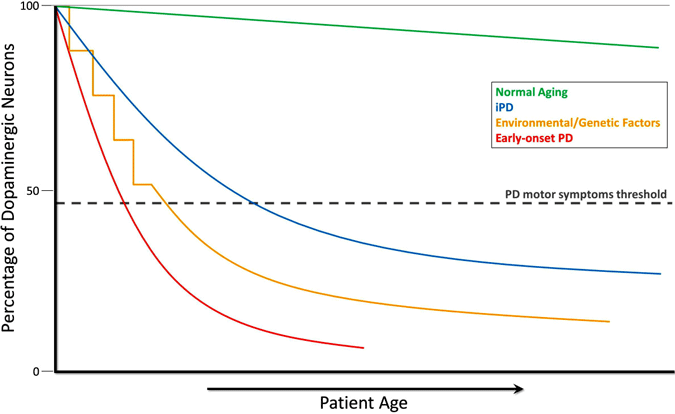
under normal åldrande (grön linje) sker liten men långsam dopaminerg degeneration utan några motoriska symtom. Idiopatisk PD (IPD, blå linje) är av okänt ursprung men tros utvecklas gradvis, med en långsam degenerering av dopaminerga neuroner som leder till de klassiska PD-motoriska symtomen senare i livet. En annan modell av dopamin-neurodegeneration som leder till PD-motoriska symtom innebär upprepad exponering för miljögifter över tid i kombination med en genetisk predisposition till dopaminerg neuronförlust (gul linje). Tidig debut PD (röd linje), som orsakas av mutationer i PARKIN genen, innebär en brant nedgång i dopaminerga neuroner, och PD motoriska symtom kan presentera decennier före de i idiopatisk PD. Ytterligare ett scenario (ej visat) av PD-motorsymtomutveckling involverar möjliga miljögifter i utero eller genetiska faktorer som leder till ett atypiskt lågt antal dopaminerga neuroner vid födseln och ökad mottaglighet för PD-utveckling (Haas et al., 2012).
degenerering av dopaminneuroner är särskilt tydlig i en del av substantia nigra som kallas pars compacta. Signifikant ökar förlusten av dopamin i pars compacta den totala excitatoriska drivningen i basala ganglier,* stör frivillig motorstyrning och orsakar de karakteristiska symptomen på PD. Normalisering av motorisk funktion ses initialt med levodopabehandling (Gasparini et al., 2013).
* huvudkomponenterna i basala ganglier är striatum (caudatkärnan och putamen), globus pallidus, substantia nigra, nucleus accumbens och subthalamic nucleus.
när svårighetsgraden av PD ökar leder utarmningen av dopamin till ytterligare förändringar i de basala ganglierna, inklusive förändrad funktion hos andra basala ganglier neurotransmittorer såsom glutamat, GABA och serotonin (Gasparini et al., 2013). Även om det finns relativ sårbarhet hos dopaminproducerande neuroner i substantia nigra, påverkas inte alla dopaminceller i Parkinsons sjukdom; i vissa delar av hjärnan sparas de dopaminproducerande neuronerna relativt (Cookson, 2009).
den nigrostriatala vägen
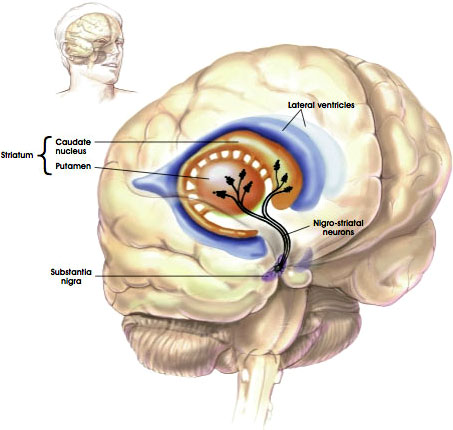
källa: NIH, nd.
Lewy-kroppar och alfa-synuklein
Lewy-kroppar är onormala aggregat och inneslutningar av protein som utvecklas inuti nervceller hos personer med Parkinsons sjukdom. Aggregeringarna består vanligtvis av olösliga fibrillära aggregat innehållande felveckade proteiner. Ett stort antal molekyler har identifierats i Lewy-kroppar men ett protein som kallas alfa-synuklein är huvudkomponenten.
Lewy-kroppar (Alfa-Synukleininkluderingar)
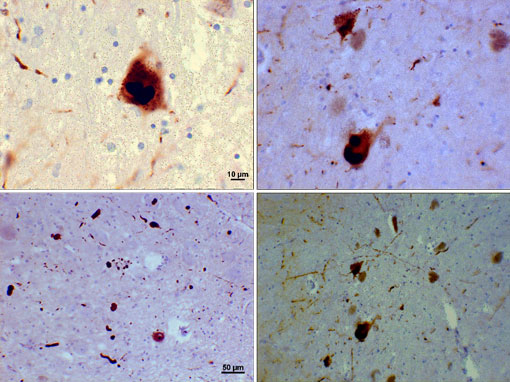
Fotomikrografi av regioner av substantia nigra i en Parkinsons patient som visar Lewy-kroppar och Lewy neuriter i olika förstoringar. Topppaneler visar en 60X förstoring av alfa-synuclein intraneuronala inklusioner aggregerade för att bilda Lewy-kroppar. Bottenpanelerna är 20 förstoringsbilder av kakor som visar strängliknande Lewy neuriter och rundade Lewy-kroppar i olika storlekar. Bilder med tillstånd av Suraj Rajan.
Lewy-patologi omfattar många regioner i hjärnan och vissa rapporter har föreslagit att substantia nigra inte är den första platsen där Lewy-kroppar bildas i Parkinsons sjukdom. Inklusioner och aggregat symboliserar sannolikt slutstadiet av en kaskad av komplicerade händelser. Ett tidigare stadium kan vara mer direkt knutet till sjukdomspatogenesen än inneslutningarna själva, vilket kan eller inte kan representera diagnostiska kännetecken.
Lewy-kroppar ses också i” demens med Lewy-kroppar”, vilket tyder på att dessa tillstånd är relaterade till varandra genom delad patologi och eventuellt genom delad etiologi. Varken cellförlust eller bildandet av Lewy-kroppar är absolut specifikt för PD men båda krävs för diagnos av PD enligt nuvarande definitioner (Cookson, 2009).
neurodegenerativa störningar såsom Alzheimers sjukdom, frontal-temporal degeneration, prionsjukdom, Huntingtons chorea och motoneuronsjukdomar realiseras alltmer för att ha vanliga cellulära och molekylära mekanismer, inklusive proteinaggregering och inklusionskroppsbildning i vissa delar av nervsystemet (Jellinger, 2011).
Inflammation och immunsvar
utlösaren av dopaminerg degeneration verkar vara multifaktoriell-påverkad av både endogena och miljömässiga element. Inflammation och immunsvar betraktas alltmer som viktiga mediatorer av dopaminerg degeneration. Stora befolkningsstudier har föreslagit att individer som tar icke-steroida antiinflammatoriska läkemedel (NSAID) har mindre risk att utveckla idiopatisk PD, vilket tyder på att antiinflammatoriska läkemedel kan vara en lovande sjukdomsmodifierande behandling för Parkinsonpatienter (Barcia, 2013).
nya försöksfaser har involverat antiinflammatoriska behandlingar – specifikt letar efter en objektiv biomarkör i behandlingar som syftar till att minska inflammatoriska förändringar hos patienter med PD. Forskare använder neuroimagingverktyg för att utveckla en relevant biomarkör med avsikt att testa detta i stora kliniska avbildningsstudier. Resultatet av dessa studier kommer att ge data för att testa och övervaka utvecklingen av antiinflammatoriska behandlingar för PD och kommer att hjälpa till att identifiera det aktuella terapeutiska fönstret för att stoppa, eller åtminstone långsam, inflammatorisk medierad dopaminerg degeneration (Barcia, 2013).
Parkinsonism
Parkinsonism, även känd som ”atypisk Parkinsons”, ”sekundär Parkinsons” eller ”Parkinsons syndrom”, är ett neurologiskt syndrom där en patient uppvisar några av symtomen associerade med Parkinsons sjukdom—tremor, styvhet, bradykinesi och postural instabilitet. Men parkinsonism är inte Parkinsons sjukdom. Parkinsonism tros inte orsakas av Parkinsons sjukdom och patienter svarar vanligtvis dåligt på farmakologisk intervention. Parkinsonism har ofta en identifierbar orsak, såsom exponering för toxiner, metamfetamin, trauma, flera stroke, andra nervsystemet eller sjukdom. I allmänhet ses Lewy-kroppar inte i parkinsonism.
termen parkinsonism är också associerad med störningar såsom Progressiv Supranukleär Pares, multipel systematrofi, Lewy body demens, kortikobasal degeneration, vaskulär parkinsonism, läkemedelsinducerad parkinsonism och parkinsonism sekundär till infektion och andra orsaker (Hohler et al., 2012). En form av reversibel parkinsonism kan uppstå vid användning av vissa neuroleptiska läkemedel, särskilt reserpin, antipsykotika (haloperidol) och metoklopramid. Exponering för vissa toxiner, svår kolmonoxidförgiftning och kvicksilverförgiftning kan också leda till parkinsonism.
utseendet i början av 1980-talet av parkinsonismsymtom hos en grupp narkomaner som hade konsumerat en förorenad sats av ett syntetiskt opiat ledde till upptäckten av den kemiska MPTP som ett medel som orsakar parkinsonismsyndrom hos icke-mänskliga primater såväl som hos människor. MPTP kan produceras när man gör en form av heroin (MPTP omvandlas till ett neurotoxin som selektivt förstör dopaminceller i substantia nigra). Dessa fall är sällsynta och har mest påverkat långvariga narkotikamissbrukare.
metamfetaminmissbruk har också kopplats till parkinsonism. I försöksdjur skadar exponering för metamfetamin dopaminerga fibrer i striatum* såväl som cellkropparna i substantia nigra, vilket ekar degenerationen som observerats hos humana patienter med PD. Selektiv skada på dopaminerga terminaler i striatum har också observerats hos humana metamfetaminanvändare, även om det hittills inte finns några bevis för att missbruk av metamfetamin skadar dopaminerga cellkroppar i substantia nigra (Granado et al., 2013).
* den största kärnan i basala ganglier, striatum består av caudatkärnan och putamen.
det har antagits att metamfetaminanvändning kan predisponera användare för framtida utveckling av PD. Denna hypotes har fått stöd av det senaste epidemiologiska arbetet som indikerar att metamfetaminanvändare har en ökad risk att utveckla PD. Detta överensstämmer med de ihållande neurotoxiska effekterna av metamfetamin i försöksdjur (Granado et al., 2013).
patienter med parkinsonism är ofta svåra att hantera som polikliniker. Komplexiteten hos deras symtom, de extra kognitiva och autonoma underskotten, det dåliga svaret på de flesta PD-Läkemedel och den relativt snabba nedgången i status bidrar till utmaningarna för att hantera dessa patienter, särskilt när sjukdomen fortskrider (Hohler et al., 2012).