tert-Butyl litium eller T-BuLi
Ben Valsler
den här veckan talar Katrina kr Jacobmer till en forskare som hoppas tämja ett farligt reagens med salta lösningsmedel.
Katrina kr Exceptioner
det finns några kemikalier som du verkligen inte vill röra med-dioxygendifluorid, till exempel, som reagerar våldsamt med alla slags föreningar även vid -180 Macau C; eller kvicksilverazid, som inte bara detonerar vid den minsta provokationen utan också spyr ut giftiga kvicksilverföreningar när det exploderar. Lyckligtvis är det kemiska nyfikenheter, något forskare gjort en gång men är osannolikt att någonsin göra igen (med god anledning). Men andra farliga föreningar är bara så användbara att kemister inte kan hålla händerna borta från dem. En av dem är tert-butyl litium, även kallad t-BuLi: en häftklammer för syntetiska kemister som har en ganska pyroforisk sida till den.
som huvudgrupp organometallisk kemist har Eva Hevia från University of Strathclyde inte bara arbetat med t-BuLi utan också med många andra alkyl litiumföreningar.

källa: ©
Eva Hevia
Organolitiumföreningar används allmänt över hela världen och det är inte bara i akademin – i maj industriella och kommersiella situationer är dessa reagenser väsentliga. Jag tror att det är 90-95 procent av läkemedel som tillverkas av läkemedelsföretag, de kräver, åtminstone i ett steg av deras syntes, användningen av dessa reagenser. Så konsekvenserna för samhället, och även för ekonomin, är stora.
Katrina kr Actuber
dessa föreningar förblir populära delvis på grund av den stora polariteten över litium-kolbindningen, vilket gör dem extremt reaktiva.
Eva Hevia
men naturligtvis kommer reaktivitet alltid med en avvägning. Avvägningen här är att dessa reagenser ibland lider av låg selektivitet; ibland begränsar de mycket typen av substrat som de kan vara kompatibla med. Så för att försöka övervinna dessa begränsningar måste du i många fall använda dessa reagenser under mycket låga temperaturer, med lösningsmedel som är relativt giftiga och du måste alltid använda dem i frånvaro av luft eller fukt eftersom de sönderdelas mycket snabbt. Och i själva verket är många av dem pyroforiska, så du måste vara mycket försiktig med hur du manipulerar dessa reagenser. Detta kan vara särskilt utmanande när vi tittar på reaktioner i större skala i ett industriellt scenario.
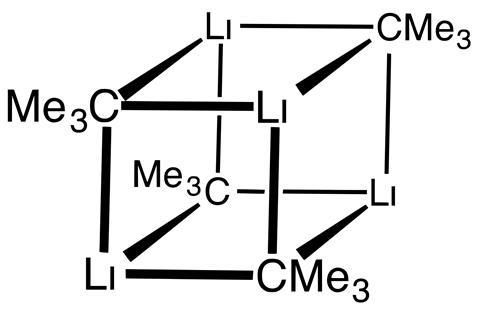
tert-butyl litium
källa: SMOKEFOOT, CC-BY-SA 4.0
Katrina kr exceptional
litium är ett av de element som verkligen vill bli av med en av dess elektroner, som den skjuter mot det närliggande kolet. Men det som verkligen gör t-BuLi reaktivt, jämfört med dess mycket vänligare linjära kusin n-butyl litium, är att det tertiära kolet inte tycker om att hantera litiums överskottselektron. Att vara omgiven av tre metylgrupper som redan är mildt elektrondonerande plus den extra elektronen betyder att det centrala kolet har mycket lokaliserad negativ laddning. Följaktligen är t-BuLi mycket basisk och plockar protoner från allt det kan nå: från svagt sura organiska föreningar till vanliga lösningsmedel som tetrahydrofuran eller dietyleter, och naturligtvis vatten.
även små mängder vatten (t.ex. vattenånga i luft) och syre är tillräckligt för att producera en våldsam reaktion. Vid kontakt med luft spricker t-BuLi spontant i ljusa orange flammor. Eftersom t-BuLi också reagerar med de flesta lösningsmedel, säljer kemiska företag det som en utspädd lösning i oreaktiv hexan eller pentan, som båda också är brandfarliga. Det betyder att om det finns en organolitiumbrand, finns det vanligtvis någon form av brandfarligt lösningsmedel i blandningen också.

källa: bild med tillstånd av Naveen Sangji
Sheharbano Sangjis tragiska olycka ledde till straffrättsliga anklagelser och en förändring av labbsäkerhetskulturen
det tragiska fallet med UCLA-studenten Sheri Sangji, som dog 2009 från stora brännskador efter ett experiment med stora mängder t-BuLi gick fel, bör påminna varje kemist om att denna förening måste behandlas med respekt. Forskare som arbetar med T-BuLi måste följa strikta säkerhetsåtgärder: att endast använda små mängder och utföra reaktioner under uteslutning av luft och fukt medan de bär icke-brandfarliga kläder och har både en berörd labmate och en nöddusch i närheten är de minsta minimikraven för att hantera t-BuLi säkert.
medan alkyl lithiums är kraftfulla reagens, de är också benägna att sidoreaktioner, bildar värdelösa biprodukter. Detta, utöver säkerhetsproblemen, är anledningen till att kemister vanligtvis utför reaktioner vid -78 kcal C och upprätthåller en inert gasatmosfär i reaktionskärlen för att hålla ut luft och fukt.
Eva Hevia
och jag antar att den ultimata utmaningen i denna typ av kemi är hur vi kan använda dem i en normal atmosfär, utan närvaro av argon eller kvävgas – under luft – och hur vi kan göra dessa reagenser kompatibla med lösningsmedel som är miljövänliga. Och vad vi har funnit är att om vi använder djupa eutektiska lösningsmedel som ett alternativbe-medium – och ett djupt eutektiskt lösningsmedel är en ny typ av lösningsmedel, relaterat till Joniska vätskor, som är miljövänliga, består av komponenter som är biologiskt nedbrytbara och biorenewable – om vi använder denna typ av lösningsmedel kan vi aktivera organolitiumlösningsmedel på ett sådant sätt att reaktionerna sker extremt snabbt vid rumstemperatur. Eftersom de är mycket snabba behöver du inte använda en inert atmosfär och du kan göra dessa reaktioner kompatibla med vatten eller fukt.
Katrina kr Exceptioner
djupa eutektiska lösningsmedel är blandningar av olika salter som är flytande vid rumstemperatur. Medan de flesta joniska föreningar har en mycket hög smältpunkt (natriumklorid till exempel Klockor I strax över 800 grader), blandar rätt salter i rätt mängder en eutektisk – en blandning som smälter vid en mycket lägre temperatur än dess enskilda komponenter. Dessa ganska ovanliga lösningsmedel är giftfria och ganska billiga – En av föreningarna som Hevias team använder är kolinklorid, ett kycklingfodertillsats.
i djupa eutektiska lösningsmedel är organolitiumreaktioner mycket snabbare än i något annat lösningsmedel. Detta skulle föreslå att redan mycket reaktiva alkyllitiumföreningar blir mer reaktiva i den salta lösningsmedelsblandningen, vilket verkar kontraintuitivt. Varför hade Hevias team inget behov av att kontrollera reaktionen genom att kyla den eller leda den under inert atmosfär?
Eva Hevia
när du arbetar i dessa system är din reaktions främsta fiende hydrolys eller nedbrytning av ditt organometalliska reagens. Så vi aktiverar det på ett sätt som vi kan övervinna denna sönderdelningsväg. Samtidigt stämmer vi deras selektivitet, så vi finner i den typ av reaktioner som vi tittar på att vi får bättre selektivitet än när vi använder konventionella lösningsmedel.
Katrina kr Exceptioner
eftersom de består av joner är djupa eutektiska lösningsmedel mycket bra på att stabilisera laddade eller mycket polära molekyler; men exakt hur de fungerar är deras magi ännu inte klart. Hevia tror att de Salta lösningsmedlen också kan tämja andra mer livliga organometalliska reagenser.
Eva Hevia
några av våra första arbeten har visat att vi kan använda Grignard-reagenser som också är mycket grundläggande och mycket viktiga i syntesen. Och en del av det arbete som för närvarande genomgår i våra forskargrupper visar att dessa lösningsmedel också erbjuder stor potential för organiska zinkreagenser som återigen används i många kol-kolbindningsbildande processer, och de är också mycket reaktiva i närvaro av luft och fukt. Så jag tror att det finns två sätt att titta på detta arbete: för det första utvecklar vi nya metoder för att använda dessa reagenser under miljövänliga förhållanden, men för det andra – och detta är något som jag verkligen vill betona – aktiverar vi dessa organometalliska reagenser, oavsett om det är organolitium, zink eller magnesium, för att få dem att fungera ännu bättre än när vi använder inerta atmosfärsförhållanden eller flyktiga organiska lösningsmedel.
Katrina kr exceptional
även om kemister fortfarande behöver hantera t-BuLi och dess bröder med omsorg, kan djupa eutektiska lösningsmedel hjälpa dem att styra t-Bulis kanonkula reaktivitet med mer pil-liknande precision.
Ben Valsler
det var Katrina kr Aukorimer, talar med Eva Hevia från University of Strathclyde om tert-butyl litium eller T-BuLi. Nästa vecka är Brian Clegg tillbaka med en familj av föreningar med några om användningsområden.
Brian Clegg
de är anmärkningsvärt konstruktiva – sällan direkt för användning själva men var och en är en viktig bidragsgivare av byggstenar till andra föreningar. Tyvärr kan vissa av dessa slutprodukter användas i kemiska vapen.
Ben Valsler
gå med Brian nästa vecka för att ta reda på mer. Tills dess, låt oss veta om det finns något du vill att vi ska täcka-e-post [email protected] eller tweet @chemistryworld. Jag är Ben Valsler, tack för att du lyssnade.