tert-Butyl lithium eller t-BuLi
Ben Valsler
i denne uge taler Katrina kr Kristmer til en forsker, der håber at tæmme et farligt reagens med salte opløsningsmidler.
Katrina kr Krismer
der er nogle kemikalier, du virkelig ikke ønsker at rode med – dioksygen difluorid, for eksempel, som reagerer voldsomt med alle mulige forbindelser selv ved -180 C; eller kviksølvat, som ikke kun detonerer ved den mindste provokation, men også spyder ud giftige kviksølvforbindelser, når det eksploderer. Heldigvis er disse kemiske nysgerrigheder, noget forskere lavede en gang, men det er usandsynligt, at de nogensinde vil gøre igen (med god grund). Men andre farlige stoffer er bare så nyttige, at kemikere ikke kan holde deres hænder væk fra dem. En af dem er tert-butyl lithium, også kaldet t-BuLi: en hæfteklammer til syntetiske kemikere, der har en ret pyrofor side til den.
som hovedgruppe organometallisk kemiker har Eva Hevia fra University of Strathclyde ikke kun arbejdet med t-BuLi, men også med en masse andre alkyl lithiumforbindelser.

kilde: ©
Eva Hevia
Organolithiumforbindelser bruges i vid udstrækning over hele verden, og det er ikke kun i den akademiske verden – i Maj Industrielle og kommercielle situationer er disse reagenser vigtige. Jeg tror, det er 90-95 procent af lægemidler, der fremstilles af farmaceutiske virksomheder, de kræver, i det mindste i et trin af deres syntese, brugen af disse reagenser. Så konsekvenserne for samfundet, og også for økonomien, er enorme.
Katrina kr Kristmer
disse forbindelser forbliver populære delvis på grund af den store polaritet på tværs af lithium-carbonbindingen, hvilket gør dem ekstremt reaktive.
Eva Hevia
men selvfølgelig kommer reaktivitet altid med en afvejning. Afvejningen her er, at disse reagenser undertiden lider af lave selektiviteter; nogle gange begrænser de meget den type underlag, som de kan være kompatible med. Så for at forsøge at overvinde disse begrænsninger skal du i mange tilfælde bruge disse reagenser under meget lave temperaturer med opløsningsmidler, der er relativt giftige, og du skal altid bruge dem i fravær af luft eller fugt, fordi de nedbrydes meget hurtigt. Og faktisk er mange af dem pyroforiske, så du skal være meget forsigtig med, hvordan du manipulerer disse reagenser. Dette kan være særligt udfordrende, når vi ser på reaktioner i større skala i et industrielt scenario.
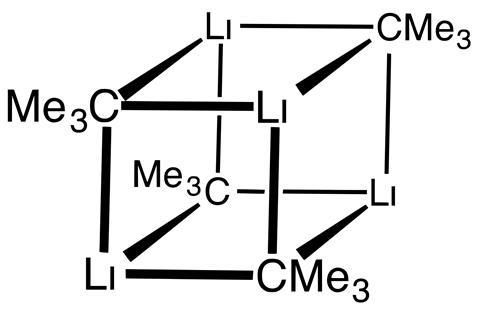
tert-butyl lithium
kilde: Røgfod, CC-BY-SA 4.0
Katrina kr Kristmer
Lithium er et af de elementer, der virkelig ønsker at slippe af med en af sine elektroner, som den skubber mod det nærliggende kulstof. Men hvad der virkelig gør t-BuLi reaktivt, sammenlignet med sin meget venligere lineære fætter n-butyl lithium, er, at det tertiære kulstof ikke nyder at håndtere lithiums overskudselektron. At være omgivet af tre methylgrupper, der allerede er mildt elektrondonerende plus den ekstra elektron, betyder, at det centrale kulstof har en masse lokaliseret negativ ladning. Derfor er t-BuLi meget basisk og plukker protoner fra alt, hvad den kan nå: fra let sure organiske forbindelser til almindelige opløsningsmidler som tetrahydrofuran eller diethylether, og selvfølgelig vand.
selv små mængder vand (såsom vanddamp i luften) og ilt er nok til at frembringe en voldsom reaktion. Ved kontakt med luft bryder t-BuLi spontant ind i lyse orange flammer. Da t-BuLi også reagerer med de fleste opløsningsmidler, sælger kemiske virksomheder det som en fortyndet opløsning i ureaktiv heksan eller pentan, som begge også er brandfarlige. Det betyder, at hvis der er en organolithium brand, er der normalt en slags brændbart opløsningsmiddel i blandingen også.

kilde: Kris Image med tilladelse fra Naveen Sangji
Sheharbano Sangjis tragiske ulykke førte til kriminelle anklager og en ændring i laboratoriesikkerhedskulturen
den tragiske sag om UCLA-studerende Sheri Sangji, der døde i 2009 af større forbrændinger efter et eksperiment, der involverede store mængder t-BuLi, gik galt, skulle minde enhver kemiker om, at denne forbindelse skal behandles med respekt. Forskere, der arbejder med t-BuLi, skal overholde strenge sikkerhedsforanstaltninger: brug af kun små mængder og udførelse af reaktioner under udelukkelse af luft og fugt, mens de bærer ikke-brændbart tøj og har både en bekymret labmate og et nødbrusebad i nærheden er de absolutte minimumskrav til håndtering af t-BuLi sikkert.
mens alkyllithium er kraftige reagenser, er de også tilbøjelige til bivirkninger og danner ubrugelige biprodukter. Dette, ud over sikkerhedsproblemerne, er grunden til, at kemikere normalt udfører reaktioner ved -78 liter C og opretholder en inaktiv gasatmosfære i reaktionsbeholderne for at holde luft og fugt ude.
Eva Hevia
og jeg formoder, at den ultimative udfordring i denne type kemi er, hvordan vi kan bruge dem i en normal atmosfære uden tilstedeværelse af argon eller nitrogengas – under luft – og hvordan vi kan gøre disse reagenser kompatible med opløsningsmidler, der er miljøvenlige. Og det, vi har fundet, er, at hvis vi bruger dybe eutektiske opløsningsmidler som et alternativ – og et dybt eutektisk opløsningsmiddel er en ny type opløsningsmiddel, der er relateret til Ioniske væsker, som er miljøvenlige, der består af komponenter, der er biologisk nedbrydelige og biorenytbare – hvis vi bruger denne type opløsningsmidler, kan vi aktivere organolithiumopløsningsmidler på en sådan måde, at reaktionerne sker ekstremt hurtigt ved stuetemperatur. Fordi de er meget hurtige, behøver du ikke bruge en inert atmosfære, og du kan gøre disse reaktioner kompatible med vand eller fugt.
Katrina kr Kristmer
dybe eutektiske opløsningsmidler er blandinger af forskellige salte, der er flydende ved stuetemperatur. Mens de fleste ioniske forbindelser har et meget højt smeltepunkt (natriumchlorid for eksempel ure ind på lige over 800 grader), blander de rigtige salte i de rigtige mængder en eutektisk – en blanding, der smelter ved en meget lavere temperatur end dens individuelle komponenter. Disse temmelig usædvanlige opløsningsmidler er ikke – giftige og ret billige-en af forbindelserne Hevias team bruger er cholinchlorid, et kyllingefoderadditiv.
i dybe eutektiske opløsningsmidler er organolithiumreaktioner meget hurtigere end i noget andet opløsningsmiddel. Dette antyder, at allerede stærkt reaktive alkyl-lithiumforbindelser bliver mere reaktive i den salte opløsningsmiddelblanding, hvilket virker kontraintuitivt. Hvorfor havde Hevias team ikke behov for at kontrollere reaktionen ved at afkøle den eller udføre den under inert atmosfære?
Eva Hevia
når du arbejder i disse systemer, er den største fjende af dine reaktioner hydrolyse eller nedbrydning af dit organometalliske reagens. Så vi aktiverer det på en måde, så vi kan overvinde denne nedbrydningsvej. Samtidig indstiller vi deres selektivitet, så vi finder i den type reaktioner, vi ser på, at vi får bedre selektiviteter, end når vi bruger konventionelle opløsningsmidler.
Katrina kr Kristmer
fordi de består af ioner, er dybe eutektiske opløsningsmidler meget gode til at stabilisere ladede eller stærkt polære molekyler; men præcis hvordan de virker deres magi er ikke klart endnu. Hevia mener, at de salte opløsningsmidler også kunne tæmme andre mere livlige organometalliske reagenser.
Eva Hevia
nogle af vores indledende arbejde har vist, at vi kan bruge Grignard reagenser, som også er meget grundlæggende og meget vigtige i syntesen. Og noget af det arbejde, der i øjeblikket foregår i vores forskningsgrupper, viser, at disse opløsningsmidler også giver et stort potentiale for organiske reagenser, som igen er bredt anvendt i mange carbon-carbon-bindingsprocesser, og de er også meget reaktive i nærvær af luft og fugt. Så jeg tror, der er to måder at se på dette arbejde: for det første udvikler vi nye metoder til at anvende disse reagenser under miljøvenlige forhold, men for det andet – og det er noget, jeg virkelig vil understrege – aktiverer vi disse organometalliske reagenser, hvad enten det drejer sig om organolithium,-sinc eller-magnesium, for at få dem til at fungere endnu bedre, end når vi bruger inerte atmosfæreforhold eller flygtige organiske opløsningsmidler.
Katrina kr Kristmer
selvom kemikere stadig skal håndtere t-BuLi og dets brødre med omhu, kan dybe eutektiske opløsningsmidler hjælpe dem med at styre t-BuLi ‘ s kanonkuglereaktivitet med mere pillignende præcision.
Ben Valsler
det var Katrina Kr, der talte med Eva Hevia fra University of Strathclyde om tert-butyl lithium eller t-BuLi. Næste uge, Brian Clegg er tilbage med en familie af forbindelser med nogle om anvendelser.
Brian Clegg
de er bemærkelsesværdigt konstruktive – sjældent direkte til brug selv, men hver er en vigtig bidragyder af byggesten til andre forbindelser. Desværre kan nogle af disse slutprodukter dog bruges i kemiske våben.
Ben Valsler
Deltag Brian næste uge for at finde ud af mere. Indtil da, lad os vide, hvis der er noget, du gerne vil have os til at dække-email [email protected] eller kvidre @kemiverden. Jeg er Ben Valsler, Tak fordi du lyttede.