Profilaktyka wrzodów stresu: konsekwencje nadużywania i niewłaściwego użycia
US Pharm. 2011;36(10):73-76.
wydaje się, że prawie każdy pacjent przyjęty do szpitala w Stanach Zjednoczonych jest przepisywany albo jako inhibitor pompy protonowej (PPI) lub antagonista histaminy-2 (H2A) jako profilaktyka wrzodów stresu (SUP). Wrzody stresu to nadżerki śluzówki żołądka, które mogą rozwinąć się u pacjentów z poważną chorobą lub ciężkim urazem. W przeciwieństwie do wrzodów trawiennych, które mają tendencję do rozwoju w antrum lub dwunastnicy, związane ze stresem urazy błony śluzowej zwykle występują w obszarach produkujących kwas żołądka (to znaczy, corpus i dna oka).1 Wrzody stresu, w przeciwieństwie do wrzodów trawiennych, mają tendencję do powodowania krwawienia z przewodu pokarmowego i nie są związane z bólem brzucha. Zmiany błony śluzowej związane ze stresem uszkodzenia błony śluzowej obejmują głównie małe nadżerki, które nie prowadzą do krwawienia, ale mogą rozwinąć się w głębsze wrzody, które powodują krwawienie.
kilka czynników przyczynia się do powstawania wrzodów stresowych, w tym nadmierne wydzielanie kwasu; zmiana normalnych mechanizmów ochronnych, takich jak wydzieliny śluzu i wodorowęglanów; uwalnianie mediatorów, takich jak metabolity kwasu arachidonowego, cytokiny i wolne rodniki tlenowe; i niedokrwienie układu pokarmowego.2 te nadżerki mogą wystąpić szybko (£24 godziny przyjęcia) lub trwać dłużej (>10-14 dni).2 wrzody stresowe i związane z nimi krwawienia powodują znaczną zachorowalność i śmiertelność u pacjentów w stanie krytycznym. W jednym badaniu śmiertelność wynosiła 46% u pacjentów w stanie krytycznym z krwawieniem z przewodu pokarmowego w porównaniu z 21% u pacjentów bez krwawienia (P <.001).3 inne badania potwierdziły tę wysoką śmiertelność.4, 5
Duże badania wykazały, że najsilniejszymi czynnikami ryzyka wystąpienia krwawienia związanego ze stresem w obrębie przewodu pokarmowego są przedłużona Wentylacja mechaniczna i koagulopatia.4 ryzyko wzrasta wraz ze wzrostem liczby dni wentylacji mechanicznej i długości pobytu na OIOM.Inne czynniki ryzyka to niedawna poważna operacja, poważny uraz, ciężkie oparzenia, uraz głowy, choroba wątroby lub nerek przy przyjęciu, posocznica i niedociśnienie.1 Tabela 1 zawiera pełną listę czynników ryzyka.

terapia profilaktyczna
chociaż udowodniono, że jest wysoce skuteczna w zmniejszaniu ryzyka zarówno jawnego, jak i klinicznie istotnego krwawienia ze śluzówki związanego ze stresem, sama terapia profilaktyczna nie zmniejsza ogólnego wskaźnika śmiertelności.Mimo to przepisywanie PPIs lub H2As jako SUP jest poparte literaturą i wytycznymi dla populacji pacjentów w stanie krytycznym. W ostatnich latach zwiększyło się stosowanie SUP u pacjentów bez intensywnej terapii-często bez wskazań. Wiele badań wykazało nadużywanie leków hamujących kwasy (ASD); aż 71% przyjętych pacjentów przepisuje się ASD, a wielu z nich jest błędnie odprowadzanych za pomocą tych środków.8 wielu pacjentów są niewłaściwie przepisywane ASDs w społeczności, i niewiele się robi, aby przerwać te leki podczas hospitalizacji. Ponadto, pacjenci przyjmujący dwa razy na dobę PPI w leczeniu objawów refluksu żołądkowo-przełykowego (GERD) często nie są poddawani terapii jednodniowej, gdy objawy te nie są bezobjawowe.9
nadużywanie i niewłaściwe stosowanie ASD może spowodować szkodę dla pacjenta i zwiększyć koszty dla systemu opieki zdrowotnej. Liczba potrzebna do leczenia (NNT), aby zapobiec pojedynczemu epizodowi klinicznie istotnego krwawienia z przewodu pokarmowego na OIOM przekracza 900; NNT jest nieznany w przypadku leczenia poza OIOM, ale oczekuje się, że będzie znacznie wyższy.9 w retrospektywnym badaniu kohortowym w szpitalu akademickim koszty szpitalne dla SUP w Ustawieniach nie-OIOM wyniosły 44 000 USD rocznie, a koszty apteki ambulatoryjnej wyniosły prawie 68 000 USD, gdy leki były kontynuowane po naładowaniu, dla łącznych rocznych szacowanych wydatków w wysokości prawie 112 000 USD.10 można było temu łatwo zapobiec.
w świetle tych statystyk SUP nadal jest nadpisywany. W przekrojowym internetowym badaniu oceniającym wiedzę lekarzy, przekonania i zachowania dotyczące przepisywania SUP u pacjentów bez intensywnej terapii, obawy przed krwawieniem z przewodu pokarmowego i prawne reperkusje nie przepisywania SUP były związane z wyższym poziomem przepisywania, podczas gdy wiedza o wskazaniach SUP i obawy o skutki uboczne były związane z niskim zachowaniem przepisywania.11 mniej niż połowa lekarzy mogła zidentyfikować pojedynczy efekt uboczny leczenia PPI.11 wielu praktyków postrzega te leki jako nieszkodliwe, ale badania sugerują, że terapia PPI i H2A jest silnie związana z większym prawdopodobieństwem zakażenia Clostridium difficile (CDI) i zwiększonym współczynnikiem nawrotów.12,13 inne często pomijane zagrożenia związane z tą terapią obejmują hipomagnezemię; niedobór witaminy B12; infekcje górnych dróg oddechowych, w tym zapalenie płuc nabyte przez społeczność (CAP) i zapalenie płuc nabyte przez szpital (HAP); złamania stawu biodrowego, kręgosłupa i nadgarstków; oraz zmienione wchłanianie leków zależnych od pH.
CDI: Toksyna wytwarzana przez c difficile, beztlenowe, zarodniotwórcze, Gram-dodatnie bakterie, jest główną przyczyną biegunki i zapalenia jelita grubego w hospitalizowanych pacjentów, który zwiększył częstość występowania, nasilenie, i śmiertelność w ostatnich latach. Około 3 milionów przypadków występuje rocznie w USA, a koszty opieki zdrowotnej przekraczają 1,1 miliarda dolarów rocznie.14,15 C16 CDI jest zamieszany w 20% do 30% wszystkich przypadków biegunki związanej z antybiotykiem, 50% do 75% przypadków zapalenia jelita grubego związanego z antybiotykiem i ponad 90% przypadków rzekomobłoniastego zapalenia jelita grubego związanego z antybiotykiem u pacjentów hospitalizowanych.
pomimo lepszej kontroli przepisywania antybiotyków i poprawy higieny szpitalnej, liczba przypadków CDI nadal rośnie.Przyczyniły się do tego poprawiona diagnoza, nadpobudliwe szczepy i starzenie się populacji, ale te czynniki Nie w pełni wyjaśniają zakres ostatnich wzrostów.Najczęstsze czynniki ryzyka CDI obejmują wiek powyżej 65 lat, bieżącą i nawracającą hospitalizację, niedawną operację przewodu pokarmowego, immunosupresję, wcześniejszą CDI, pobyt w domu opieki lub zakładzie opieki długoterminowej oraz stosowanie antybiotyków. Stosowanie antybiotyków jest największym czynnikiem ryzyka rozwoju CDI, ale często nie można go uniknąć u pacjentów z infekcjami. Mniej powszechnym, ale bardziej modyfikowalnym czynnikiem ryzyka jest stosowanie ASD u pacjentów hospitalizowanych, u których leki te nie są wskazane.
kwas żołądkowy jest niespecyficznym mechanizmem ochronnym przed spożywanymi patogenami. Żołądek jest zwykle wolny od bakterii, z wyjątkiem Helicobacter pylori, która jest wyjątkowo przystosowana do radzenia sobie z kwasowością żołądka.19 C difficile jest przenoszony przez spożycie, a jego stosunkowo stabilne zarodniki kiełkują w jelicie cienkim i okrężnicy. Komórki wegetatywne C difficile, w przeciwieństwie do zarodników, są zwykle zabijane w środowisku o niskim pH żołądka; stwierdzono jednak, że pozostają żywotne w treści żołądkowej pacjentów przyjmujących ASDs. Badania przeprowadzone na modelach zwierzęcych wykazały, że zarodniki C. C. przekształcają się w komórki wegetatywne w ciągu 1 godziny po spożyciu. Jest prawdopodobne, że transformacja ta może wystąpić w żołądku, jeśli pH jest wyższe lub w przypadku wolniejszego czasu tranzytu żołądka.
kilka badań wykazało związek między stosowaniem PPI lub H2A a CDI. Ostatnie retrospektywne badanie kohortowe wykazało, że nawracające CDI występowało częściej u pacjentów narażonych na PPI niż u pacjentów nienaświetlonych (25,2% vs 18,5%) i że stosowanie PPI podczas leczenia CDI wiązało się ze zwiększonym o 42% ryzykiem nawrotu.Największe ryzyko występowało u 12 pacjentów w wieku powyżej 80 lat.12 niedawna analiza danych dotyczących wypisów pacjentów z trzeciego ośrodka medycznego w okresie 5 lat wykazała, że ryzyko wystąpienia szpitalnej CDI było dodatnio skorelowane z poziomem supresji kwasów i było najwyższe u pacjentów otrzymujących leczenie PPI częściej niż raz na dobę, co sugeruje wpływ na odpowiedź dawki na ryzyko szpitalnej CDI.13
: Chociaż wyniki badań były niespójne, kilka badań wykazało związek między stosowaniem ASD a zwiększonym ryzykiem zakażeń dróg oddechowych i CAP. Niedawny przegląd systematyczny i metaanaliza sugerowały, że stosowanie PPIs i H2As wiąże się z większym ryzykiem zarówno CAP, jak i HAP, szacując wystąpienie jednego przypadku zapalenia płuc na każde 200 pacjentów leczonych ASD.20 biorąc pod uwagę, że 40% do 70% pacjentów przyjmujących szczepionkę ASD, wielkość zachorowalności i śmiertelności HAP może być w pełni doceniona. Największy wzrost ryzyka zapalenia płuc związanego z PPIs obserwowano w pierwszym tygodniu stosowania.
podobnie jak w przypadku zakażeń jelitowych, uważa się, że ASD zwiększa ryzyko zapalenia płuc poprzez hamowanie wydzielania kwasu żołądkowego, umożliwiając w ten sposób przerost bakterii i kolonizację. Bakterie mogą być następnie przenoszone do płuc przez aspirację.U pacjentów z wentylacją mechaniczną kolonizacja jamy ustnej i gardła organizmami gram-ujemnymi może prowadzić do kolonizacji żołądka.19 inna teoria głosi, że adenozynotrifosfataza wodorowo-potasowa jest obecna nie tylko w komórkach ciemieniowych żołądka, ale także w drogach oddechowych.Hamowanie tego enzymu przez PPI może sprzyjać rozwojowi bakterii w drogach oddechowych, co prowadzi do zwiększonego ryzyka zapalenia płuc.20 wreszcie, badania in vitro wykazały, że ASD może upośledzać funkcję neutrofilów i aktywność naturalnych komórek zabójcy.
pacjenci w wieku powyżej 65 lat są narażeni na zwiększone ryzyko zapalenia płuc z powodu ASD. Nie tylko pacjenci w podeszłym wieku są na ogół podchloryczni z powodu procesu starzenia się, ale stosowanie PPI lub H2A jest powszechne w tej grupie; do 5% regularnie przyjmuje te leki, a wysoki odsetek hospitalizowanych pacjentów w podeszłym wieku otrzymuje SUP.21 ponadto wiele PPIs i H2A nie wymaga recepty, co skutkuje zwiększonym i niemonitorowanym stosowaniem, często przez długi czas bez nadzoru lekarskiego.
Inne zagrożenia: oprócz CDI, z ASD związane były inne zakażenia jelitowe—w szczególności z gatunkami Salmonella i Campylobacter. Zarówno Campylobacter, jak i Salmonella są drobnoustrojami wrażliwymi na kwasy. Infekcje pasożytnicze są również związane z supresją kwasu, zwłaszcza giardiasis i strongyloidiasis.Jak wspomniano wcześniej, kwas żołądkowy jest ważny w zabijaniu spożywanych organizmów, ale podwyższone pH żołądka może mieć inne negatywne skutki dla obrony gospodarza przewodu pokarmowego, takie jak opóźnione opróżnianie żołądka, zwiększona translokacja bakterii, zmniejszona lepkość śluzu żołądka i zmiany w normalnej florze drobnoustrojów.
interakcje z lekami są kolejnym problemem związanym z supresją kwasu. Digoksyna, nifedypina, indynawir, midazolam, dydanozyna, alendronian, metadon, aspiryna) mogą mieć wpływ zarówno na PPI, jak i H2A, co powoduje zwiększenie szybkości wchłaniania.Ketokonazol, cefpodoksym, dipirydamol, atazanawir, itrakonazol).Istnieje wiele interakcji związanych z CYP450 między PPI a innymi lekami. Potencjalna interakcja pomiędzy PPIs i klopidogrelem przyciąga uwagę ze względu na możliwe poważne działania niepożądane. Alarm bezpieczeństwa FDA w listopadzie 2009 r.zalecił unikanie stosowania omeprazolu lub ezomeprazolu z klopidogrelem, ostrzegając, że interakcja z udziałem CYP może zmniejszyć skuteczność klopidogrelu.22 Z powodu niewystarczających danych FDA nie wydała żadnych szczegółowych zaleceń dotyczących innych PPI.
zgłaszano kilka przypadków pacjentów z hipomagnezemią, a następnie hipokaliemią i hipokalcemią, u których występowały zagrażające życiu objawy wymagające hospitalizacji. Większość z tych przypadków była związana z długotrwałym stosowaniem PPI. Mechanizm tego działania niepożądanego nie jest znany. U pacjentów z hipomagnezemią wywołaną PPI nie stwierdzono widocznego złego wchłaniania magnezu ani wyniszczenia magnezu przez nerki.Chociaż hipomagnezemia jest rzadka, ponieważ jest tak zagrażająca życiu dostawcy są zachęcani do uważnego obserwowania niewyjaśnionej hipomagnezemii, hipokaliemii lub hipokalcemii u użytkowników PPI.
stosowanie PPIs przez 12 miesięcy lub dłużej było związane z niedoborem witaminy B12, szczególnie u pacjentów w podeszłym wieku.9 kwasowość żołądka i pepsyna umożliwiają uwalnianie spożywanej witaminy B12 ze stanu wiązania z białkami; dlatego zmniejszenie stężenia kwasu żołądkowego może prowadzić do złego wchłaniania i niedoboru witaminy B12.Wyniki badań były niespójne i potrzebne są większe badania, aby określić związek między stosowaniem PPI a złym wchłanianiem witaminy B12 i późniejszym niedoborem. Słabe wchłanianie żelaza w diecie było również związane z terapią PPI, ale obecne dane są słabe. Kwas żołądkowy ułatwia wchłanianie żelaza nonheme poprzez redukcję żelaza żelazowego do bardziej rozpuszczalnej postaci żelaza, a także zwiększa dysocjację żelaza i soli z spożywanego pokarmu.Istnieje kilka przypadków, ale nie przeprowadzono prospektywnych badań w tej dziedzinie.
długotrwałe stosowanie PPI wiązało się ze zwiększoną częstością złamań. Możliwe mechanizmy obejmują zmniejszone wchłanianie wapnia w bardziej zasadowym środowisku żołądka i upośledzenie przebudowy kości z powodu zmniejszonej aktywności osteoklastów, co prowadzi do zahamowania naprawy mikropęknięć.22 po raz kolejny badania są niespójne, ale istniejące dowody wystarczyły, aby skłonić FDA do zmiany oznakowania PPI w maju 2010 r., aby uwzględnić nowe informacje dotyczące bezpieczeństwa dotyczące możliwego zwiększonego ryzyka złamań stawu biodrowego, nadgarstka i kręgosłupa.Ryzyko złamań może być bardziej istotne klinicznie u pacjentów z osteoporozą lub innymi czynnikami ryzyka złamań, takimi jak stosowanie sterydów. Zachęca się lekarzy do rozważenia ryzyka i korzyści ze stosowania PPI u pacjentów wrażliwych. Jeśli suplementy wapnia są przepisywane użytkownikom PPI, powinny być w postaci rozpuszczalnej, takiej jak cytrynian, a nie węglan.22
właściwe stosowanie
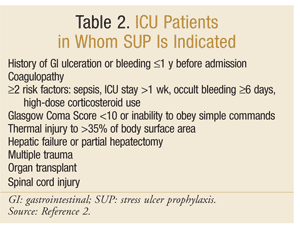
Amerykańskie Towarzystwo farmaceutów systemów zdrowotnych opracowało jedną z najbardziej kompleksowych wytycznych dotyczących SUP. Obecne wytyczne terapeutyczne zostały opublikowane w 1999 roku, z aktualizacją w toku w tym piśmie.Nie zaleca się stosowania SUP u pacjentów spoza intensywnej terapii; profilaktyka jest zalecana tylko u pacjentów z intensywną opieką medyczną, którzy wymagają mechanicznej wentylacji przez ponad 48 godzin, u których w ciągu 1 roku przed przyjęciem stwierdzono owrzodzenie przewodu pokarmowego lub krwawienie w wywiadzie lub u których występuje koagulopatia. Zaleca się również profilaktykę u pacjentów OIOM z co najmniej dwoma z następujących czynników ryzyka: posocznica, pobyt OIOM przekraczający 1 tydzień, utajone krwawienie trwające 6 dni lub dłużej oraz stosowanie dużych dawek kortykosteroidów (hydrokortyzon >250 mg/dobę lub równoważny). Dodatkowo, SUP jest zalecany w szczególnych populacjach OIOM, takich jak pacjenci ze śpiączką Glasgow <10 (lub niezdolnością do przestrzegania prostych poleceń), uszkodzeniem termicznym >35% powierzchni ciała, niewydolnością wątroby lub częściową hepatektomią, wielokrotnym urazem, przeszczepem lub uszkodzeniem rdzenia kręgowego.2 zalecenia przedstawiono w tabeli 2.
wniosek: rola farmaceuty
wysiłki klinicystów mające na celu ograniczenie stosowania ASD u pacjentów nie będących OIOM mogą zapobiec znaczącej zachorowalności pacjentów i zmniejszyć zarówno koszty szpitalne, jak i Koszty ogólnego systemu opieki zdrowotnej. Ważne jest, aby dokładnie rozważyć ryzyko i korzyści z ASD przed użyciem tych leków w warunkach szpitalnych. Szczególną uwagę należy zwrócić na pacjentów już narażonych na ryzyko zapalenia płuc, takich jak osoby w podeszłym wieku, osoby z przewlekłą chorobą płuc oraz osoby przyjmujące leki immunosupresyjne. Należy dołożyć wszelkich starań, aby krytycznie ocenić terapię supresją kwasu u pacjentów i w miarę możliwości przerwać leczenie. Jeśli wskazana jest SUP, pacjent powinien otrzymać najmniejszą możliwą dawkę.
farmaceuci mogą pomóc w powstrzymaniu stosowania ASD, identyfikując pacjentów, którzy są niewłaściwie przepisywani tymi lekami, i mogą być pomocni w edukowaniu lekarzy o tym, którzy pacjenci powinni otrzymywać SUP. Farmaceuci zajmujący się przetwarzaniem leków wydzielinowych mogą pomóc zapewnić, że pacjenci nie są wysyłani do domu na terapię supresyjną bez odpowiedniego wskazania. Niestety, środki podjęte w celu zapobiegania owrzodzeniom stresu u hospitalizowanych pacjentów stworzyły nowy problem, a współpracując z zespołem opieki zdrowotnej może pomóc w zapobieganiu dalszej niepotrzebnej chorobowości, egzekwując wytyczne w swojej instytucji.
1. Spirt MJ. Choroby błony śluzowej związane ze stresem: czynniki ryzyka i terapia profilaktyczna. Clin Ther. 2004;26:197-213.
2. Wytyczne terapeutyczne ASHP dotyczące profilaktyki wrzodów stresu. Komisja ASHP ds. terapii i zatwierdzona przez Zarząd ASHP w dniu 14 listopada 1998 r. Am J Health Syst Pharm. 1999;56:347-379.
3. Cook DJ, Griffith LE, Walter SD, et al. Przypisana śmiertelność i długość pobytu na oddziale intensywnej terapii w przypadku klinicznie istotnych krwawień z przewodu pokarmowego u pacjentów w stanie krytycznym. Opieka Krytyczna. 2001;5:368-375.
4. Cook DJ, Fuller HD, Guyatt GH, et al. Czynniki ryzyka krwawienia z przewodu pokarmowego u pacjentów w stanie krytycznym. Canadian Critical Care Trials Group. N Engl J Med. 1994;330:377-381.
5. Zuckerman GR, Szuman R. cele terapeutyczne i możliwości leczenia w profilaktyce zespołu wrzodowego stresu. Am J Med. 1987;83:29-35.
6. Harris SK, Bone RC, Ruth WE. Krwotok żołądkowo-jelitowy u pacjentów na oddziale intensywnej terapii układu oddechowego. Klatka piersiowa. 1977;72:301-304.
7. Sesler JM. Związane ze stresem choroby błony śluzowej na oddziale intensywnej terapii: aktualizacja profilaktyki. AACN Adv Crit Care. 2007;18:119-128.
8. Grube RR, May DB. Profilaktyka owrzodzeń stresowych u pacjentów hospitalizowanych nie na oddziałach intensywnej terapii. Am J Health Syst Pharm. 2007;64:1396-1400.
9. Heidelbaugh JJ, Goldberg KL, Incomi JM. Nadmierne wykorzystanie inhibitorów pompy protonowej: przegląd opłacalności i ryzyka w PPI. Am J Gastroenterol. 2009; 104 (suppl 2): S27-S32.
10. Heidelbaugh JJ, właśc. Skala i ekonomiczny wpływ niewłaściwego stosowania profilaktyki owrzodzeń wywołanych stresem u pacjentów hospitalizowanych bez intensywnej terapii. Am J Gastroenterol. 2006;101:2200-2205.
11. Hussain s, Stefan m, Visintainer P, Rothberg M. dlaczego lekarze przepisują profilaktykę wrzodów stresowych pacjentom medycyny ogólnej? South Med J. 2010;103:1103-1110.
12. Linsky a, Gupta K, Lawler EV, et al. Inhibitory pompy protonowej i ryzyko nawracającego zakażenia Clostridium difficile. Arch Intern Med. 2010;170:772-778.
13. Howell MD, Novack V, Grgurich P, et al. Jatrogenna supresja kwasu żołądkowego i ryzyko zakażenia szpitalnego Clostridium difficile. Arch Intern Med. 2010;170:784-790.
14. Kyne L, Hamel MB, Polavaram R, Kelly CP. Koszty opieki zdrowotnej i śmiertelność związana z biegunką szpitalną spowodowaną Clostridum difficile. Clin Infect Dis. 2002;34:346-353.
15. Schroeder pani Clostridium difficile-związana z biegunką. Jestem Lekarzem. 2005;71:921-928.
16. McMaster-Baxter NL, Musher DM. Clostridium difficile: najnowsze odkrycia epidemiologiczne i postępy w terapii. Farmakoterapia. 2007;27:1029-1039.
17. Kelly CP, Pothoulakis C, LaMont JT. Clostridium difficile colitis. N Engl J Med. 1994;330:257-262.
18. Cunningham R, Dial S. czy nadmierne stosowanie inhibitorów pompy protonowej napędza obecną epidemię biegunki związanej z Clostridium difficile? J Hosp Infect. 2008;70:1-6.
19. Vakil N. hamowanie kwasów i infekcje poza przewodem pokarmowym. Am J Gastroenterol. 2009; 104: S17-S20.
20. Eom CS, Jeon CY, Lim JW, et al. Stosowanie leków hamujących kwasy i ryzyko zapalenia płuc: przegląd systematyczny i metaanaliza. CMAJ. 2011;183:310-319.
21. Eurich DT, Sadowski CA, Simpson SH, et al. Nawracające zapalenie płuc nabyte we Wspólnocie u pacjentów rozpoczynających stosowanie leków hamujących kwasy. Am J Med. 2010;123:47-53.
22. Sheen E, Triadafilopoulos G. niekorzystny wpływ na długotrwałą terapię inhibitorem pompy protonowej. Dig Dis Sci. 2011;56:931-950.
23. Wybierz użycie inhibitora pompy protonowej i infekcje jelitowe. Am J Gastroenterol. 2009; 104 (suppl 2): S10-S16.
24. Lahner e, Annibale B, Della Fave G. przegląd systematyczny: zaburzenia wchłaniania leku związane z jednoczesnym podawaniem terapii przeciwwydzielniczej. Aliment Pharmacol Ther. 2009;29:1219-1229.
25. American Society of Health-System Pharmacists. Terapeutyczne guidelines.www.ashp.org/Import/practiceandpolicy/PolicyPositionsGuidelinesBestPractices/BrowsebyDocumentType/TherapeuticGuidelines.aspx [dostęp 19 września 2011].